光化学烟雾是汽车尾气在紫外线作用下生成的有害浅蓝色烟雾,由氮的氧化物和烃类等一次污染物,与它们发生一系列光化学反应生成的臭氧、醛类、过氧乙酰硝酸酯(PAN)等二次污染物组成。光化学烟雾导致眼睛及粘膜受刺激,引发呼吸道疾病,严重时使人头痛、呕吐,甚至死亡。下列叙述中错误的是( )

A. 光化学烟雾的分散剂为空气
B. NO2为酸性氧化物
C. O2转化成O3的反应为非氧化还原反应
D. 汽车节能减排措施可以缓解光化学烟雾带来的污染
高二化学单选题中等难度题
光化学烟雾是汽车尾气在紫外线作用下生成的有害浅蓝色烟雾,由氮的氧化物和烃类等一次污染物,与它们发生一系列光化学反应生成的臭氧、醛类、过氧乙酰硝酸酯(PAN)等二次污染物组成。光化学烟雾导致眼睛及粘膜受刺激,引发呼吸道疾病,严重时使人头痛、呕吐,甚至死亡。下列叙述中错误的是( )

A. 光化学烟雾的分散剂为空气
B. NO2为酸性氧化物
C. O2转化成O3的反应为非氧化还原反应
D. 汽车节能减排措施可以缓解光化学烟雾带来的污染
高二化学单选题中等难度题
光化学烟雾是汽车尾气在紫外线作用下生成的有害浅蓝色烟雾,由氮的氧化物和烃类等一次污染物,与它们发生一系列光化学反应生成的臭氧、醛类、过氧乙酰硝酸酯(PAN)等二次污染物组成。光化学烟雾导致眼睛及粘膜受刺激,引发呼吸道疾病,严重时使人头痛、呕吐,甚至死亡。下列叙述中错误的是( )

A. 光化学烟雾的分散剂为空气
B. NO2为酸性氧化物
C. O2转化成O3的反应为非氧化还原反应
D. 汽车节能减排措施可以缓解光化学烟雾带来的污染
高二化学单选题中等难度题查看答案及解析
上世纪80年代后期人们逐渐认识到,NO在人体内起着多方面的重要生理作用。下列关于NO的说法不正确的是
A. NO对臭氧层有破坏作用 B. NO是造成光化学烟雾的因素之一
C. NO是汽车尾气的有害成分之一 D. NO分子所含电子总数为偶数
高二化学单选题中等难度题查看答案及解析
氮氧化物(用NOx表示)是大气污染的重要因素,根据NOx的来源和性质特点,已开发出多种化学治理其污染的方法。
(1)汽车尾气中的NO2是城市大气污染的主要污染物之一。在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染。反应过程为①2NO2→2NO+2O,②2NO+O2→2NO2,③O+O2→O3。下列关于该反应过程及生成物的叙述正确的是____(填序号)。
A.NO2起催化作用
B.NO起催化作用
C.NO2只起氧化作用
D.O3与O2互为同素异形体
(2)汽车尾气中的CO来自于____,NO来自于____。
(3)汽车尾气中的CO、NOx可在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:_____。
(4)工业尾气中氮氧化物常采用碱液吸收法处理。NO2被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为1∶1,该反应的离子方程式为____;1molNO2被完全吸收时,转移电子的物质的量为____。NO与NO2按物质的量之比1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式为____。
高二化学综合题中等难度题查看答案及解析
下列做法与可持续发展理念不符合的是
A. 加大清洁能源的开发利用,提高资源的利用率
B. 催化处理汽车尾气,减轻氮氧化物污染和光化学烟雾
C. 对工业废水、生活污水净化处理,减少污染物的排放
D. 加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求
高二化学单选题简单题查看答案及解析
高二化学选择题中等难度题查看答案及解析
下列有关城市各项污染源与其造成的恶果对应正确的是( )
A.汽车尾气——光化学烟雾 工业废气——酸雨 工业废水——“公害病”
B.汽车尾气——酸雨 工业废气——“公害病” 工业废水——光化学烟雾
C.汽车尾气——“公害病” 工业废气——酸雨 工业废水——光化学烟雾
D.汽车尾气——光化学烟雾 工业废气——“公害病” 工业废水——酸雨
高二化学选择题简单题查看答案及解析
汽车尾气中的NO(g) 是导致光化学烟雾和破坏臭氧层的重要源头之一。现拟用下列方法处理NO,根据题意回答下列问题:
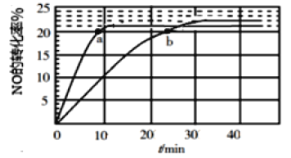
(1)采用某种催化剂催化分解NO,发生反应2NO(g)N2(g)+O2(g),在T1 ℃ 和T2 ℃时(T1>T2)NO的转化率随时间变化的结果如图所示。

① 反应 2NO(g)N2(g)+O2(g) 为(填“吸热”或“放热”)____________反应。
② T2℃时,反应的平衡常数K=__________(保留2位小数)。
③ 在T1 ℃下,要提高NO转化率,可采取的措施是_________________________
④ 比较a、b处反应速率大小:va(正)________ vb(逆)(填“大于”“小于”或“等于”)。已知反应速率 v正=k正x2(NO),v逆=k逆 x(N2)·x(O2),k正、k逆 分别为正、逆向反应速率常数,x为物质的量分数,计算b点处v(正)/v(逆)=__________(保留1位小数)。
(2)臭氧也可用于处理NO.O3氧化NO结合水洗可产生HNO3和O2,写出该反应的化学方程式___________________,每生成1mol的HNO3转移_______mol电子.
高二化学综合题困难题查看答案及解析
汽车尾气中的NO(g)是导致光化学烟雾和破坏臭氧层的重要源头之一。现拟用下列方法处理NO,根据题意回答下列问题:
(1)采用某种催化剂催化分解NO,发生反应2NO(g)N2(g)+O2(g),在T1℃和T2℃时(T1>T2)NO的转化率随时间变化的结果如图所示。
①反应2NO(g)N2(g)+O2(g)为____________(填“吸热”或“放热”)反应。
②T2℃时,反应的平衡常数K=__________(保留2位小数)。
③在T1℃下,要提高NO转化率,可采取的措施是_________________________
④比较a、b处反应速率大小:υa(正)________υb(逆)(填“大于”“小于”或“等于”)。已知反应速率υ正=k正x2(NO),υ逆=k逆x(N2)·x(O2),k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算b点处=__________(保留1位小数)。
(2)臭氧也可用于处理NO,O3氧化NO结合水洗可产生HNO3和O2,若生成1 mol的HNO3则转移_______ mol电子。
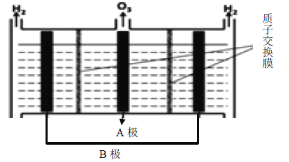
(3)O3可由电解稀硫酸制得,原理如下图所示,图中阴极为________(填“A”或“B”),阳极(惰性电极)的电极反应式为___________________________________。
高二化学综合题中等难度题查看答案及解析
汽车尾气含有烃类、CO、NO、SO2等物质,是城市空气的主要污染源。在汽车排气管上加装"催化转化器"可使CO和NO反应生成无毒气体。下列说法错误的是( )
A. CO和NO反应的化学方程式为:2CO + 2NO 2CO2 + N2
B. 此法的缺点是由于CO2的增多会大大提高空气的酸度
C. 汽车改用天然气为燃料或用氢气为能源,可减少对空气的污染
D. CO和NO均可与人体血红蛋白结合而使人中毒
高二化学选择题中等难度题查看答案及解析
减少汽车尾气造成环境污染的方法之一是在汽车的排气管上安装“催化转化器”(用铂、钯合金作催化剂),它的作用是使CO、NO反应生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧和SO2的转化。
(1)写出CO与NO反应的化学方程式:________________。
(2)“催化转化器”的缺点是在一定程度上提高空气的酸度,其原因是___________。
高二化学填空题中等难度题查看答案及解析