-
通过下列两步实验测定草酸晶体(H2C2O4·xH2O)中结晶水x的值:
①称取2.52 g草酸晶体,配制成100 .00 mL溶液。
②取25.00 mL所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为0.100 mol·L-1 KMnO4溶液进行滴定。其反应原理是:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
请回答下列问题:
(1)实验②中,KMnO4应装在______滴定管中(填“酸式”、“碱式”)。
(2)如图表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积______。
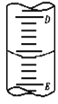
A.是amL B.是(50-a)mL
C.一定大于amL D.一定大于(50-a)mL
(3)判断达到滴定终点的现象是_____________________________;
若滴定终点时,共用去KMnO4溶液20.00 mL,则x =__________。
(4)若在滴入KMnO4溶液之前滴定管的尖嘴部分有气泡,滴定结束后气泡消失,则会使测定结果______(偏高、偏低或无影响)。
-
草酸(H2C2O4)是一种重要的化工产品.草酸晶体的组成可用H2C2O4•xH2O表示,为了测定x值进行如下实验:
①称取1.260g纯草酸晶体,将其配制成100.00mL水溶液为待测液.
②取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O.试回答:
(1)实验中需要用到的玻璃仪器有:滴定管、100mL量筒、烧杯、胶头滴管、锥形瓶、玻璃棒,其中还缺少的仪器有(填名称及规格)______.
(2)滴定时,将KMnO4标准液装在如图中的______(填“甲”或“乙”)滴定管中.达到滴定终点的现象是______.
(3)在滴定过程中若用去0.1000mol/L的KMnO4溶液10.00mL(已取三次平均值),则所配制的草酸溶液的物质的量浓度为______mol/L,由此可计算x的值是______.
(4)①若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得x值会______填“偏大”、“偏小”或“无影响”,下同).
②若滴定终点时仰视滴定管刻度,则由此测得的x值会______.

-
化学学习小组进行实验测定H2C2O4·xH2O 中x值。已知:M(H2C2O4)=90 g·mol-1
①称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液;
②取25.00mL 待测液放入锥形瓶中,再加入适量稀H2SO4;
③用浓度为 0.05 000 mol·L-1的 KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式__________。
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是__________(选填 a、b)。
a. 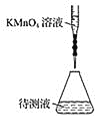 b.
b. 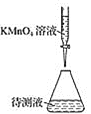
(3)由图可知消耗KMnO4溶液体积为_______mL。

(4)滴定过程中眼睛应注视________。
(5)通过上述数据,求得x=______。以标准KMnO4溶液滴定样品溶液的浓度,未用标准KMnO4溶液润洗滴定管,引起实验结果______ (偏大、偏小或没有影响) 。
-
(5分)草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,做了如下实验:
①称取W g纯草酸晶体,将其配制成100.0 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为a mol•L-1的KMnO4标准溶液进行滴定,滴定时发生的反应为:
2KMnO4+5H2C2O4+3H2SO4=====K2SO4+2MnSO4+l0CO2  +8H2O
+8H2O
请回答:
(1)滴定时,将KMnO4标准液装在________滴定管中,操作时用________手拿锥形瓶。
(2)若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会________(填“偏大”“偏小”或“不变’’)。
(3)假设滴定终点时,用去V mL KMnO4溶液,则待测草酸溶液的物质的量浓度为________mol•L-1。
-
用氧化还原滴定法测定某种草酸晶体(H2C2O4·X H2O)中结晶水分子数的实验步骤如下:
①用分析天平称取草酸晶体1.260g,将其配制成100.00mL待测草酸溶液;
②用移液管移取25.00mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化
③用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,三次结果如下:
| 第一次滴定 | 第二次滴定 | 第三次滴定 |
| 待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
| 标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
已知:H2C2O4的相对分子质量为90。
回答下列问题:
(1)滴定时,KMnO4标准溶液应该装在_____ (填“酸式”或“碱式”)滴定管中。
(2)H2C2O4在溶液中与KMnO4溶液反应的化学方程式是______________
(3)到达滴定终点的标志是____________。
(4)根据上述数据计算X=________________。
(5)误差分析(填:偏高、偏低、无影响):
①若滴定开始时仰视滴定管刻度,滴定结束时俯视滴定管刻度,则X值_________;
②若滴定管水洗后直接加入KMnO4标准溶液,则X值_______。
-
用氧化还原滴定法测定某种草酸晶体(H2C2O4·X H2O)中结晶水分子数的实验步骤如下:
①用分析天平称取草酸晶体1.260g,将其配制成100.00mL待测草酸溶液;
②用移液管移取25.00mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化
③用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,三次结果如下:
| 第一次滴定 | 第二次滴定 | 第三次滴定 |
| 待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
| 标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
已知:H2C2O4的相对分子质量为90。
回答下列问题:
(1)滴定时,KMnO4标准溶液应该装在_____ (填“酸式”或“碱式”)滴定管中。
(2)H2C2O4在溶液中与KMnO4溶液反应的化学方程式是______________
(3)到达滴定终点的标志是____________。
(4)根据上述数据计算X=________________。
(5)误差分析(填:偏高、偏低、无影响):
①若滴定开始时仰视滴定管刻度,滴定结束时俯视滴定管刻度,则X值_________;
②若滴定管水洗后直接加入KMnO4标准溶液,则X值_______。
-
草酸晶体的化学式可表示为H2C2O4·xH2O,为测定x值进行下列实验:
(1)称取wg草酸晶体,配成100.00 mL溶液。
(2)取25.00mL所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为a mol/LKMnO4溶液滴定。KMnO4+H2C2O4+H2SO4→K2SO4+MnSO4+CO2↑+H2O(未配平)
回答下列问题:
①滴定时,KMnO4溶液应盛在__________(填酸式或碱式)滴定管中;
②若滴定用的KMnO4溶液因放置而变质,浓度偏低,则根据实验求出的x值______(填偏高、偏低或无影响);
③滴定终点时,锥形瓶内溶液颜色变化是_____________________;
④若滴定终点时,共用去KMnO4溶液V mL,求x的值为________________。
-
乙二酸俗名草酸,易溶于水,为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,至滴定达到终点。
④重复实验。记录整理数据如下:
| 实验序号 | V(KMnO4溶液) |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 0.10 | 10.00 |
| 2 | 1.10 | 11.10 |
| 3 | 1.50 | 13.50 |
| 4 | 0.70 | 10.80 |
回答下列问题:
(1)乙二酸和KMnO4标准溶液反应的离子方程式为____________
(2)步骤①需要使用烧杯、量筒、玻璃棒、胶头滴管,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为__________________(填名称)。
(3)本实验滴定达到终点的标志是__________________________;
(4)根据数据,计算H2C2O4溶液的物质的量浓度为______mol/L,x=____________;
(5)若滴定终点时仰视滴定管刻度,则x值会_____________(填“偏大”、“偏小”或“不变”) 。
-
草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x 值,进行如下实验:
①称取wg草酸晶体,配成100.00 mL水溶液。
②量取25.00 mL所配制的草酸溶液置于锥形瓶内,加入适量稀硫酸。
③用浓度为a mol/L的KMnO4溶液滴定到终点。
所发生的反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O 。试回答:
(1)实验中不需要的仪器有___________(填序号),还缺少的玻璃仪器有________(填名称)。
a.托盘天平(带砝码,镊子) b.滴定管 c.100mL量筒 d.100mL容量瓶 e.烧杯 f.漏斗 g.锥形瓶 h.玻璃棒 i.药匙 j.烧瓶
(2)实验中,标准液KMnO4溶液应装在_____________式滴定管中。
(3)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的x值会____________(填“偏大”、“ 偏小”、“ 无影响”)
(4)滴定时,根据_______________现象,即可确定反应达到终点。
(5)在滴定过程中若用amol/L的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为_______mol/L,由此可计算x的值是____________。
-
为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260 g草酸晶体,配成100 mL溶液。
②取25.00 mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000 mol/L的KMnO4溶液滴定H2C2O4溶液,当__________________时,滴定结束。
④记录数据,重复实验。整理数据如:
| 实验序号 | V(KMnO4溶液) |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 0.10 | 10.00 |
| 2 | 1.10 | 11.10 |
| 3 | 1.50 | 11.50 |
回答下列问题:
(1)步骤①需使用烧杯、量筒、玻璃棒,还缺少的玻璃仪器为______________(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为_______________(填名称)。
(2)该反应原理的化学方程式为_____________________________________________。
(3)请将步骤③补充完整_____________________________________________________。
(4)根据数据,计算H2C2O4溶液的物质的量浓度为_________mol/L,x=________。
(5)若滴定终点读数时俯视KMnO4溶液液面,则x值会_________(填“偏大”“偏小”或“无影响”)。


 b.
b. 
