-
电负性的大小可以作为判断元素金属性和非金属性强弱的尺度。下列关于电负性的变化规律正确的是( )
A. 周期表从左到右,同周期主族元素的电负性逐渐变大
B. 周期表从上到下,元素的电负性逐渐变大
C. 电负性越大,金属性越强
D. 电负性越小,非金属性越强
高二化学选择题中等难度题查看答案及解析
-
电负性的大小也可以作为判断金属性和非金属性强弱的尺度,下列关于电负性的变化规律正确的是
A. 周期表中同周期元素从左到右,元素的电负性逐渐增大
B. 周期表中同主族元素从上到下,元素的电负性逐渐增大
C. 电负性越大,金属性越强
D. 电负性越小,非金属性越强
高二化学单选题简单题查看答案及解析
-
电负性的大小也可以作为判断元素金属性和非金属性强弱的尺度。下列关于电负性的变化规律正确的是( )
A. 周期表从左到右,元素的电负性逐渐变大
B. 周期表从上到下,元素的电负性逐渐变大
C. 电负性越大,金属性越强
D. 电负性越小,非金属性越强
高二化学单选题简单题查看答案及解析
-
电负性的大小也可以作为判断金属性和非金属性强弱的尺度,下列关于电负性的变化规律正确的是
A.周期表中同周期元素从左到右,元素的电负性逐渐增大
B.周期表中同主族元素从上到下,元素的电负性逐渐增大
C.电负性越大,金属性越强
D.电负性越小,非金属性越强
高二化学单选题简单题查看答案及解析
-
下列叙述正确的是( )
A.电负性的大小可以作为判断元素金属性和非金属性强弱的尺度
B.在同一电子层上运动的电子,其自旋方向肯定不同
C.镁原子的核外电子排布由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
D.基态原子价层电子排布是5s1的元素,其氢氧化物的溶液一定不能溶解氢氧化铝
高二化学单选题简单题查看答案及解析
-
下列说法不正确的是( )
A. 第ⅠA族元素的电负性从上到下逐渐减小,而第ⅦA族元素的电负性从上到下逐渐增大
B. 电负性的大小可以作为衡量元素的金属性和非金属性强弱的尺度
C. 元素的电负性越大,表示其原子在化合物中吸引电子能力越强
D. NaH的存在能支持可将氢元素放在第ⅦA族的观点
高二化学单选题简单题查看答案及解析
-
下列各项叙述中正确的是( )
A. 电负性的大小可以作为判断金属性和非金属性强弱的尺度
B. 在同一电子层上运动的电子,其自旋方向肯定不同
C. 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
D. 原子最外层电子排布是5s1的元素,其氢氧化物一定不能溶解氢氧化铝
高二化学选择题简单题查看答案及解析
-
下列各项叙述中正确的是( )
A. 电负性的大小可以作为判断金属性和非金属性强弱的尺度
B. 在同一电子层上运动的电子,其自旋方向肯定不同
C. 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
D. 原子最外层电子排布是5s1的元素,其氢氧化物一定不能溶解氢氧化铝
高二化学选择题中等难度题查看答案及解析
-
元素周期律的发现为人类认识元素间的规律做出了巨大贡献。下列关于元素周期表和元素周期律的说法正确的是:
A. 在元素周期表左上方的元素比右下方的元素金属性强
B. 在金属和非金属的分界处可以找到冶炼活泼金属的还原剂
C. 同周期主族元素电子层数相同,但最外层电子数逐渐增多,因此从左到右原子半径逐渐增大
D. 不同主族元素的单质从上到下熔沸点变化不完全相同
高二化学选择题简单题查看答案及解析
-
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R为元素周期表中的电负性最强的元素。则下列判断正确的是( )
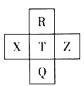
A.非金属性:Z<T<X
B.R与Q的电子数相差24
C.气态氢化物的沸点:R<T<Q
D.最高价氧化物的水化物的酸性:T>Q
高二化学单选题中等难度题查看答案及解析