氨气是一种重要的化工原料,工业上用N2和H2合成NH3。现己知N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化示意图如下图。则N-H键键能为( )
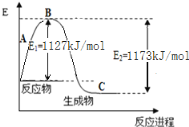
| 化学键 | H-H | N≡N |
| 键能(kJ/mol) | 436 | 946 |
A. 248kJ/mol B. 391kJ/mol C. 862kJ/mol D. 431kJ/mol
高一化学单选题中等难度题
氨气是一种重要的化工原料,工业上用N2和H2合成NH3。现己知N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化示意图如下图。则N-H键键能为( )

| 化学键 | H-H | N≡N |
| 键能(kJ/mol) | 436 | 946 |
A. 248kJ/mol B. 391kJ/mol C. 862kJ/mol D. 431kJ/mol
高一化学单选题中等难度题
氨气是一种重要的化工原料,工业上用N2和H2合成NH3。现己知N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化示意图如下图。则N-H键键能为( )

| 化学键 | H-H | N≡N |
| 键能(kJ/mol) | 436 | 946 |
A. 248kJ/mol B. 391kJ/mol C. 862kJ/mol D. 431kJ/mol
高一化学单选题中等难度题查看答案及解析
(10分) 氨气是一种重要的化工原料,工业上用N2和H2合成NH3。现已知N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量变化示意图如下左图。回答下列问题:
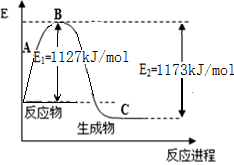
(1)该反应为 (填“吸热”或“放热”)反应。
(2)合成氨的热化学方程式为 。
(3)若又已知键能数据如上表,结合以上数据求出N-H键键能为 kJ/mol。
(4)工业上,以氨气为原料生产硝酸的第一步为氨催化氧化,请写出该反应的化学方程式 。
高一化学填空题中等难度题查看答案及解析
氨气是一种重要的化工产品。
(1)工业中用氯气和氢气在一定条件下合成氨气,有关方程式如下: 3H2 (g)+N2(g)⇌2NH3 (g) + 92.4 kJ
①对于该反应:要使反应物尽可能快的转化为氨气,可采用的反应条件是__________,要使反应物尽可能多的转化为氨气,可采用的反应条件是__________:(均选填字母)
A.较高温度B.较低温度C.较高压强 D.较低压强 E.使用合适的催化剂
工业上对合成氨适宜反应条件选择,是综合考虑了化学反应速率、化学平衡和设备材料等的影响。
②该反应达到平衡后,只改变其中一个因素,以下分析中不正确的是_______:(选填字母)
A.升高温度,对正反应的反应速率影响更大
B.增大压强,对正反应的反应速率影响更大
C.减小生成物浓度,对逆反应的反应速率影响更大
③某化工厂为了综合利用生产过程中副产品CaSO4,和相邻的合成氨厂联合设计了制备(NH4)2SO4的工艺流程(如图),该流程中:
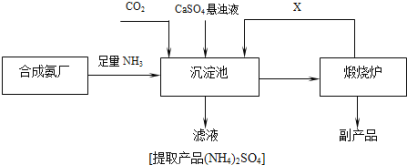
向沉淀池中通入足量的氨气的目的是______________________________,可以循环使用的X是_______________。(填化学式)
(2)实验室中可以用铵盐与强碱共热得到氨气。有关的离子方程式为_____________________。
①0.01 mol/L硝酸铵溶液0.5L,与足量的氢氧化钠溶液共热,可产生氨气_____L(标准状态)。
②若有硝酸铵和硫酸铵的混合溶液0.5L,与足量的氢氧化钠溶液共热,可产生氨气0.025mol;在反应后的溶液中加入足量的氯化钡溶液,产生0.01 mol 白色沉淀,则原混合液中,硝酸铵的浓度为_______mol/L。
③现有硝酸铵、氯化铵和硫酸铵的混合溶液V L,将混合溶液分成两等分:一份溶液与足量的氢氧化钠溶液共热,共产生氨气A mol;另一份溶液中慢慢滴入C mol/L的氯化钡溶液B L,溶液中SO42-恰好全部沉淀;将沉淀过滤后,在滤液中继续滴入硝酸银溶液至过量,又产生D mol沉淀。则原混合溶液中,氯化铵的浓度为________mol/L,硝酸铵的浓度为_______mol/L。(用含有字母的代数式表示)
高一化学工业流程困难题查看答案及解析
氨是最重要的氮肥,是产量最大的化工品之一。其合成原理为:N2(g)+3H2(g)2NH3(g), 某同学为了探究氮气和氢气反应生成氨气,在一恒温、恒容密闭容器中充入1 mol N2和3 mol H2混合发生下列反应,其中断裂1mol H2需要吸收436 kJ的能量,断裂1 mol N2需要吸收945 kJ的能量,断裂1 mol N-H键吸收391 kJ的能量。
(1)写出NH3的电子式___________________。
(2)该反应________(填“吸收”或“放出”)热量______________。
(3)当反应达到平衡时,N2和H2的转化率之比为____________。
高一化学填空题简单题查看答案及解析
下列转变过程属于氮的固定的是
A.氨气和HCl气体混合生成NH4Cl固体 B.氨的催化氧化
C.工业上用N2和H2 合成氨 D.NO遇到空气变为红棕色
高一化学选择题简单题查看答案及解析
下列过程属于“氮的固定”的是
A.合成氨工业中将氮气与氢气化合生成氨气
B.N2和O2经放电生成NO
C.通过加压、降温等方法将氮气转变为液态氮
D.NH3被H2SO4硫酸吸收生成(NH4)2SO4
高一化学选择题简单题查看答案及解析
氨气(NH3)是一种重要的化工原料,广泛应用于制氮肥、制药、合成纤维等。请回答下列问题:
(1)2molNH3在标准状况下的体积是___。
(2)2molNH3的质量是___,其中所含氢元素的质量是___。
(3)2molNH3所含的氨分子数为___,电子数为___。
(4)工业上用反应N2+3H2 2NH3来合成氨气,则若制得2molNH3,标准状况下参与反应的H2的体积为___;14克N2参与反应可得NH3物质的量为___。
高一化学计算题中等难度题查看答案及解析
(10分)工业合成氨的反应:是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.
⑴相同条件下,1 mol N2和3 mol H2所具有的能量________(“大于”、“小于”、“等于”)2 molNH3具有的能量 ;
⑵如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量________(“大于”、“小于”、“等于”)上述数值,其原因是________;
⑶实验室模拟工业合成氨时,在容器为2L的密闭容器内,反应经过10min后,生成10 mol NH3,则用N2表示的该反应速率为:________;
⑷一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是________
a.正反应速率和逆反应速率相等 b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值 d.N2和H2的浓度相等
e. N2、H2和NH3的体积分数相等 f.反应达到最大限度
高一化学填空题中等难度题查看答案及解析
高一化学选择题中等难度题查看答案及解析
高一化学选择题中等难度题查看答案及解析