Licht等科学家设计的Al—MnO4—电池原理如图所示,电池总反应为Al+MnO4—===AlO2—+MnO2,下列说法正确的是( )

A. 电池工作时,K+向负极区移动
B. Al电极发生还原反应
C. 正极的电极反应式为MnO4—+4H++3e-===MnO2+2H2O
D. 理论上电路中每通过1mol电子,负极质量减小9g
高二化学单选题中等难度题
Licht等科学家设计的Al—MnO4—电池原理如图所示,电池总反应为Al+MnO4—===AlO2—+MnO2,下列说法正确的是( )

A. 电池工作时,K+向负极区移动
B. Al电极发生还原反应
C. 正极的电极反应式为MnO4—+4H++3e-===MnO2+2H2O
D. 理论上电路中每通过1mol电子,负极质量减小9g
高二化学单选题中等难度题
Licht等科学家设计的Al—MnO4—电池原理如图所示,电池总反应为Al+MnO4—===AlO2—+MnO2,下列说法正确的是( )

A. 电池工作时,K+向负极区移动
B. Al电极发生还原反应
C. 正极的电极反应式为MnO4—+4H++3e-===MnO2+2H2O
D. 理论上电路中每通过1mol电子,负极质量减小9g
高二化学单选题中等难度题查看答案及解析
A1-MnO4−电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示。已知电池总反应为Al + MnO4− ═AlO2- + MnO2.下列说法正确的是( )

A. 电池工作时,K+向负极移动
B. 电池工作时,电子由Al经电解质溶液流向Ni
C. 负极反应为Al- 3e− + 4OH− ═AlO2− + 2H2O
D. 电池工作时,Ni电极周围溶液pH减小
高二化学单选题中等难度题查看答案及解析
据报道,最近有科学家设计了一种在常压下运行的集成BaZrO3基质子陶瓷膜反应器( PCMR) ,将PCMR与质子陶瓷燃料电池相结合进行电化学法合成氨的原理如图所示,下列说法正确的是
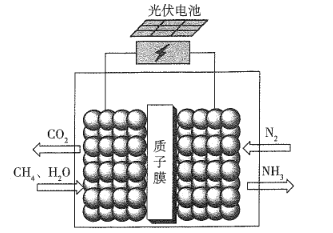
A.阳极的电极反应式为CH4+2H2O+8e-=CO2 +8H+
B.阴极可能发生副反应2H+ +2e- =H2 ↑
C.质子(H+)通过交换膜由阴极区向阳极区移动
D.理论上电路中通过3 mol电子时阴极最多产生22.4 L NH3
高二化学单选题简单题查看答案及解析
(11分)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。 回答下列问题:

(1)外电路的电流方向是由________极流向________极。(填字母)
(2)电池正极反应式为__________________________。
(3)是否可用水代替电池中的混合有机溶剂?________(填“是”或“否”),原因是 ________________________________________________。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为____________________________________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为____。
高二化学填空题困难题查看答案及解析
锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。 回答下列问题:

(1)外电路的电流方向是由________极流向________极(填字母)。
(2)电池正极反应式为___________________________________。
(3)是否可用水代替电池中的混合有机溶剂?________(填“是”或“否”),原因是________________________________________________________________。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为_______________________________________________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________。
高二化学填空题中等难度题查看答案及解析
锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质的有机溶液迁移入 MnO2 晶格中,生成 LiMnO2。下列说法正确的是
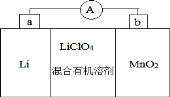
A. 外电路的电流方向是由 a 极流向 b 极。
B. 电池b 极反应式为 MnO2+e-+Li+=LiMnO2
C. 可用水代替电池中的混合有机溶剂
D. a 极发生还原反应
高二化学单选题中等难度题查看答案及解析
锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。 回答下列问题:

(1)外电路的电流方向是由________极流向________极(填字母)。
(2)电池正极反应式为___________________________________。
(3)是否可用水代替电池中的混合有机溶剂?________(填“是”或“否”),原因是________________________________________________________________。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为_______________________________________________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________。
高二化学填空题困难题查看答案及解析
锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:

(1)外电路的电子流方向是由__________极流向__________极。(填字母a或b)
(2)电池正极反应式为________________________________________。
(3)是否可用水代替电池中的混合有机溶剂?__________(填“是”或“否”)原因是_______________。
(4)MnO2可与KOH和KClO4在高温条件下反应,生成K2MnO4,该反应的氧化产物和还原产物的物质的量比为________,K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2,该反应的离子方程式为______________。
高二化学简答题困难题查看答案及解析
锂锰电池的体积小、性能优良,是常用的一次性电池。该电池反应原理如图所示,其中电解质LiC1O4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。下列说法正确的是
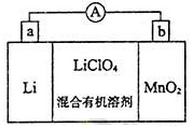
A. 外电路的电流方向是由Li极流向MnO2极
B. 正极的电极反应式:MnO2+Li++e-=LiMnO2
C. Li电极发生还原反应
D. 在放电过程中ClO4-向正极迁移
高二化学选择题中等难度题查看答案及解析
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜(含有少量锌、金、银等杂质)的精炼原理,其中乙装置中X为阳离子交换膜。回答下列问题:
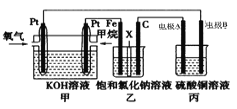
(1)甲烷燃料电池负极的电极反应式为_________。
(2)乙装置中阳离子通过X膜向________ 极(填“Fe”或“C”)移动;丙装置中粗铜为_______电极(填“A”或“B”)
(3)若在标况下,有2.24L氧气参与反应,则乙装置中右侧溶液________(填“增加”或“减少”)______g,丙装置中CuSO4浓度__________(填“增加”、“减少” 或“不变”)。
高二化学填空题中等难度题查看答案及解析