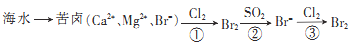-
海水是一个巨大的化学资源宝库,下图是海水综合利用的部分工业流程图:

Ⅰ.在过程①中应加入的试剂分别为A.Na2CO3溶液、B.盐酸、C.BaCl2溶液、D.NaOH溶液,这4种试剂添加的合理顺序是____(填序号);过程①中须完成的实验操作分别为a.多步过滤、b.蒸发浓缩、c.冷却结晶,操作a中需要的玻璃仪器是烧杯、__________。
Ⅱ.(1)氯碱工业的反应原理是电解饱和食盐水,下列物质不可能是氯碱工业产品的是____。
A.H2 B.Cl2 C.Na2CO3 D.NaOH
(2)如图所示是离子交换膜法电解原理示意图,两极均用惰性电极材料。精制饱和食盐水进入阳极室,H+在右电极上发生____反应(填“氧化”或“还原”),所使用的离子交换膜的主要作用是____________。

(3)操作人员欲用pH试纸测定右室溶液酸碱度,其操作方法为________。
Ⅲ.过程④制取金属镁的化学方程式为MgCl2(熔融) Mg+Cl2↑。简述工业上不使用电解MgO制取金属镁的原因:___。
Mg+Cl2↑。简述工业上不使用电解MgO制取金属镁的原因:___。
Ⅳ.过程⑤用纯碱溶液吸收Br2,发生的主要反应为:3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑,则吸收1 mol Br2,转移的电子数为____mol。
-
海洋是一个巨大的化学资源宝库,海水资源综合利用的部分流程图。
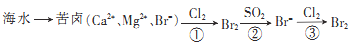
(1)由海水提取的粗盐中常含有 等,可以加入_______________(填化学式)除去,反应的离子方程式为__________________。
等,可以加入_______________(填化学式)除去,反应的离子方程式为__________________。
(2)步骤①反应的离子方程式为__________________。
(3)步骤②中溴单质被SO2还原为 ,硫元素被氧化为
,硫元素被氧化为 ,从该反应原理中不能得出溴的非金属性强于硫,其原因是__________________。当有0.25 mol SO2被氧化,转移的电子的物质的量为__________mol。
,从该反应原理中不能得出溴的非金属性强于硫,其原因是__________________。当有0.25 mol SO2被氧化,转移的电子的物质的量为__________mol。
-
(14分)海洋是巨大的化学资源宝库。下面是海水化学资源综合利用的部分流程图:

回答:
(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、____(填试剂化学式),然后____(填操作名称)。在溶液中再加适量 (填试剂),加热蒸干溶液即得到精盐。
(2)某同学在实验室模拟氯碱工业的生产原理电解饱和食盐 水。用玻璃棒蘸浓氨水检验阳极产生的气体,发现产生大量白烟。阳极生成的气体是 ,白烟的主要成分是 。
水。用玻璃棒蘸浓氨水检验阳极产生的气体,发现产生大量白烟。阳极生成的气体是 ,白烟的主要成分是 。
(3)制取MgCl2的过程中涉及反应:MgCl2·6H2O MgCl2 + 6H2O,该反应要在HCl气流中进行,原因是 。
MgCl2 + 6H2O,该反应要在HCl气流中进行,原因是 。
(4)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是 。
(5)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时有CO2放出。最后再用H2SO4处理得到Br2,最后一步反应的离子方程式是__________ 。
-
海洋是巨大的化学资源宝库。下面是海水化学资源综合利用的部分流程图:

回答:
(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、_____(填试剂化学式),然后_____________(填操作名称)。在溶液中再加适量________(填试剂),加热蒸干溶液即得到精盐。
(2)某同学在实验室模拟氯碱工业的生产原理电解饱和食盐水。用玻璃棒蘸浓氨水检验阳极产生的气体,发现产生大量白烟。阳极生成的气体是________,白烟的主要成分是________。
(3)制取MgCl2的过程中涉及反应:MgCl2·6H2O MgCl2 + 6H2O,该反应要在HCl气流中进行,原因是 ________。
MgCl2 + 6H2O,该反应要在HCl气流中进行,原因是 ________。
(4)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是_________。
-
海洋是一个巨大的化学资源宝库。 海水综合利用的部分流程如下:

已知:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。
(1)电解饱和 NaCl 溶液的化学方程式为_____________________________________。粗盐中常含 Ca2+、Mg2+、SO42-等杂质离子,可依次加入NaOH、___________、___________、盐酸试剂来进行提纯。
(2)下列方法不可用于海水淡化的是________(填字母代号)。
A. 蒸馏法 B. 萃取法 C. 离子交换法 D. 电渗析法
(3)工业上用电解法制Mg 时,通常在MgCl2中加入适量 CaCl2,其原因是:①___________; ②增加电解质的密度,便于分离出熔融的镁。
(4) 利用右图所示装置从母液中提取溴,在 B 瓶中得到较浓的溴水。实验方案为:关闭b、d,打开a、c,由a 向A中缓慢通入________至反应完全;关闭a、c,打开b、d、e,由b向A中鼓入足量__________, 同时由 e 向 B 中通入足量_________;关闭b、e,打开a,再由a 向B中缓缓鼓入足量___________ (实验中须使用的试剂有:SO2、Cl2、热空气) 。

-
海洋是一个巨大的化学资源宝库,下图是海水加工的示意图:
(1)海水淡化工厂通常采用的制备淡水的方法有 (写出两种)。
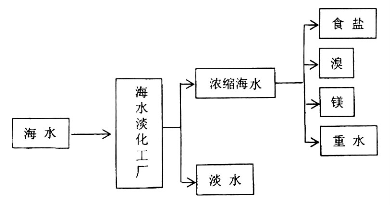
(2)下图是从浓缩海水中提取溴的流程图。写出下图中试剂A的化学式 ,
 溶液中发生反应的化学方程式为 。
溶液中发生反应的化学方程式为 。
(3)制备金属镁是通过电解熔融的 ,而不用MgO,其原因是
,而不用MgO,其原因是
。
(4)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和Cl2。海水中得到的粗盐往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 。电解食盐水在离子交换膜电解槽中进行,阳离子交换膜的作用是 。
-
南海是一个巨大的资源宝库,开发利用海水资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法不正确的是 ( )
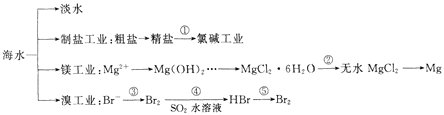
A.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法
B.氯碱工业中采用阳离子交换膜可提高产品的纯度
C.由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干
D.溴工业中③、④的目的是富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原
-
南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法正确的是( )
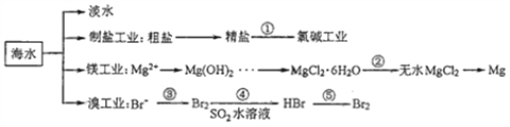
A. 海水淡化的方法主要有蒸馏法、电渗析法、冰冻法
B. 氯碱工业中采用阴离子交换膜可提高产品的纯度
C. 由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干
D. 溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原
-
南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法正确的是( )
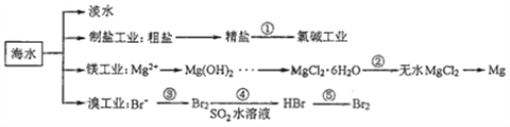
A. 海水淡化的方法主要有蒸馏法、电渗析法、冰冻法
B. 氯碱工业中采用阴离子交换膜可提高产品的纯度
C. 由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干
D. 溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原
-
南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法正确的是( )
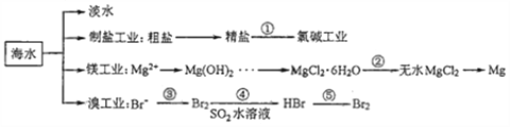
A. 海水淡化的方法主要有蒸馏法、电渗析法、冰冻法
B. 氯碱工业中采用阴离子交换膜可提高产品的纯度
C. 由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干
D. 溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原


Mg+Cl2↑。简述工业上不使用电解MgO制取金属镁的原因:___。