(7分)以粗盐(主要成分是NaCl,含有不溶性泥砂、可溶性的MgCl2、CaCl2等杂质)为原料,电解食盐水生产氢氧化钠的简要流程如下:
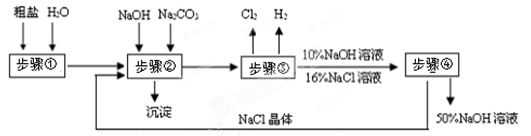
(1)步骤①除去不溶性杂质,其主要操作有溶解、 。
(2)步骤②除去可溶性杂质,写出其中一个化学方程式 。
(3)写出步骤③中一种单质的名称 ,工业上可利用本步骤中产生的两种气体生产盐酸,写出盐酸的一种用途 。
(4)步骤④中制得的氢氧化钠有强烈的腐蚀性,如果不慎沾到皮肤上,要 。
(5)该流程中可以循环利用的物质是 。
九年级化学填空题困难题
(7分)以粗盐(主要成分是NaCl,含有不溶性泥砂、可溶性的MgCl2、CaCl2等杂质)为原料,电解食盐水生产氢氧化钠的简要流程如下:

(1)步骤①除去不溶性杂质,其主要操作有溶解、 。
(2)步骤②除去可溶性杂质,写出其中一个化学方程式 。
(3)写出步骤③中一种单质的名称 ,工业上可利用本步骤中产生的两种气体生产盐酸,写出盐酸的一种用途 。
(4)步骤④中制得的氢氧化钠有强烈的腐蚀性,如果不慎沾到皮肤上,要 。
(5)该流程中可以循环利用的物质是 。
九年级化学填空题困难题
(7分)以粗盐(主要成分是NaCl,含有不溶性泥砂、可溶性的MgCl2、CaCl2等杂质)为原料,电解食盐水生产氢氧化钠的简要流程如下:

(1)步骤①除去不溶性杂质,其主要操作有溶解、 。
(2)步骤②除去可溶性杂质,写出其中一个化学方程式 。
(3)写出步骤③中一种单质的名称 ,工业上可利用本步骤中产生的两种气体生产盐酸,写出盐酸的一种用途 。
(4)步骤④中制得的氢氧化钠有强烈的腐蚀性,如果不慎沾到皮肤上,要 。
(5)该流程中可以循环利用的物质是 。
九年级化学填空题困难题查看答案及解析
(15分)某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【查阅资料】
①生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质(不与酸反应).
②生产原理反应:NaCl+ NH3 + CO2 + H2O= NaHCO3↓+ NH4Cl,分离得晶体B,并使其充分受热,可分解制得纯碱,同时得到二氧化碳和水.
③氯化铵分解的化学方程式是NH4Cl △ NH3↑+HCl↑.
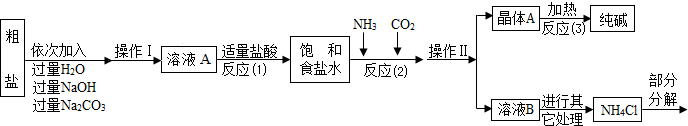
④部分生产流程如下图所示:
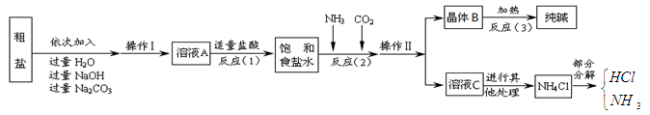
【问题讨论】
(1)①溶液A中的溶质有NaCl和 、 ,
②操作Ⅱ的名称为 .
③流程中Na2CO3溶液的作用是除去粗盐中的 .
④写出加入NaOH溶液与MgCl2反应的化学方程式 .
⑤晶体B受热分解的化学方程式为 .
(2)上述生产流程中可循环使用的是 (填序号).
A.NaOH B.NH3 C.HCl D.CO2
【组成探究一】
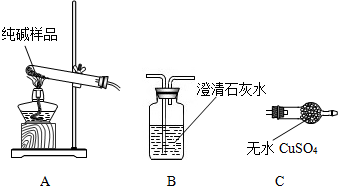
(3)设计实验检验纯碱样品中是否混有晶体B,请完成下表
| 选择的装置 | 实验现象 | 实验结论 |
| 选择的装置(填序号) | 实验现象 | 实验结论 |
| 样品不含晶体B |
【组成探究二】
(4)取纯碱样品加水溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.产生沉淀的方程式为 ,由此确定纯碱样品含有杂质NaCl.
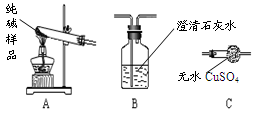
【组成探究三】
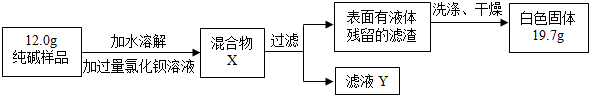
(5)同学们为了测定该纯碱样品的纯度,设计了如下实验:
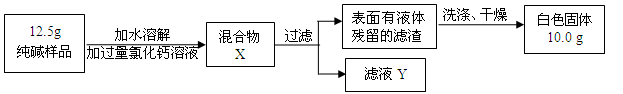
①判断加入氯化钙溶液是否过量的方法是 ,然后观察现象判断.
②判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观察现象判断.
A.氯化钡溶液 B.硝酸银溶液 C.碳酸钠溶液 D.稀盐酸
③根据实验数据,计算样品中碳酸钠的质量分数是多少?(写出计算过程.3分)
九年级化学探究题困难题查看答案及解析
| 选择的装置 | 实验现象 | 实验结论 |
| ________ | ________ | 样品不含晶体A |
九年级化学填空题中等难度题查看答案及解析
氯碱工业以粗盐(主要成分是NaCl,此外还含有少量泥沙,CaCl2、MgCl2)为原料,生产氯气、氢气和氢氧化钠,模拟流程如下:

(1)图一精制过程中除去滤渣的操作是_____。
(2)图一流程中可以循环利用的物质是_____(填物质名称)。
(3)写出电解NaCl溶液的化学方程式:_____。
(4)图二为氢氧化钠和氯化钠的溶解度曲线,t℃时氢氧化钠的溶解度为_____,图一脱盐操作中除去氯化钠可以采用_____。(填“降温结晶”或“蒸发结晶”)法。
九年级化学流程题中等难度题查看答案及解析
(10分)某粗盐中主要成分为NaCl ,还含有的少量MgCl2、CaCl2和少量泥沙。为了除去杂
质,得到纯净的氯化钠,进行如下实验。
(1)除难溶性杂质。将5g的粗盐溶解于足量水中,需用玻璃棒不断搅拌,目的是 ;进行过滤操作时,需要的玻璃仪器有烧杯、玻璃棒和 ;过滤后,将滤液转移到 (填仪器名称)进行加热蒸发,得到固体精盐4g。若所得精盐的产率偏低,可能的原因是 (填字母)。
A.部分粗盐未溶解 B.蒸发时未使用玻璃棒进行搅拌,导致液滴飞溅 C. 过滤时,滤纸破损了
(2)除可溶性杂质。经过上述操作后,精盐中仍存在少量的MgCl2、CaCl2未除去,现设计如下实验进行提纯,提纯的流程如下:

回答下列问题:
①用NaOH为了除去MgCl2杂质,反应的化学方程式为____________________ _。
②NaOH和Na2CO3如果添加过量了,需往滤液中加入适量___________除去。
③过滤后,所得滤渣中含有的物质是 (填化学式)。
④从滤液中得到氯化钠固体的主要操作是蒸发,为了获得纯净的氯化钠,应蒸发至__ _(填序号)。
A.完全蒸干时停止加热 B.快干时停止加热,利用余热蒸干
九年级化学推断题困难题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
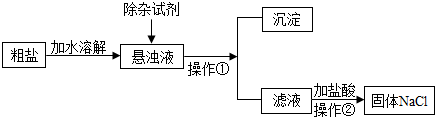
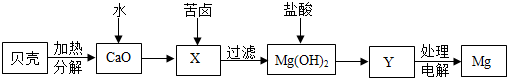
某兴趣小组利用海水(含 NaCl、MgCl2 和 CaCl2 等可溶性杂质及泥沙等难溶性杂质)和石灰石为原料制取漂白粉,流程如下:
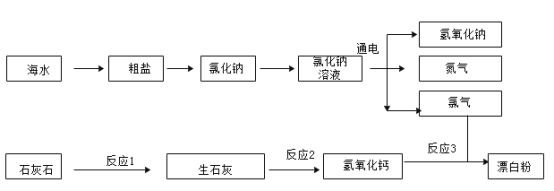
①海水暴晒得到粗盐,利用了氯化钠的溶解度随温度升高而______(选填“变大”、“变小”或“变化不大”)的 性质。
②粗盐提纯得到固体氯化钠,发生了______(填编号)。
A物理变化 B化学变化
③提纯操作中,过滤时用到了铁架台、烧杯、______(填仪器名称)。
④氯化钠溶液通电后发生的不是分解反应,判断的依据是______。
⑤反应1中的化学方程式______。
⑥设计实验方案证明石灰石已完全分解。
| 实验 | 现象 | 结论 |
| ______ | ________ | 石灰石已完全分解 |
⑦实际工业生产中,反应3化学方程式:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2X,X 的化学式为______,Ca(ClO)2中氯元素的化合价为______,反应物氢氧化钙最好用______(填“饱和石灰水”或“石灰乳”)并不断搅拌。
九年级化学流程题中等难度题查看答案及解析
食盐是一种重要的化工原料,请回答下列问题。
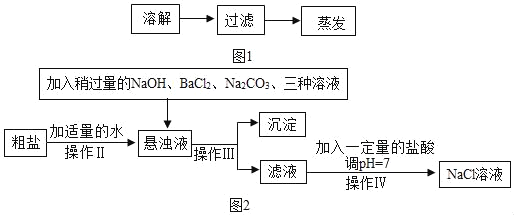
(1)如图1是实验室除去粗盐中泥沙等难溶性杂质的实验步骤。操作Ⅰ的名称是_____。
(2)由于粗盐中还含有少量的MgCl2、CaCl2、Na2SO4等可溶性杂质,不能满足化工生产的要求。因此必须将粗盐进行精制。其流程如图2所示:
①加入稍过量的Na2CO3溶液的目的是除去溶液中的_____ (填离子符号)。
②通过操作Ⅲ所得滤液中的溶质有三种,除了氧化钠外,还有两种,请分别写出它们的化学式_____、_____。
九年级化学流程题中等难度题查看答案及解析

九年级化学解答题中等难度题查看答案及解析
某厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵。生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质。部分生产流程如下图所示:

(1)生产原理:将氨气(NH3)和二氧化碳通入饱和食盐水中得到小苏打和氯化铵的混合物,先通入氨气的原因是:_______ 分离出固体产物,使其充分受热即可分解制得纯碱,此反应的化学方程式为 _______ 。
(2)溶液A中的溶质为 __________。
(3)上述生产流程中可循环使用的是 _____
九年级化学流程题简单题查看答案及解析