-
(1)用热水配制AlCl3溶液,会出现浑浊现象,原因是(用离子方程式和必要的文字说明):
。要消除浑浊现象,又不污染药品,可加入适量的__________溶液。
(2)常温下,有①0.01 mol/L HCl溶液;②pH=12的氨水,其中水的电离程度① ②,(选填“>”、“<”或“=”);若将①、②混合后所得溶液pH=7,则消耗溶液的体积:①________②(选填“>”、“<”或“=”)。若用①来滴定未知浓度的氨水,通常选用____________作指示剂,达滴定终点时各离子浓度由大到小的顺序是_________________________________。
(3)某温度(T℃)时,测得0.01 mol·L-1NaOH溶液的pH=11,则在该温度下,将100 mL 0.2 mol·L-1的稀盐酸与100 mL 0.4 mol·L-1的NaOH溶液混合后,溶液的pH=________。
高三化学填空题中等难度题查看答案及解析
-
把AlCl3溶液蒸干灼烧,最后得到的主要固体产物是什么?为什么?(用化学方程式表示,并配以必要的文字说明)
高三化学解答题中等难度题查看答案及解析
-
的
溶液加水稀释100倍后,pH______
填“
”“
”或“
”
,原因是______
用离子方程式和必要的文字说明
;pH相等的NaOH溶液与
溶液,分别加热到相同的温度后
溶液的pH______NaOH溶液的
填“
”“
”或“
”
;
相等时,
三种溶液中
由大到小的顺序为______;
等体积、等浓度的氢氧化钠与醋酸混合后溶液呈 ______ 性,溶液中
______
填“
”“
”或“
”
;
的氢氧化钠与
的醋酸等体积混合后溶液呈______性,溶液中
______
填“
”“
”或“
”
;
,用
溶液滴定
某一元酸HA溶液所得滴定曲线如图。
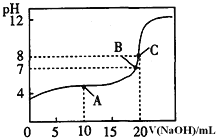
为减小实验误差,由图可知滴定时指示剂应选用______
填“石蕊”、“酚酞”、“甲基橙”
;
、B、C三点所示溶液导电能力最强的是 ______ 点对应的溶液;
,A点的离子浓度大小关系是 ______ .
高三化学综合题中等难度题查看答案及解析
-
的
溶液加水稀释100倍后,pH______
填“
”“
”或“
”
,原因是______
用离子方程式和必要的文字说明
;pH相等的NaOH溶液与
溶液,分别加热到相同的温度后
溶液的pH______NaOH溶液的
填“
”“
”或“
”
;
相等时,
三种溶液中
由大到小的顺序为______;
等体积、等浓度的氢氧化钠与醋酸混合后溶液呈 ______ 性,溶液中
______
填“
”“
”或“
”
;
的氢氧化钠与
的醋酸等体积混合后溶液呈______性,溶液中
______
填“
”“
”或“
”
;
,用
溶液滴定
某一元酸HA溶液所得滴定曲线如图。
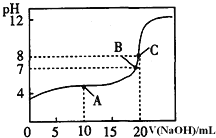
为减小实验误差,由图可知滴定时指示剂应选用______
填“石蕊”、“酚酞”、“甲基橙”
;
、B、C三点所示溶液导电能力最强的是 ______ 点对应的溶液;
,A点的离子浓度大小关系是 ______ .
高三化学综合题中等难度题查看答案及解析
-
已知:常温下
,
下列说法正确的是( )
A.常温下,若配制
溶液,为使配制过程中不出现浑浊现象,则至少需要加入
的盐酸
(总体积忽略加入盐酸体积)
B.向
含
和
的酸性混合溶液中通入
,至该溶液的
时,溶液体积变化忽略不计,所得溶液中
的值为
C.常温下,
溶于水所得饱和溶液中
为
D.pH越小,越有利于去除废水中的
高三化学单选题中等难度题查看答案及解析
-
在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。

(1)用离子方程式解释现象I中出现胶状沉淀的原因: 。
(2)II中加碱时出现的现象是 ,此现象说明溶液中发生反应的离子方程式是 。
(3)III中加碱时出现的现象是 。
(4)用离子方程式解释IV中加碱时出现的现象: 。
(5)滴加试剂顺序的变化,会影响溶液中的现象和发生的反应,请继续分析以下实验。
实验
试剂及操作
现象
试管
滴管
1.0 mL
0.1 mol·L−1 Fe(NO3)2溶液
先滴加1.5 mL 1.0 mol·L−1 H2SO4溶液;
再滴加1.0 mL 0.5 mol·L−1 NaOH溶液
V.加酸时溶液无明显现象;加碱后溶液依然没有明显变化
①探究加酸时Fe(NO3)2溶液中是否发生了反应:向1.0 mL 0.1 mol·L−1 Fe(NO3)2溶液中 ,溶液立即变红,说明溶液中含Fe3+,证明加酸时溶液中发生了反应。
② 推测溶液中产生Fe3+的可能原因有两种:
a.酸性条件下,0.1 mol·L−1 Fe(NO3)2溶液中的Fe2+被NO3-氧化;
b. (用离子方程式表示)。
高三化学实验题极难题查看答案及解析
-
在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。
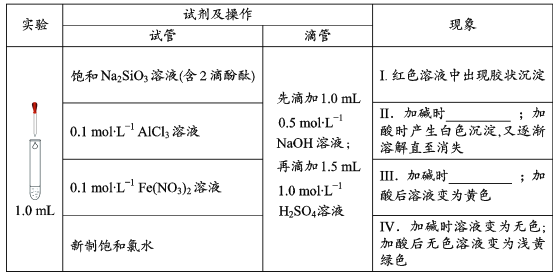
(1)用离子方程式解释现象Ⅰ中出现胶状沉淀的原因:___。
(2)Ⅱ中加碱时出现的现象是___,此现象说明溶液中发生反应的离子方程式是___。
(3)Ⅲ中加碱时出现的现象是___。
(4)滴加试剂顺序的变化,会影响溶液中的现象和发生的反应,请继续分析以下实验。

①探究加酸时Fe(NO3)2溶液中是否发生了反应:
向1.0mL0.1mol/LFe(NO3)2溶液中__,溶液立即变血红,说明溶液中含Fe3+,证明加酸时溶液中发生了反应。
②推测溶液中产生Fe3+的可能原因有两种:
a.酸性条件下,0.1mol/LFe(NO3)2溶液中的Fe2+被NO3-氧化;
b.__。
高三化学实验题中等难度题查看答案及解析
-
自来水用氯气消毒,某学生用这种自来水配制下列物质溶液,不会产生药品变质的是
( )
A.AlCl3 B.FeCl2 C.Na2SO3 D.AgNO3
高三化学选择题中等难度题查看答案及解析
-
(1)A为用惰性电极电解饱和食盐水(含少量Ca2+、Mg2+)的装置.
①电解一段时间后,B中出现浑浊现象,请用离子方程式表示原因________.
此时电极a附近的现象为________,因此工业上电解所用的食盐水需精制.
②随反应的进行,C中溶液红色褪去,主要原因有两种可能.请按要求填写表格.
(2)电解饱和食盐水所得气体X,可应用于提取溴单质.现有流程图如下:假设 主要操作 现象 结论 假设1: 假设2:可能是H+与OH-中和,导致溶液褪色 
请回答:
①气体X的化学式为________,反应II的化学方程式为________.
②在母液苦卤中含有较多的NaCl、KCl、MgCl2、MgSO4等物质.用沉淀法测定苦卤中镁元素的含量(g/L),实验过程中应测定的数据有________.
③电解200kg 质量分数为25%的饱和食盐水,当浓度下降到20%时,收集到氯气的物质的量为________(溶于溶液中的氯气忽略不计,计算结果保留一位小数).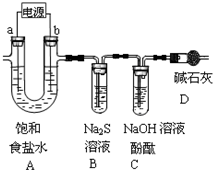
高三化学填空题中等难度题查看答案及解析
-
自来水可用氯气消毒,某学生用这种自来水配制下列物质的溶液,不会产生明显药品变质问题的是( )
A. AlCl3 B. FeCl2 C. AgNO3 D. Na2CO3
高三化学单选题简单题查看答案及解析