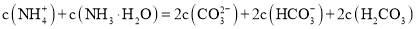-
碳和碳的化合物广泛的存 在于我们的生活中。
在于我们的生活中。
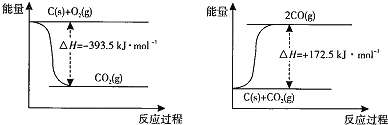
(1)根据下列反应的能量变化示意图,2C(s)+O2(g) =2CO(g) △H= ________________________________________________。
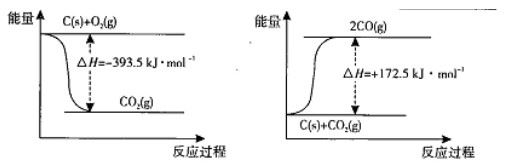
(2)在体积为2L的密闭容器中,充人1 mol CO2和3mol H2,一定
条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H
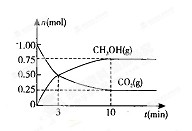
测得CO2(g)和CH3OH(g)的物质的量随时间变化的曲线如右图所示:
①从反应开始到平衡,H2O的平均反应速率v(H2O)= ________________________________________________________________________________________________ 。
②下列措施中能使化学平衡向正反应方向移动的是 ________________________________________________________________(填编号)。
A.升高温度 B.将CH3OH(g)及时液化移出
C.选择高效催化剂 D.再充入l mol CO2和4 mol H2
(3) CO2溶于水生成碳酸。已知下列数据:
| 弱电解质 | H2CO3 | NH3.H2O |
| 电离平衡常数( 25℃) | Ka1=  4.30 × 10一7 4.30 × 10一7 Ka2= 5.61× 10一11 | Kb = 1.77× 10一5 |
现有常温下1 mol·L-1的( NH4)2CO3溶液,已知:NH4+水解的平衡常数Kh=Kw/Kb,
CO32-第一步水解的平衡常数Kh=Kw/Ka2。
①判断该溶液呈 ________________________________________(填“酸”、“中”、 “碱”)性,写出该溶液中CO32-
发生第一步水解的离子方程式________________________________________________________________________________________________________________ 。
②下列粒子之间的关系式,其中正确的是 。
A.c(NH4+)>c(HCO3-)> c(CO32-)>(NH4+)
B.c(NH4+)+c(H+)= c(HCO3-)+c(OH-)+ c(CO32-)
C. c(CO32-)+ c(HCO3-)+c(H2CO3)=1mol/L
D. c(NH4+)+ c(NH3.H2O)=2 c(CO32-)+ 2c(HCO3-) +2c(H2CO3)
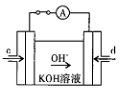
(4)据报道,科学家在实验室已研制出在燃料电池的反应容器中,利用特
殊电极材料以CO和O2为原料做成电池。原理如图所示:通入CO的管口是________________________________ (填“c”或“d”),写出该电极的电极反应式:________________________________________________________________________ 。
-
碳和碳的化合物广泛的存在于我们的生活中。
(1)根据下列反应的能量变化示意图, ______ 。
______ 。
(2)在体积为2L的密闭容器中,充入1mol  和3mol H,一定条件下发生反应:
和3mol H,一定条件下发生反应: ,测得
,测得 和
和 的物质的量随时间变化的曲线如图所示:
的物质的量随时间变化的曲线如图所示:
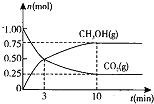
①从反应开始到平衡, 的平均反应速率
的平均反应速率 ______ 。
______ 。
②下列措施中能使化学平衡向正反应方向移动的是 ______  填编号
填编号 。
。
A.升高温度
 将
将 及时液化移出
及时液化移出
C.选择高效催化剂
 再充入1mol
再充入1mol  和4mol
和4mol 
(3) 溶于水生成碳酸。已知下列数据:
溶于水生成碳酸。已知下列数据:
现有常温下 的
的 溶液,已知:
溶液,已知: 水解的平衡常数
水解的平衡常数 ,
, 第一步水解的平衡常数
第一步水解的平衡常数 。
。
①判断该溶液呈 ______  填“酸”、“中”、“碱”
填“酸”、“中”、“碱” 性,写出该溶液中
性,写出该溶液中 发生第一步水解的离子方程式 ______ 。
发生第一步水解的离子方程式 ______ 。
②下列粒子之间的关系式,其中正确的是 ______ 。
A.
B.
C.
D.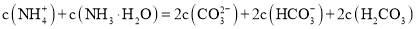
(4)据报道,科学家在实验室已研制出在燃料电池的反应容器中,利用特殊电极材料以CO和 为原料做成电池。原理如图所示:
为原料做成电池。原理如图所示:
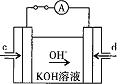
通入CO的管口是 ______  填“c”或“d”
填“c”或“d” ,写出该电极的电极反应式: ______ 。
,写出该电极的电极反应式: ______ 。
-
根据能量变化示意图,下列说法正确的是( )
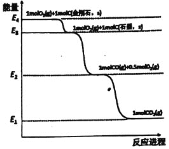
A.C(金刚石,s)+O2(g)=CO2(g) ΔH=(E4-E1)kJ/mol
B.2C(石墨,s)+O2(g)=2CO(g) ΔH=(E2-E3)kJ/mol
C.C(石墨,s)=C(金刚石,s) ΔH=(E3-E4)kJ/mol
D.2CO2(g)=2CO(g)+O2(g) ΔH=2(E2-E1)kJ/mol
-
根据能量变化示意图,下列说法正确的是
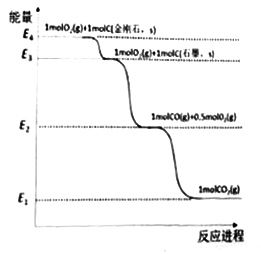
A. C(金刚石,s)+O2=CO2(g) ΔH=(E4-E1)kJ/mol
B. 2C(石墨,s)+O2(g)=2CO(g) ΔH=(E2-E3)kJ/mol
C. C(石墨,s)=C(金刚石,s) ΔH=(E3-E4)kJ/mol
D. 2CO2(g)=2CO(g)+O2(g) ΔH=2(E2-E1)kJ/mol
-
根据能量变化示意图得出的结论正确的是( )
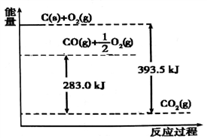
A. 1mol C完全燃烧生成CO2时放出的热量为393.5 kJ/mol
B. 2C(s)+O2(g)=2CO(g) △H=-221.0 kJ/mol
C. 2CO2 (g)=2CO(g)+O2(g) △H=+283.0 kJ/mol
D. C(s)+O2(g)= CO2 (g) △H=+393.5 kJ/mol
-
下列说法正确的是( )
A.如图可表示水分解过程中的能量变化

B.若2C(s)+O2(g)=2CO(g) △H=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol
C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D.已知:Ⅰ:对于反应:H2(g)+Cl2(s)=2HCl (g) △H=- a kJ/mol,
Ⅱ:
且a、b、c均大于零,则断开1molH-Cl键所需的能量为- a-b-c
-
下列说法正确的是
A.右图可表示水分解过程中的能量变化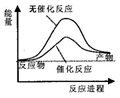
B.若2C(s)+O2(g)=2CO(g) △H= -221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol
C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D.已知:Ⅰ:对于反应:H2(g)+Cl2(s)=2HCl (g) △H= - a kJ/mol,
Ⅱ:
且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为- a-b-c kJ
-
已知:① 2C(s) + O2(g) = 2CO(g) ΔH=-220 kJ·mol-1
② 氢气燃烧的能量变化示意图:
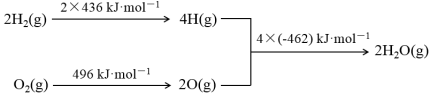
下列说法正确的是
A.1molC(s)完全燃烧放出110 kJ的热量
B.H2(g) + 1/2O2(g) === H2O(g) ΔH=-480 kJ·mol-1
C.C(s) + H2O(g) === CO(g)+H2(g) ΔH=+130 kJ·mol-1
D.欲分解2 mol H2O(l),至少需要提供4×462 kJ的热量
-
己知:①2C(s)+O2(g)=2CO(g) △H=—220kJ·mol—1
②氢气燃烧的能量变化示意图:
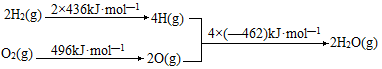
下列说法正确的是
A.lmolC(s)完全燃烧放出110 kJ的热量
B.H2(g)+1/2O2(g)=H2O(g) △H=—480kJ·mol—1
C.C(s)+H2O(g)=CO(g)+H2(g) △H=+130kJ·mol—1
D.欲分解2molH2O(l),至少需要提供4×462kJ的热量
-
已知:① 2C(s)+O2(g)=2CO(g);ΔH= -220kJ·mol-1
② 氢气燃烧的能量变化示意图:
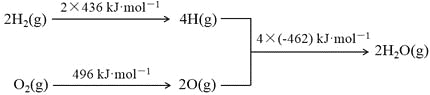
下列说法正确的是
A.1mol C(s)完全燃烧放出110 kJ的热量
B.H2(g)+1/2O2(g)=H2O(g);ΔH= -480kJ·mol-1
C.C(s)+H2O(g)=CO(g)+H2(g);ΔH= +130kJ·mol-1
D.欲分解2mol H2O(l),至少需要提供4×462kJ的热量
在于我们的生活中。


CH3OH(g)+H2O(g) △H