-
环境问题越来越受到人们的重视,研究表明氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如图所示)。
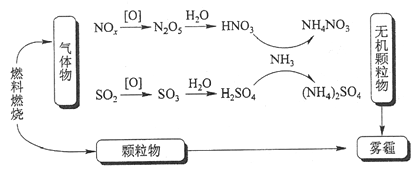
回答下列问题:
(1) 的电子式为____________,
的电子式为____________, 中含有的化学键是____________。
中含有的化学键是____________。
(2)下列关于雾霾的叙述错误的是______(填序号):
A.雾霾中含有硝酸铵和硫酸铵 B. 是形成无机颗粒物的催化剂
是形成无机颗粒物的催化剂
C.雾霾的形成与过度施用氮肥有关 D.雾霾的形成过程涉及氧化还原反应
(3)预防含硫化合物雾霾生成的方法之一是将氨气和二氧化硫通入水中,再充入 充分反应生成一种正盐,该反应的化学方程式为_________。
充分反应生成一种正盐,该反应的化学方程式为_________。
(4)在有氧条件下,催化剂能催化 与
与 反应生成
反应生成 。将一定比例的
。将一定比例的 、
、 和
和 混合气体匀速通入装有催化剂的反应器中反应,测得反应温度高于380℃时,
混合气体匀速通入装有催化剂的反应器中反应,测得反应温度高于380℃时, 的去除率迅速下降,其原因之一是催化剂活性下降,另一重要原因是____________。在无氧条件下,反应器中
的去除率迅速下降,其原因之一是催化剂活性下降,另一重要原因是____________。在无氧条件下,反应器中 能将
能将 还原为
还原为 ,当生成
,当生成 时转移电子______
时转移电子______ (可用分数表示)。
(可用分数表示)。
-
环境问题越来越受到人们的重视,研究表明氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。
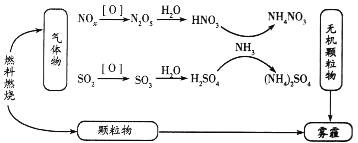
回答下列问题:
(1)NH3的电子式为____________,NH4NO3中含有的化学键是________________:
(2)下列关于雾霾的叙述错误的是________(填序号)
A.雾霾中含有硝酸铵和硫酸铵 B.NH3是形成无机颗粒物的催化剂
C.雾霾的形成与过度施用氮肥有关 D.雾霾的形成过程涉及氧化还原反应
(3)预防含硫化合物雾霾生成的方法之一是将氨气和二氧化硫通入水中,再充入O2充分反应生成一种正盐,该反应的化学方程式为________________________。预防含氮化合物雾霾生成的方法之一是用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸,电解后该溶液的pH_______(填“变大”“变小”或“不变”)。
(4)在有氧条件下,催化剂能催化NH3与NOx反应生成N2,将一定比例的O2、NH3和NOx混合气体匀速通入装有催化剂的反应器中反应,测得反应温度高于380℃时,NOx的去除率迅速下降,其原因之一是催化剂活性下降,另一重要原因是__________________________。在无氧条件下,反应器中NH3能将NO2还原为N2,当生成1mol N2时转移电子________mol(可用分数表示)。
-
近段时间,全国范围内的雾霾天气严重影响了人们的身体健康,环境问题越来越受到人们的重视。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题。请回答下列问题:
(1)汽车尾气中含有较多的NOx和CO,两种气体均会使人体中毒。可以利用如下化学方法将其转化为无毒无害的物质。
已知:N2(g)+O2(g)⇌2NO(g) ΔH=+180 kJ·mol-1
2CO(g)+O2(g)⇌2CO2(g) ΔH=-564 kJ·mol-1
请写出把汽车尾气转化为无毒无害的物质的热化学方程式: _________
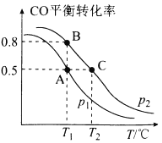
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)⇌CH3OH(g)。在密闭容器中充有2mol CO和4molH2,在催化剂作用下发生反应生成甲醇,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。则该反应为______反应(填“吸热”或“放热”)。若达到平衡状态A时,容器的体积为2L,则在平衡状态B时容器的体积为_______2L(填“>”、“=”或“<”)。该反应T2温度下,若反应进行到1 min达到平衡状态,用CO的分压变化表示的平均反应速率vp(CO)=_______ kPa·min-1,此时的化学平衡常数Kp=_____(Kp是以分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数))。
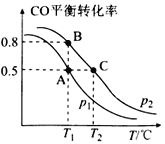
(3)工业上可采用CH3OH⇌CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为______ (填A、B)。
(4)如图为计算机模拟的各步反应的能量变化示意图。
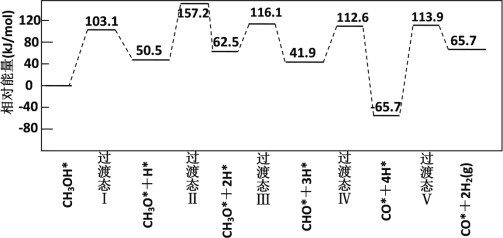
该历程中,放热最多的步骤的化学方程式为________。
-
雾霾天气严重影响了人们的身体健康,环境问题越来越受到人们的重视。汽车尾气中含有较多的NO和CO,两种气体均会使人体中毒。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题。
请回答下列问题
(1)一氧化碳、氢气既是重要的能源,也可以催化还原NO等消除污染,还可以在一定条件下制取CH3OH。
已知:①N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1;
②2H2(g)+O2(g)=2H2O(1) △H=-571.6kJ·mol-1;
③H2O(g)=H2O(1) △H=-44kJ·mol-1。
写出H2与NO反应生成N2和水蒸气的热化学方程式:__。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。在密闭容器中充有10molCO和20molH2,在催化剂作用下发生反应生成甲醇,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。则该反应的△H___0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时平衡常数K=___。
CH3OH(g)。在密闭容器中充有10molCO和20molH2,在催化剂作用下发生反应生成甲醇,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。则该反应的△H___0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时平衡常数K=___。
(3)工业上采用加压条件下,在含冷却装置的吸收塔中,以去离子水为吸收剂吸收NO,得到40%的硝酸。原理如下:
2NO(g)+O2(g) 2NO2(g) △H=-114kJ·mol-1
2NO2(g) △H=-114kJ·mol-1
3NO2(g)+H2O(l) 2HNO3(aq)+NO(g) △H=-69.92kJ·mol-1
2HNO3(aq)+NO(g) △H=-69.92kJ·mol-1
采用降温操作的一个原因是__。
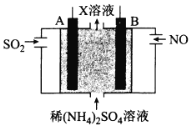
(4)利用电解原理也可以处理工厂烟气。如图为工业生产模拟装置。其中A、B为多孔电极(外接电源未画出),则A为___极(填“正”“负”“阴”或“阳”),电极反应式为___。
-
当今环境问题越来越受到人们的重视。汽车尾气中含有较多的NO和CO,两种气体均会使人体中毒。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题。请回答下列问题
(1)用还原法将NO转化为无污染的物质。已知:
2C(s)+O2(g) 2CO △H1=-221.0KJ/mol
2CO △H1=-221.0KJ/mol
N2(g)+O2(g) 2NO △H2=+180.5KJ/mol
2NO △H2=+180.5KJ/mol
2NO+C(s) CO2(g)+N2(g) △H3=-573.75KJ/mol
CO2(g)+N2(g) △H3=-573.75KJ/mol
请写出CO与NO生成无污染气体CO2与N2的热化学方程式_______________________。
(2)在一定温度下,向甲、乙、丙三个恒容密闭容器中加入一定量的NO和足量的焦炭,反应过程中测得各容器中c(NO)(mol/L)随时间(s)的变化如下表。
已知:三个容器的反应温度分别为T甲= 500℃、T乙= 500℃、T丙= a℃
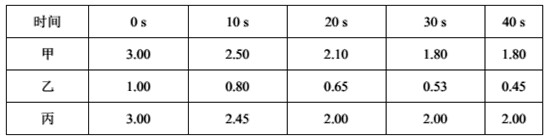
甲容器中,该反应的平衡常数K=_______。丙容器的反应温度a _______500℃(填“˃”、“<”或“=”),理由是_______________________________。
(3)某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。
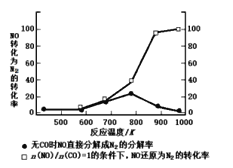
①若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为_________。
②在n(NO)/n(CO)=1的条件下,为更好的除去NO物质,应控制的最佳温度在_____K左右。
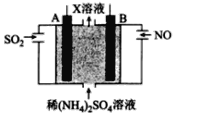
(4)利用电解原理也可以处理NO。下图为工业生产模拟装置。其中A、B为多孔电极(外接电源未画出),则B为___________极(填“正”“负”“阴”或“阳”,),A电极反应式为______________________。
-
环境问题越来越受到人们的重视,“绿水青山就是金山银山”的理念已被人们认同。运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染具有重要意义。回答下列问题:
(1)亚硝酰氯(C—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为______________________。
相关化学键的键能如下表所示:
| 化学键 | Cl—Cl | N≡O(NO气体) | Cl—N | N=O |
| 键能/(kJ·mol-1) | 243 | 630 | 200 | 607 |
(2)为研究汽车尾气转化为无毒无害的物质的有关反应,在某恒容密闭容器中充入4molCO和4 mol NO,发生反应2CO+2NO 2CO2+N2,平衡时CO的体积分数与温度(T1<T2)压强的关系如图所示:
2CO2+N2,平衡时CO的体积分数与温度(T1<T2)压强的关系如图所示:
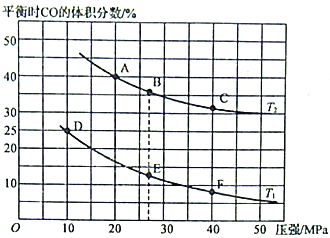
①该可逆反应达到平衡后,为在提高反应速率的同时提高NO的转化率,可采取的措施有___________(填标号)。
a.按体积比1:1再充入CO和NO b.改用高效催化剂
c.升高温度 d.增加CO的浓度
②由图可知,压强为20MPa、温度为T2下的平衡常数Kp=___________MPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。保留4位小数)。
③若在B点对反应容器降低温度至T1的同时缩小体积至体系压强增大,达到新的平衡状态时,可能是图中A~F点中的___________点(填标号)。
(3)有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为______________________。
(4)用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中 ,则该混合溶液的pH=___________(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
,则该混合溶液的pH=___________(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
(5)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:
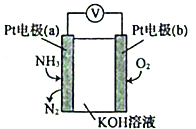
①电极b上发生的是___________反应(填“氧化”或“还原”)。
②电极a的电极反应为_______________________。
-
环境问题越来越受到人们的重视,“绿水青山就是金山银山”的理念已被人们认同。运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染具有重要意义。回答下列问题:
(1)亚硝酰氯(Cl—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为______________________。相关化学键的键能如下表所示:
| 化学键 | Cl—Cl | N≡O(NO气体) | Cl—N | N=O |
| 键能/(kJ·mol-1) | 243 | 630 | 200 | 607 |
(2)有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为______________________。
(3)用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中 ,则该混合溶液的pH=___________(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
,则该混合溶液的pH=___________(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
-
雾霾严重危害人类健康和生态环境,开发稳定高效的脱硫脱硝工艺技术是国内外研究的热点。研究表明,氮氧化物(NOx)和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如下图所示。
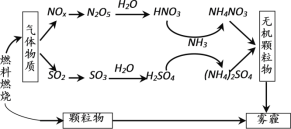
(1)NH3的电子式是_________。
(2)NH4NO3溶液中的离子浓度由大到小顺序是_________。
(3)①已知:SO2生成SO3总反应方程式是
2SO2(g)+O2(g)  2SO3(g) ΔH=-196.6 kJ/mol
2SO3(g) ΔH=-196.6 kJ/mol
此反应可通过如下两步完成:
2NO(g)+O2 (g )  2NO2(g) ΔH1=-113 kJ/mol
2NO2(g) ΔH1=-113 kJ/mol
NO2(g)+SO2(g)  SO3(g)+NO(g) ΔH2=_________。
SO3(g)+NO(g) ΔH2=_________。
② 一定温度下,向2 L恒容密闭容器中充入NO2和SO2各1 mol,5min达到平衡,此时容器中NO2和NO的浓度之比为1∶3,则NO2的平衡转化率是_________。
(4)利用NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。
① 制备少量NaClO2,其装置如下图所示:
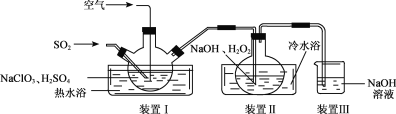
装置I控制温度在35~55℃,通入SO2将NaClO3还原为ClO2(沸点:11℃),反应的离子方程式是_____________________________________________,
装置Ⅱ中反应生成NaClO2,此反应中作为氧化剂的是_______________ ,反应后溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH-外还可能含有的一种阴离子是_______________ 。
② 用制得的NaClO2/H2O2酸性复合吸收剂同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液pH对脱硫脱硝的影响如下图所示:
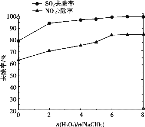
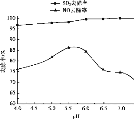
从上图中可知脱硫脱硝最佳条件是_________。图 中SO2的去除率随pH的增大而增大,而NO 的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因是______________________________。
-
近段时间,全国范围内的雾霾天气严重影响了人们的身体健康,环境问题越来越受到人们的重视。汽车尾气中含有较多的NO和CO,两种气体均会使人体中毒。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题
请回答下列问题
(1)一氧化碳、氢气既是重要的能源,也可以催化还原NO等消除污染,还可以在一定条件下制取CH3OH。
已知:①N2(g)+O2(g)===2NO(g) △H=+180.5kJ·mol-1;
②2H2(g)+ O 2(g)===2H2O(1) △H=-571.6kJ·mol-1;
③H2O(g)===H2O(1) △H=-44kJ·mol-1。
写出H2与NO反应生成N2和水蒸气的热化学方程式:______________________。
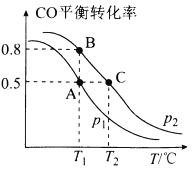
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。在密闭容器中充有10 mol CO和20molH2,在催化剂作用下发生反应生成甲醇,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。则该反应的△H___________0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时平衡常数K=___________,此时容器的体积为___________L。
CH3OH(g)。在密闭容器中充有10 mol CO和20molH2,在催化剂作用下发生反应生成甲醇,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。则该反应的△H___________0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时平衡常数K=___________,此时容器的体积为___________L。
(3)工业上采用加压条件下,在含冷却装置的吸收塔中,以去离子水为吸收剂吸收NO,得到40%的硝酸。原理如下:
2NO(g)+O2(g) 2NO2(g) △H=-114 kJ/mol
2NO2(g) △H=-114 kJ/mol
3NO2(g)+H2O(l) 2 HNO3(aq)+ NO(g) △H=-69 92 kJ/molo
2 HNO3(aq)+ NO(g) △H=-69 92 kJ/molo
采用降温操作的两个原因是_________________________________。
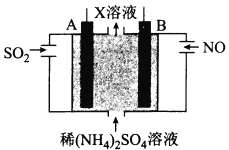
(4)利用电解原理也可以处理工厂烟气。如图为工业生产模拟装置。其中A、B为多孔电极(外接电源未画出),则A为___________极(填“正”“负”“阴”或“阳”),电极反应式为______________________。Ⅹ溶液中溶质的成分为___________(填化学式)。
-
“雾霾”成为人们越来越关心的环境问题。雾霾中含有二氧化硫、氮氧化物和可吸入颗粒物等污染性物质。请回答下列问题:
(1)汽车尾气是雾霾形成的原因之一。尾气治理可用汽油中挥发出来的烃类物质(CxHy)催化还原尾气中的NO气体,该过程的化学方程式为___________________。
(2)冬季燃煤供暖产生的废气也是雾霾的主要来源之一。经研究发现将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:
2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH
N2(g)+2CO2(g) ΔH
已知:①N2(g)+O2(g) 2NO(g) ΔH1=+180.5 kJ·mol-1
2NO(g) ΔH1=+180.5 kJ·mol-1
②2CO(g) 2C(s)+O2(g) ΔH2=+221 kJ·mol-1
2C(s)+O2(g) ΔH2=+221 kJ·mol-1
③C(s)+O2(g) CO2(g) ΔH3=-393.5 kJ·mol-1
CO2(g) ΔH3=-393.5 kJ·mol-1
则ΔH=_____________。
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图一所示,电极材料为石墨。
①a表示_____离子交换膜(填“阴”或“阳”)。A~E分别代表生产中的原料或产品,其中C为硫酸,则A表示_________,E表示___________。
②阳极的电极反应式为___________________________。
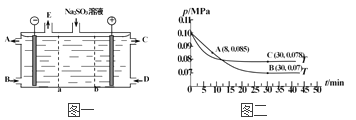
(4)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g) 2SO3(g)。若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2) ∶n(O2)=2∶1],测得容器内总压强与反应时间如图二所示。
2SO3(g)。若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2) ∶n(O2)=2∶1],测得容器内总压强与反应时间如图二所示。
①图中A点时,SO2的转化率为____________。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率vc(正)与A点的逆反应速率vA(逆)的大小关系为vc(正)______vA(逆)(填“>”、“<”或“=”)。
③图中B点的压强平衡常数Kp=_______________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。

















