-
某无色溶液中可能含有Na+、K+、NH
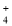 、Mg2+、Cu2+、SO
、Mg2+、Cu2+、SO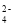 、SO
、SO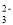 、Cl-、Br–、CO
、Cl-、Br–、CO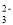 中的若干种,各离子浓度均为 0. l mol•L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:
中的若干种,各离子浓度均为 0. l mol•L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验: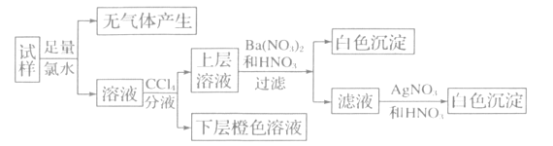
则关于原溶液的判断中正确的是
A.无法确定原溶液中是否存在Cl-
B.若步骤中 Ba(NO3)2 和 HNO3的混合溶液改用 BaCl2和盐酸, 则对溶液中离子的判断无影响
C.肯定存在的离子是NH
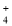 、Mg2+、SO
、Mg2+、SO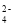 、Br–
、Br–D.是否存在 Na+ 、K+需要通过焰色反应来确定
高二化学单选题困难题查看答案及解析
-
二氯化二硫 ( S2Cl2)是一种黄红色液体,常用作橡胶的低温硫化剂和粘结剂。S2Cl2分子中各原子最外层均有8个电子。S2Cl2遇水反应会产生淡黄色沉淀和刺激性气味气体。下列说法不正确的是
A.S2Cl2的结构式为 Cl—S —S—Cl
B.S2Cl2 可能使品红溶液褪色
C.S2Cl2 与水反应时 ,氧化产物与还原产物的物质的量之比为 1 : 3
D.将S2Cl2气体通入 AgNO3溶液中,若有白色沉淀产生,则 S2Cl2气体中有 HCl
高二化学单选题困难题查看答案及解析
-
常温下,向l0mL0.1mol/L 的HR 溶液中逐渐滴入0.lmol/L 的NH3·H2O 溶液,所得溶液pH 及导电性变化如图。下列分析不正确的是
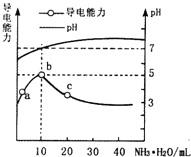
A. a~b点导电能力增强,说明HR为弱酸
B. b点溶液c(NH3·H2O)=c(R-)+c(H+)-c(OH-)
C. c点溶液,存在c(NH4+)>c(R-)>c(OH-)>c(H+)
D. 常温下,HR 和NH3·H2O 的电离平衡常数近似相等
高二化学单选题困难题查看答案及解析
-
硼氢化物NaBH4(B元素的化合价为+3价)燃料电池(DBFC), 由于具有效率高、产物清洁无污染和燃料易于储存和运输等优点,被认为是一种很有发展潜力的燃料电池。其工作原理如下图所示,下列说法正确的是
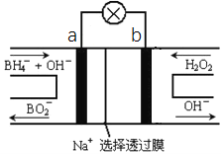
A.电池的负极反应为BH4-+2H2O-8e-=BO2-+8H+
B.放电时,每转移2mol电子,理论上需要消耗9.5gNaBH4
C.电池放电时Na+从b极区移向a极区
D.电极a采用MnO2,MnO2既作电极材料又有催化作用
高二化学单选题困难题查看答案及解析
-
下列有关同分异构体的说法正确的是
A.甲醇在铜催化和加热条件下生成的产物不存在同分异构体
B.2-氯丁烷(CH3CHClCH2CH3)与NaOH乙醇溶液共热,得到三种烯烃。
C.有机物
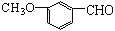 的同分异构体中,其中属于酯且苯环上有2个取代基的同分异构体有2种。
的同分异构体中,其中属于酯且苯环上有2个取代基的同分异构体有2种。D.分子式为C5H10O2的有机物中含有
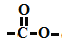 结构的同分异构体有12种
结构的同分异构体有12种高二化学单选题困难题查看答案及解析
-
下列实验能达到预期目的是
编号
实验内容
实验目的
A
室温下,用pH试纸分别测定浓度为0.1 mol·L-1Na2CO3溶液和0.1 mol·L-1CH3COONa溶液的pH
比较H2CO3和CH3COOH的酸性强弱
B
室温下,分别测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH
比较S、C元素的非金属性强弱
C
相同条件下,向一支试管中加入2 mL 5% H2O2和1 mL H2O,向另一支试管中加入2 mL 5% H2O2和1 mL FeCl3溶液,观察并比较实验现象
探究FeCl3对H2O2分解速率的影响
D
向2支盛有5 mL不同浓度NaHSO3溶液的试管中,同时加入2 mL 5% H2O2溶液,观察并比较实验现象
探究浓度对反应速率的影响
A.A B.B C.C D.D
高二化学单选题困难题查看答案及解析
-
下列溶液中微粒的物质的量浓度关系正确的是
A.20mL0.1000mol/L氨水用0.1000mol/L的盐酸滴定,当滴入盐酸达30mL时,溶液中:c(
 )+c(H+)<c(OH-)+c(Cl-)
)+c(H+)<c(OH-)+c(Cl-)B.0.1mol/L的NaHX溶液pH为4,该溶液中:c(HX-)>c(H2X)>c(X2-)>c(H+)>c(OH-)
C.在Na2S稀溶液中,c(OH-)=c(H+)+2c(H2S)+c(HS-)
D.0.1mol/L(NH4)2Fe(SO4)2溶液:c(
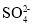 )>c(
)>c( )>c(H+)>c(Fe2+)
)>c(H+)>c(Fe2+)高二化学单选题困难题查看答案及解析
-
青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有
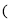 不考虑立体异构
不考虑立体异构

A.6种 B.7种 C.8种 D.9种
高二化学单选题困难题查看答案及解析
-
“84”消毒液 (主要成分为NaClO)广泛应用于杀菌消毒。某化学学习小组用甲烷燃料电池电解饱和食盐水制备“84”消毒液,装置如图所示,a、b、c、d 均为惰性电极,下列说法正确的是
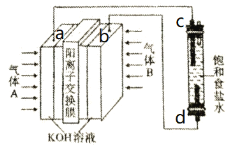
A.c是阳极
B.甲烷发生的电极反应方程式为CH4-8e-+8OH-=CO2↑+6H2O
C.消耗2.24L (标准状况)甲烷,K+通过交换膜向左室移动0.8 mol
D.电解装置中的总反应为NaCl+H2O
 NaClO+H2↑
NaClO+H2↑高二化学单选题困难题查看答案及解析
-
25°C时,向50 mL浓度均为1.0 mol/L的醋酸和醋酸钠混合溶液中,缓慢滴加1.0 mol/L的NaOH溶液,所得溶液的pH变化情况如图所示(已知: 25°C时,Ka(CH3COOH) =1.8×10—5)。下列叙述错误的是
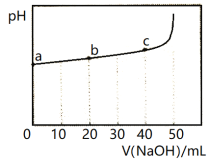
A.V(NaOH)≤50mL时,随V(NaOH)增大,溶液中离子总浓度增大
B.b点溶液中,c(Na+)>c(CH3COOH)
C.a点溶液中,c(H+)约为1.8×10-5 mol/L
D.从a到c的过程中,溶液中
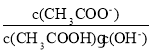 不变
不变高二化学单选题困难题查看答案及解析