-
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)已知CH3OH(l)的燃烧热△H为-238.6kJ·mol-1
CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) △H=-QkJ·mol-1(Q>0)
则Q__________(填“>”“<”或“ =”)238.6。
(2)使Cl2和H2O(g))通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:________________ .
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煆烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为__________。
高二化学计算题简单题查看答案及解析
-
已知
2H2(g)+O2(g)=2H2O(g), △H=-483.6kJ·mol-1
2H2(g)+O2(g)=2H2O(l), △H=-571,6 kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l), △H=-2220kJ·mol-1根据上述热化学方程式,回答下列问题:
(1)H2的燃烧热△H为__________,C3H8的燃烧热△H为__________.
(2)1molH2和2molC3H8组成的混合气体完全燃烧恢复到室温时释放的热量为__________.
(3)现有H2和C3H8的混合气体共5mol,完全燃烧恢复到室温时放热3847kJ,则在混合气体中H2和C3H8的体积比是__________。
高二化学计算题简单题查看答案及解析
-
随着化石能源的减少,新能源的开发利用需求日益迫切。Bunsen热化学循环制氢工艺由下列三个反应组成:
SO2(g)+I2(g)+2H2O(g)=2HI(g)+H2SO4(l) △H=a kJ·mol-1
2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g) △H=b kJ·mol-1
2HI(g)=H2(g)+I2(g) △H=c kJ·mol-1则:2H2O(g)=2H2(g)+O2(g) △H=__________
高二化学计算题简单题查看答案及解析
-
在2 L密闭容器中进行反应:mX(g)+nY(g) ===pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
物质
时间
X
Y
Z
Q
起始/mol
0.7
1
2 min末/mol
0.8
2.7
0.8
2.7
3 min末/mol
0.8
已知2 min内v(Q)=0.075 mol·L-1·min-1,v(Z) ∶v(Y) =1 ∶2 ,
(1)试确定以下物质的物质的量:起始时n(Y)=______,n(Q)=______;
(2)方程式中m=________,n=________,p=________,q=________;
(3)用Z表示2 min内的反应速率_______________________________;
(4) 2 min时,Z的转化率为__________________。
高二化学计算题简单题查看答案及解析
-
一定质量的液态化合物XY2与标准状况下的一定质量的O2恰好完全反应,化学方程式为:XY2(l)+3O2(g)===XO2(g)+2YO2(g),冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56g/L,则:
(1)反应前O2的体积是________。
(2)化合物XY2的摩尔质量是________。
高二化学计算题简单题查看答案及解析
-
常温下电解200 mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如右图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:
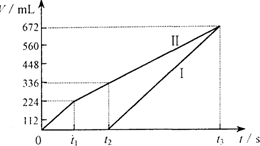
(1)原混合溶液NaCl和CuSO4的物质的量浓度。
(2)t2时所得溶液的pH。
(3)电解至t3时,消耗水的质量。
高二化学计算题简单题查看答案及解析
-
在溶液中,反应A+2B
C分别在三种不同实验条件下进行,它们的起始浓度均为
、
及
。反应物A的浓度随时间的变化如下图所示。
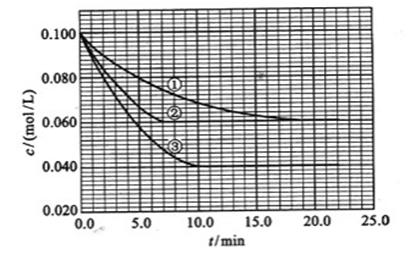
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。
②_______________;
③_______________;
(2)该反应的
_________0,
(以下要写出计算过程)
(3)求:实验②平衡时B的转化率和实验③平衡时C的浓度为
(4)求:该反应进行到4.0min时的平均反应速度率:
实验②:
实验③:
高二化学计算题简单题查看答案及解析
-
室温时,将0.05mol/L的盐酸溶液和未知浓度的NaOH溶液以1:2的体积比混和,所得溶液的pH=12,求NaOH溶液的物质的量浓度
高二化学计算题简单题查看答案及解析
-
室温时,将20mL某气态烃与过量的氧气混合,充分燃烧后冷却至室温,发现混合气体的体积减少60mL,将所得混合气体通过苛性钠溶液后,体积又减少80mL。
(1)通过计算确定气态烃分子式
(2)若该烃能使溴水和高锰酸钾褪色,且该烃与H2加成后的产物有三个甲基,请写出该烃的结构简式。又知该烃在一定的温度、压强和催化剂的作用下,生成一种高聚物,写出其方程式
高二化学计算题简单题查看答案及解析
-
(6分)有机物A由碳、氢、氧三种元素组成。现取23 g A与28 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重27 g,碱石灰增重22 g。回答下列问题:
(1)23 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
高二化学计算题简单题查看答案及解析