-
化合物A含有C、H、O三种元素,相对分子质量为60,其中碳的质量分数为60%,氢的质量分数为13.3%。A在催化剂Cu的作用下被氧气氧化成B,B不能发生银镜反应。 求:
(1)分子式____________
(2)A的结构简式_______________
高二化学计算题简单题查看答案及解析
-
(1)常温下,有pH值为12的NaOH溶液100 mL,欲将其pH值变为11,采取下列三种措施(设混合后溶液的体积等于两混合溶液体积之和)。请回答有关问题:
①若加水,应加入约________ mL。
②若用pH=10的NaOH溶液,应加入此NaOH溶液________ mL。
③若用pH=2的盐酸,应加入________ mL。
(2)pH=2的HA、HB两种酸溶液各1mL,分别加水稀释到1000mL, 其pH的变化如图所示
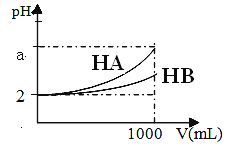
①稀释前两溶液的浓度c(HA)________c(HB)(填>.<.=,或无法确定)
② HB _______ 是弱酸 (填“一定”、“可能”或“一定不”)
③若 a = 5,则HA酸是否是强酸 ____(填“一定是”、“可能是”、 “一定不是”或“无法确定”)
④稀释后的溶液中,由水电离产生的c(H+): HA中_____ HB中(填>.<.=,或无法确定)
高二化学计算题简单题查看答案及解析
-
为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验:
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成气体(标准状况,下同)的体积为b L。反应的化学方程式是_________________________________________________________;样品中铝的质量是________ g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是__________________________________________________;氧化铁与铝的质量比是________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=________。
高二化学计算题简单题查看答案及解析
-
氢气是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为________________
②该反应的热化学方程式为_____________________
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:Mg(s)+H2(g)=MgH2(s)ΔH1=-74.5kJ·mol-1,Mg2Ni(s)+2H2(g)=Mg2NiH4(s)ΔH2,Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1,则ΔH2=____________kJ·mol-1。
高二化学计算题简单题查看答案及解析
-
(1)实验测得,通常情况下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则表示H2燃烧热的热化学方程式为__________________________________________。
(2)CuCl(s)和O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是____________________________。
高二化学计算题简单题查看答案及解析
-
某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。

(1)X的转化率是_______;
(2)由图中所给数据进行分析,该反应的化学方程式为_______________;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=__________;
(4)当反应进行到第___min,该反应达到平衡。若三种物质都是气体,平衡时Y所占体积的百分比为______。
高二化学计算题简单题查看答案及解析
-
25℃时,在2L 0.3mol/L的HF溶液中,有0.02mol的HF电离成离子,求该温度下HF的电离常数。_____________
高二化学计算题简单题查看答案及解析
-
在2L密闭容器中进行反应:mX(g)+nY(g)⇌pZ(g)+qQ(g),式中m、n、p、q为化学计量数.在0~3min内,各物质物质的量的变化如下表所示:
物质
X
Y
Z
Q
时间
起始/mol
0.7
1
2min末/mol
0.8
2.7
0.8
2.7
3min末/mol
0.8
已知:2min内v(Q)=0.075mol•L﹣1•min﹣1,v(Z):v(Y)=1:2。
(1)2min内Z的反应速率v(Z)=_______________________。
(2)试确定以下物质的相关量:起始时n(Y)=______,n(Q)=______。
(3)方程式中m=______,n=______,p=______,q=______。
(4)对于该反应,能增大正反应速率的措施是___________
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度
(5)该反应达到化学平衡状态时___________
A.反应停止了
B.正反应速率与逆反应速率均为0
C.反应物与生成物浓度相等
D.正反应速率与逆反应速率相等
高二化学计算题简单题查看答案及解析
-
常温下,有pH=12的NaOH溶液100 mL,若将其pH变为11(溶液混合忽略体积变化;计算结果保留到小数点后一位)。
(1)若用pH=10的NaOH溶液,应加入_________mL。
(2)若用pH=2的盐酸,应加入_________mL。
(3)若用水稀释,则加入水的体积为____________________ mL。
(4)常温下,设pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=11的NaOH溶液中由水电离出的H+浓度为c2,则c1/c2=_________。
(5)常温下,pH=11的NaOH溶液aL与pH=5的H2SO4溶液bL混合,若所得混合溶液呈中性,则a∶b=_________。
高二化学计算题简单题查看答案及解析
-
苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是C8H10(g)
C8H8(g)+H2(g) ΔH=+125kJ·mol-1。某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内物质的量,得到数据如下表:
时间/min
0
10
20
30
40
n(C8H10)/mol
0.40
0.30
0.26
n2
n3
n(C8H8)/mol
0.00
0.10
n1
0.16
0.16
(1)当反应进行到20min时,该段时间内H2的平均反应速率是________。
(2)该温度下,该反应的化学平衡常数是________(保留两位有效数字)。
(3)若保持其他条件不变,用0.40mol H2(g)和0.40mol C8H8(g)合成C8H10(g),当有30kJ热量放出时,该反应中H2的转化率是________。
高二化学计算题简单题查看答案及解析