-
在500mLNaCl和NaBr的混合溶液中,加入200mL0.05ml/L的AgNO3溶液,生成1.326g沉淀;往滤液中加入过量盐酸,又得到0.287g沉淀。求原混合液中Cl- 和Br-的物质的量浓度。
高三化学计算题中等难度题查看答案及解析
-
某混合气体由两种气态烃组成。取2.24 L该混合气体,完全燃烧后得到4.48 L二氧化碳和3.6 g水(上述气体体积都已折算为标准状况下的数据)。试通过计算,确定混合气体的可能组合。
高三化学计算题简单题查看答案及解析
-
(8分)含氮废水进入水体而对环境造成的污染越来越严重,环境专家认为可以用金属铝将水体中的NO3-还原为N2,从而消除污染。其反应的离子方程式是:
6NO3-+ 10Al + 18H2O → 3N2↑+ 10Al(OH)3 + 6OH-
(1)现在要除去1m3含氮元素0.3mol的废水中的NO3-(设氮元素都以NO3-的形式存在,下同),则至少需要消耗金属铝__________g。
(2)有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同。
① 写出镁和含氮废水反应的离子方程式:___________________________________
② 已知金属镁是从海水中提取的MgCl2,通过电解制得的。若要除去1m3含氮元素0.3mol的废水中的NO3-,则至少需要含0.5%(质量分数)MgCl2的海水_________ kg。
高三化学计算题简单题查看答案及解析
-
(6分)浓硫酸与铜在加热时反应,生成二氧化硫气体的体积为2.24L(标准状况).试计算:
(1)反应后生成硫酸铜的质量
(2)若将生成的硫酸铜配制成500mL溶液,则该溶液中溶质的物质的量浓度是多少?
高三化学计算题简单题查看答案及解析
-
取A、B两份物质的量浓度相等的NaOH溶液,体积均为50 mL,分别向其中通入一定量的CO2后,再分别稀释到100 mL,在稀释后的溶液中分别逐滴加0.1 mol/L的盐酸,产生的CO2的体积(标准状况)与所加盐酸的体积关系如图所示:
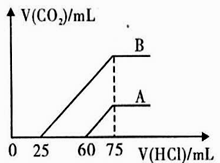
(1)原NaOH溶液的物质的量浓度_________________。
(2)B份混合溶液与盐酸反应产生气体的最大体积为________mL(标准状况)。
高三化学计算题中等难度题查看答案及解析
-
向130mL某浓度的硫酸溶液中加入一定量的铜片,在微热条件下反应,待铜片完全溶解,冷却后将溶液稀释至500mL,再加入过量铁粉,使之充分反应,生成的气体在标况下的体积为16.8L;过滤得到残留固体,经干燥、称量,比原铁粉质量减轻了35.6g。
(1)与硫酸铜反应的铁的质量为_________g。
(2)原浓硫酸的物质的量浓度为__________。
高三化学计算题中等难度题查看答案及解析
-
在标准状况下进行甲、乙、丙三组实验:各取30mL同浓度的盐酸溶液,加入不同质量的同一种镁铝合金粉末,产生气体,有关数据记录如下:

试回答:
(1)计算出盐酸的物质的量浓度为__________________mol/L(保留两位有效数字)。
(2)镁、铝的物质的量之比为__________________。
高三化学计算题中等难度题查看答案及解析
-
将MnO2与FeSO4溶液、硫酸充分反应后过滤,将滤液加热至60℃后,再加入Na2CO3溶液,最终可制得碱式碳酸锰[aMnCO3·bMn(OH)2·cH2O]。
(1)用废铁屑与硫酸反应制备FeSO4溶液时,所用铁屑需比理论值略高,原因是 ,反应前需将废铁屑用热Na2CO3溶液浸泡,其目的是 。
(2)为测定碱式碳酸锰组成,取7.390 g样品溶于硫酸,生成CO2 224.0 mL(标准状况),并配成500 mL溶液。准确量取10.00 mL该溶液,用0.0500 mol·L-1 EDTA(化学式Na2H2Y)标准溶液滴定其中的Mn2+(原理为Mn2+ +H2Y2-=MnY2-+2H+),至终点时消耗EDTA标准溶液28.00 mL。通过计算确定该样品的化学式。(写出计算过程)
高三化学计算题困难题查看答案及解析
-
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42—等杂质,提纯工艺线路如图所示:
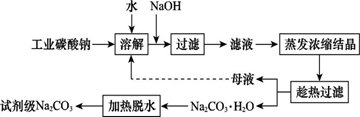
Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
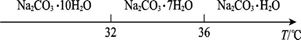
Ⅱ.有关物质的溶度积如下
物质
CaCO3
MgCO3
Ca(0H)2
Mg(OH)2
Fe(OH)3
Ksp
4.96×10-9
6.82×10-6
4.68×10-6
5.61×10-12
2.64×10-39
回答下列问题:
(1)加入NaOH溶液时,反应的离子方程式为________。向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=________。
(2)“母液”中除了含有Na+、CO32—外,还含有________等离子。
(3)有人从“绿色化学”角度设想将“母液”沿流程中虚线进行循环使用。请你分析在实际工业生产中是否可行:________(填“可行”或“不可行”),并说明理由:________ 。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g)
=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g)
=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式:________。
高三化学计算题中等难度题查看答案及解析
-
[s1] 将5.1 g镁铝合金溶于600 mL 0.5 mol·L-1H
SO
溶液中,完全溶解后再加入1.0 mol·L-1的NaOH溶液,得到沉淀的质量为13.6 g,继续滴加NaOH溶液时则沉淀会减少。
(1)当加入___▲__mLNaOH溶液时,可使溶解在硫酸中的Mg
和Al
恰好完全沉淀。
(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积。(列出算式)
[s1]33.
高三化学计算题极难题查看答案及解析