-
硫化钠在无机制备、废水处理等领域常用作沉淀剂,其水溶液称为“臭碱”。可在特殊条件下以硫酸钠固体与炭粉为原料制备:Na2SO4+2C
 Na2S+2CO2↑
Na2S+2CO2↑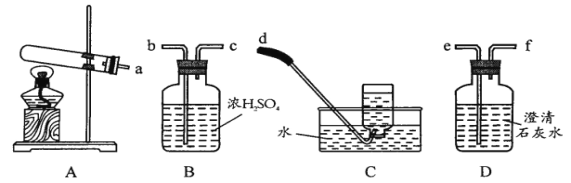
(1)硫化钠固体在保存时需注意________,原因是________。
(2)实验室用上图装置以Na2SO4与炭粉为原料制备Na2S并检验气体产物、进行尾气处理。步骤如下:
①连接仪器顺序为________(按气流方向,用小写字母表示);
②检查装置气密性;③________;
④加热,进行实验。
(3)若 a mol Na2SO4和2 a mol C按上述步骤充分反应,实际得到Na2S小于amol,则实验改进方案是________。
某同学从氧化还原角度分析固体产物中可能含有少量Na2SO3,请设计实验证明其猜测是否合理(供选择的试剂有:酚酞溶液、硝酸、稀盐酸、蒸馏水) ________。
(4)经实验测定,硫酸钠与炭粉在一定条件下反应还可生成等物质的量的两种盐和体积比为1︰3的CO2和CO两种气体。反应方程式为________。
高三化学实验题中等难度题查看答案及解析
-
已知:pCu=-1gc(Cu+),pX=-lgc(X-)。298K时,Ksp(CuCl)=a×10-6,Ksp(CuBr)=b×10-9,Ksp(CuI)=c×10-12。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所示。下列说法正确的是
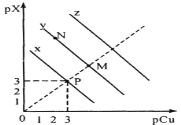
A. 298K时,在CuCl的饱和溶液中加入少量NaCl,c(Cu+)和c(Cl-)都减小
B. 图中x代表CuI曲线,且P点c(Cu+)=c(I-)
C. 298K时增大M点的阴离子浓度,则y上的点向N点移动
D. 298K时CuBr(s)+I-(aq)
 CuI(s)+Br-(aq)的平衡常数K的数量级为103或102
CuI(s)+Br-(aq)的平衡常数K的数量级为103或102高三化学单选题中等难度题查看答案及解析
-
港珠澳大桥设计寿命120年,对桥体钢构件采用了多种防腐方法。下列分析错误的是
A. 防腐原理主要是避免发生反应:2Fe+O2+2H2O===2Fe(OH)2
B. 钢构件表面喷涂环氧树脂涂层,是为了隔绝空气、水等防止形成原电池
C. 采用外加电流的阴极保护时需外接镁、锌等作辅助阳极
D. 钢构件可采用不锈钢材料以减缓电化学腐蚀
高三化学单选题简单题查看答案及解析
-
短周期主族元素X、Y、Z、W、R、Q原子序数依次增大。由这些元素组成的化合物甲、乙、丙、丁的0.1mol/L水溶液pH如下表,丙、丁为二元化合物。甲溶液逐滴滴入丙溶液中,先产生白色沉淀,后沉淀消失;乙的水溶液可除油污。下列说法一定正确的是

A. W和Q形成的化合物只含有离子键
B. Y和Z的氢化物沸点:Y<Z
C. 离子半径:r(Q>r(R)>r(Z)
D. Y和Q氧化物的水化物酸性:Q>Y
高三化学单选题中等难度题查看答案及解析
-
NA代表阿伏加德罗常数的值。下列判断正确的是
A. 1LpH=13的Ba(OH)2溶液中含OH-的数目为0.2NA
B. 46gCH3CH2OH含C-H键数目为6NA
C. 4.6gNa与含0.1 mol CH3COOH的稀醋酸完全反应,转移的电子数为0.1NA
D. 2.24LCH4和0.5 molCl2充分反应所得混合物中氯原子数为NA
高三化学单选题中等难度题查看答案及解析
-
下列实验操作不能达到实验目的的是
选项
实验目的
实验操作
A
除去酯化反应后乙酸乙酯中的杂质
振荡实验后的饱和Na2CO3溶液,分液
B
验证Mg(OH)2的溶解
向盛有少量Mg(OH)2固体的试管中加入NH4Cl溶液
C
观察Fe(OH)2白色絮状沉淀生成
向含有铁粉的FeSO4溶液中加入NaOH溶液
D
检验阿司匹林片剂中含有淀粉
将浓硝酸滴到阿司匹林片上
A. A B. B C. C D. D
高三化学单选题中等难度题查看答案及解析
-
有机物X、Y、Z的结构简式分别为
 。下列分析正确的是
。下列分析正确的是A. Y、Z互为同系物
B. Y中最多有4个C原子处于同一直线上
C. X、Z的二氯代物数目相同
D. 可用酸性KMnO4溶液一次区分X、Y、Z三种物质
高三化学单选题中等难度题查看答案及解析
-
生活中下列物质的有关说法错误的是
A. 食盐和白醋都可作调味剂
B. 糖类和蛋白质都可发生水解
C. 液化石油气和天然气都是含烃混合物
D. 双氧水和碘酒都可作医用消毒剂
高三化学单选题简单题查看答案及解析
-
化学方程式是能够直接形象地表示化学反应过程与特征的一种符号,书写化学方程式是我们必须掌握的一项基本技能。请按照要求完成下列空白。
Ⅰ.生活中很多现象和原理都可以用化学反应来解释:
(1)写出泡沫灭火器反应原理的离子方式:___________________。
(2)用ClO2进行饮用水处理比使用Cl2具有更高的优越性,不仅杀菌消毒效率高,不产生致癌的有机氯化物,而且还能除去水中的Fe2+、Mn2+。请写出用ClO2除去饮用水中Mn2+的离子方程式_________(已知Mn2+转变为MnO2, ClO2转变为ClO2—)。
Ⅱ.根据体系中的物质及物质的性质,我们可以推测出该体系所发生的变化,并能用方程式表示出来:
(1)某一反应体系有反应物和生成物共六种物质:N2O、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O。写出该反应的化学方程式_____________。
(2)将NaClO溶液逐滴滴入含淀粉的KI溶液中,溶液变蓝,继续滴加,溶液颜色先加深,后逐渐变浅,最终消失。经检测得知此时溶液中含有一种含正五价元素的含氧酸根,写出上述变化过程的两个离子反应方程式__。
高三化学综合题中等难度题查看答案及解析
-
工业上由黄铜矿(主要成分 CuFeS2)制取 FeSO4·7H2O 和Cu的主要流程如下:
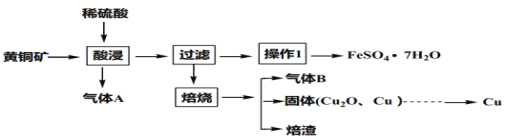
(1)检验酸浸过程中 Fe2+是否被氧化,应选择________(填字母编号)。
A.KMnO4 溶液 B.K3[Fe(CN)6]溶液 C.KSCN 溶液
(2)酸浸过程中主要反应的化学方程式为__________。
(3)某同学向盛有 H2O2 溶液的试管中加入几滴酸化的 FeSO4 溶液,溶液变成棕黄色,发生反应的离子方程式为___________。一段时间后.溶液中有气泡出现,并放热,随后有红褐色沉淀生成;产生气泡的原因是_________,生成沉淀的原因是___________(用平衡移动原理解释)。
高三化学推断题中等难度题查看答案及解析