-
将mg Al2O3和Fe2O3的混合物溶于100mL盐酸中,然后逐滴加入1mol/LNaOH溶液,其结果如图所示:

(1)最初加入V1mLNaOH溶液的作用是____________;
(2)盐酸的物质的量浓度是___________________;
(3)若mg混合物中Al2O3和Fe2O3按不同比例进行上述实验(其他条件不变),则V2的值会不会改变__________(填“会”或 “不会”),(V2—V1)的取值范围是____________。
高一化学计算题困难题查看答案及解析
-
3.84g Fe 和Fe2O3的混合物溶于120mL的盐酸,刚好完全反应。生成0.03 mol H2,向反应后的溶液中加入KSCN检验,溶液不显色。
(1)求原混合物中Fe2O3的质量;
(2)求原盐酸的物质的量浓度。
高一化学计算题困难题查看答案及解析
-
19.2gCu加入到100mL一定浓度的HNO3溶液中,假定两者恰好完全反应,同时产生标准状态下8.96LNO和NO2混合气体(忽略气体的溶解及转化)。求:
(1)混合气体中NO2和NO的体积比 ?
(2)HNO3溶液的物质的量浓度?
高一化学计算题困难题查看答案及解析
-
(5分)0.01mol某液态烷烃完全燃烧需要消耗2.56g氧气,通过计算求该烷烃的化学式。写出全部符合该化学式的烃的结构简式。
高一化学计算题困难题查看答案及解析
-
二氧化氯是一种广谱杀菌消毒剂,有众多的用途,工业上制取二氧化氯的化学方程式如下:2NaClO3 + 2NaCl + 2H2SO4 → 2ClO2↑+ Cl2↑+ 2H2O + 2Na2SO4
(1)完成下列计算:0.2 mol NaClO3完全反应,得到气体的体积为 L(标准状况)。
(2)将27.0 g ClO2溶于水得0.5 L溶液,则ClO2的物质的量浓度为 mol/L。
(3)为使上述反应产生的Cl2转化为ClO2,将得到的混合气体和NaClO2反应,
反应方程式为:2NaClO2 + Cl2 → 2ClO2+ 2NaCl假设NaClO3的转化率为90%,Cl2的转化率为95%,计算由0.2 mol NaClO3最终可制得的ClO2的质量(保留两位小数)。
高一化学计算题困难题查看答案及解析
-
某有机物中只含C、H、O三种元素,相对分子质量为62,3.1g该物质完全燃烧后生成0.1mol二氧化碳和2.7g水,该化合物的分子式。
高一化学计算题困难题查看答案及解析
-
(5分)一定质量的某金属
X和足量的稀H2SO4反应共有0.3mol电子发生转移,生成6.02×1022个
Xn+ ,这些阳离子共有1.3×6.02×1023个质子、1.4×6.02×1023个中子。
(1)求Z、n和A的值。(写过程)
(2)写出该金属与NaOH溶液反应的化学方程式。
高一化学计算题困难题查看答案及解析
-
将0.1molMg 、Al混合物溶于100mL3mol/LHCl中,再滴加1mol/LNaOH 溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V变化如图所示:
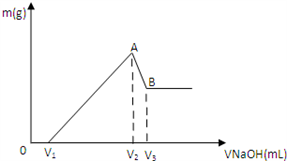
(1)写出A→B段反应的离子方程式_____________。
(2)A点沉淀的总物质的量n= _________________。
(3)欲使Mg2+ 、Al3+刚好沉淀完全,则加入NaOH溶液的体积为多少___________mL?(写出计算过程,下同)
(4)若V1=60mL,则混合物中Mg的物质的量为多少___________? V3点所加NaOH溶液的体积为多少___________mL?
高一化学计算题困难题查看答案及解析
-
取50mL的Na2CO3和Na2SO4 的混合溶液,加入适量Ba(OH)2溶液50mL后,恰好完全反应,过滤得到滤液和12.54g白色沉淀(干燥后),再用足量的稀硝酸处理沉淀,最后沉淀减少到4.66g,并有气体放出。
(1)4.66g白色沉淀是_________(填化学式),写出12.54g白色沉淀加入稀硝酸后变为4.66g所发生反应的离子方程式___________________________;
(2)产生的气体在标准状况下的体积为__________ml;
(3)原混合液中Na2SO4的物质的量浓度______;
(4)计算过滤出12.54g沉淀后,所得滤液中溶质的物质的量浓度(忽略混合溶液体积的变化)______。
高一化学计算题困难题查看答案及解析
-
在实验室里,用50mL的浓盐酸与一定量的MnO2反应,来制取氯气。
(1)用“双线桥法”标出电子转移情况
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
(2)若生成2.8L标准状况时的氯气,请计算:
①理论上需要多少克MnO2参加反应?
②被氧化的HCl的物质的量为多少?
高一化学计算题困难题查看答案及解析