-
I.20mL0.1mol/LBaCl2溶液中Cl-的物质的量浓度为________,Ba2+的物质的量为_______。
II.把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6 LH2(标准状况下)。
(1)合金中镁的物质的量_________。
(2)写出该合金溶于足量NaOH溶液的化学方程式_________。同时产生H2的体积(标准状况下)为____________ 。
III.在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则:
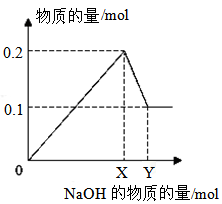
①生成Mg(OH)2的质量为__________;
②X=_______;Y=_________。
高一化学简答题中等难度题查看答案及解析
-
工业上从铝土矿(主要成分是Al2O3,还含有SiO2、Fe2O3等杂质)中提取铝可选用如下工艺流程:
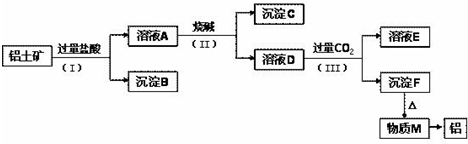
已知:SiO2不溶于水且不与盐酸反应。
请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是______(填操作名称)。
(2)步骤(Ⅱ)中加入的烧碱溶液应该是______(填“少量”或“过量”)。沉淀B的成分是______(填化学式,下同);溶液D中含铝元素的溶质的是______。
(3)①物质M在生产生活中有重要用途,写出沉淀F转化为物质M的化学方程式:______;
②溶液D中通入______CO2生成沉淀F的离子方程式为:______.
高一化学简答题中等难度题查看答案及解析
-
用下面两种方祛可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)制取所需的FeSO4溶液需要的反应物为_______。
(2)生成白色Fe(OH)2沉淀的操作是用长滴管吸取NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是__________。
方法二:在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。

(3)在试管Ⅰ里加入的试剂是________________________________________。
(4)在试管Ⅱ里加入的试剂是________________________________________。
操作:先打开止水夹,使I管中反应一段时间后再夹紧止水夹,实验中观察到I管中溶液被压入II管中,II中发生反应的离子方程式为:_____________。
(5)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是_____________________。
高一化学简答题中等难度题查看答案及解析
-
(1)机智如化学老师的你用固体烧碱配制500mL 0.20 mol L-1的NaOH溶液,需要称取____g固体,定容时除了胶头滴管和玻璃棒,还需要的仪器为______。
(2)语文老师要用36.5% (ρ=1.18g cm-3)的浓盐酸配制0.4 mol L-1的盐酸240 mL,需准确量取36.5%的浓盐酸____mL。
(3)若配制0.5mol L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,下列所配制的硫酸溶液浓度偏低的是_______(填序号)。
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒。
B.移液时容量瓶中有少量蒸馏水。
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切。
E.稀释后没冷却到室温就将溶液转移至容量瓶。
高一化学简答题中等难度题查看答案及解析
-
铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
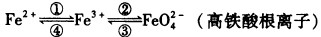
I.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:___________。检验反应后溶液中还存在Fe3+的试剂是__________。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是______,生成1molNa2FeO4转移电子数目为__________。
II.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______,加铁粉后溶液增重的是______;
(2)向Fe2+的溶液中滴加NaOH溶液,现象是___________________ 。
(3)欲除去FeCl2中FeCl3选用合适的试剂和分离方法,并写出相应离子方程式:__________。
高一化学简答题中等难度题查看答案及解析
-
已知铅元素有+2价、+4价两种常用价态,铅及其化合物可用于耐酸设备及X射线防护等。
(1)我国古代炼丹中经常使用到红丹(用X表示),在一定条件下,与过量硝酸能发生非氧化还原反应:X+4HNO3===PbO2+2Pb(NO3)2+2H2O(已配平)。
①PbO2中铅元素的化合价是________,PbO2不是碱性氧化物,判断的依据是_________________________________________________。
②X的化学式是________。
(2)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为____________________________________________。
(3)PbO2在加热的过程中发生分解生成PbO和O2,其失重曲线如图所示,已知失重曲线上的a点为样品分解40%的残留固体。若a点固体组成表示为PbOx,则x=________。
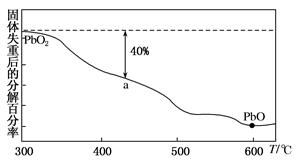
高一化学简答题困难题查看答案及解析
-
在生产和生活中,金属材料几乎无处不在。
(1)铝是一种活泼金属,具有较强的还原性。
①金属铝在高温下与三氧化二铁反应,2Al+Fe2O3=Al2O3+2Fe,称为铝热反应。试 用双线桥法表示电子转移情况:____________________。
②能否用铝制容器盛装NaOH溶液?________(填“能”或“不能”),
(2)将镁、铝的混合物共0.2 mol,溶于200 mL 4 mol·L﹣1的盐酸溶液中,然后再滴加2 mol·L﹣1的NaOH溶液。请回答下列问题:
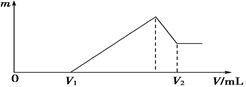
①若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示。当V1=160 mL时,则金属粉末中n (Al)=________________________mol。
②0~V1段发生的反应的离子方程式为______________________________;
③若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=_____________mL;
高一化学简答题中等难度题查看答案及解析
-
实验室需配制4.6 mol·L-1的H2SO4溶液0.5 L。
⑴ 需要浓度为18.4 mol·L-1的浓硫酸_______________ mL;
⑵ 需要用的玻璃仪器除玻璃棒、量筒外还有___________________________;
⑶ 配制过程中下列操作导致溶液浓度偏高的是____________________。
( A)移液时未充分洗涤烧杯和玻棒
( B)移液时未用玻棒引流而使少量液体外溢
( C)定容俯视刻度线
高一化学简答题中等难度题查看答案及解析
-
(12分)牛奶放置时间长了会变酸,这是因为牛奶中含有不少乳糖,在微生物的作用下乳糖分解而变成乳酸。乳酸最初就是从酸牛奶中得到并由此而得名的。乳酸的结构简式为
。完成下列问题:
(1)写出乳酸分子中官能团的名称:________ ______。
(2)一定条件下乳酸能发生的反应类型有____ __ __(填序号)。
A.水解反应 B.取代反应 C.加成反应D.中和反应 E.氧化反应 F.酯化反应
(3)写出乳酸与碳酸钠溶液反应的化学方程式:____________ _。
(4)乳酸在浓硫酸作用下,两分子相互反应生成链状结构的物质,写出此生成物的结构简式:____
高一化学简答题简单题查看答案及解析
-
(1)某气态氧化物的化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为___________,R 的相对原子质量为_____________。
(2)已知CO、CO2的混合气体质量共14.4 g,标准状况下体积为8.96L,则可推知该混合气体中含CO________g。
(3)质量比为51∶32∶34的NH3、CH4、H2S,所含质子数之比为_____。
(4)质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水。得到的溶液每亳升质量为q g,物质的量浓度为c。则溶质的相对分子质量为_______。
高一化学简答题困难题查看答案及解析