-
已知在K2Cr2O7的溶液中存在着如下平衡:Cr2O72﹣(橙色)+H2O⇌2CrO42﹣(黄色)+2H+,加入下列物质能使溶液变为橙色的是( )
A.氨水 B.硫酸 C.NaOH D.水
-
已知在K2Cr2O7的溶液中存在着如下平衡:Cr2O72﹣(橙色)+H2O⇌2CrO42﹣(黄色)+2H+,加入下列物质能使溶液变为橙色的是( )
A. 氨水 B. 硫酸 C. NaOH D. 水
-
完成下列问题。
(1)重铬酸钾(K2Cr2O7为橙色,K2CrO4为黄色)溶液存在着如下平衡:Cr2O72-+H2O  2CrO42-+2H+。
2CrO42-+2H+。
①若平衡体系的pH=2,则溶液显___________色。
②能说明该反应达平衡状态的是___________。
a.溶液呈酸性 b.溶液的颜色不变
c.2v(Cr2O72-)=v(CrO42-) d.Cr2O72-和CrO42-的浓度相同
(2)25℃时,2NO2(g) N2O4(g)△H=-56.9kJ/mol。
N2O4(g)△H=-56.9kJ/mol。
①该反应的化学平衡常数表达式_________________________________。
②其它条件不变,缩小容器体积,达到新平衡,此过程的现象:
_______________________________________________________。
③其它条件不变,将该体系升温至100oC,此过程的现象:
_____________________________________________。
(3)明矾[KAl(SO4)2·12H2O]是一种常用的净水剂。
①用离子方程式表示净水的原因:_________________________。
②明矾溶液中滴加Ba(OH)2溶液至SO42- 刚好沉淀完全时,溶液的pH______7(填“>”“=”或“<”,下同)。
③明矾溶液中滴加Ba(OH)2溶液至Al3+刚好沉淀完全时,溶液的pH______7。
④明矾溶液中离子浓度由大到小的顺序:______________________________。
-
(1)重铬酸钾(K2Cr2O7)主要用于制革、印染、电镀等.其水溶液中存在平衡:Cr2O72﹣+H2O 2CrO42﹣+2H+。以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图
2CrO42﹣+2H+。以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图
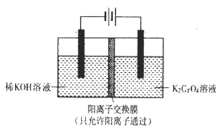
①写出阴极区的电极反应式___________________,透过离子交换膜的离子是____________,移动方向为____________(填“由左向右”或“由右向左)。
②阳极区能得到重铬酸钾溶液的原因为_______________________________________________________。
(2)工业上采用下面的方法处理含有Cr2O72-的酸性工业废水:废水中加入适量NaCl,以铁为电极进行电解,有Cr(OH)3和Fe(OH)3沉淀生成,关于上述方法,下列说法正确的是_______(填字母序号)。
A.阴极反应:2H++2e-===H2↑
B.阳极反应:Fe-3e-===Fe3+
C.在电解过程中当电路转移0.6mol电子时,被还原的Cr2O72-为0.05mol
D.可以将铁电极改为石墨电极
-
在水溶液中橙色的Cr2O72-与黄色的CrO42-存在如下平衡:Cr2O72-+H2O 2CrO42-+2H+,已知重铬酸钾(K2Cr2O7)稀溶液为橙色。取甲、乙两支试管分别加入2mL重铬酸钾稀溶液,进行如下操作:
2CrO42-+2H+,已知重铬酸钾(K2Cr2O7)稀溶液为橙色。取甲、乙两支试管分别加入2mL重铬酸钾稀溶液,进行如下操作:
(1)向甲试管中加入NaOH溶液,上述平衡向方向 移动(填“正反应”或“逆反应”);
(2)向乙试管中加入足量Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),溶液最终显 色。
-
已知重铬酸钾(K2Cr2O7)是一种比高锰酸钾还要强的氧化剂,其溶液中存在如下平衡:
2CrO42—(黄色)+2H +  Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
若要使溶液的橙色加深,下列可采用的方法是
A.加入适量稀盐酸 B.加入适量稀硫酸
C.加入适量烧碱固体 D.加水稀释
-
已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O72-(橙色)+ H2O 2H++ 2CrO42-(黄色)
2H++ 2CrO42-(黄色)
①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。
②向2 mL 0.1 mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+ = 2Cr3+(绿色) + 6Fe3+ + 7H2O。
下列分析正确的是
A. 实验①和②均能证明K2Cr2O7溶液中存在上述平衡
B. 实验②能说明氧化性:Cr2O72-> Fe3+
C. CrO42-和Fe2+在酸性溶液中可以大量共存
D. 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小
-
已知高锰酸钾与重铬酸钾(K2Cr2O7)都是化学中常用的强氧化剂,高锰酸钾溶液呈紫红色而重铬酸钾溶液中存在如下平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O,若要使溶液的橙色加深,下列可采用的方法是( )
Cr2O72-(橙色)+H2O,若要使溶液的橙色加深,下列可采用的方法是( )
A.加入适量小苏打 B.加入适量稀硝酸
C.加入适量烧碱固体 D.加水稀释
-
已知高锰酸钾与重铬酸钾(K2Cr2O7)都是化学中常用的强氧化剂,高锰酸钾溶液呈紫红色而重铬酸钾溶液中存在如下平衡:
2CrO42—(黄色)+2H +  Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
若要使溶液的橙色加深,下列可采用的方法是
A.加入适量稀盐酸 B.加入适量稀硝酸
C.加入适量烧碱固体 D.加水稀释
-
已知高锰酸钾与重铬酸钾(K2Cr2O7)都是化学中常用的强氧化剂,高锰酸钾溶液呈紫红色而重铬酸钾溶液中存在如下平衡:2CrO42-(黄色)+2H+  Cr2O72-(橙色)+H2O;
Cr2O72-(橙色)+H2O;
若要使溶液的橙色加深,下列可采用的方法是
A.加入适量稀硝酸 B.加入适量稀盐酸
C.加入适量烧碱固体 D.加水稀释
2CrO42-+2H+。
N2O4(g)△H=-56.9kJ/mol。
