将4molSO2和2mol O2在2L的恒容密闭容器中混合,并在一定条件下发生如下反应: 2SO2(g)+ O2(g)2SO3(g),若经2s后测得SO3的浓度为0.6mol/L。下列说法中不正确的是
A. 用SO2表示反应的平均速率为0.3mol/( L·s)
B. 用O2表示反应的平均速率为0.15mol/(L.s)
C. 2s时O2的浓度为0.7mol/L
D. 2s时SO2的转化率为70%
高二化学单选题简单题
将4molSO2和2mol O2在2L的恒容密闭容器中混合,并在一定条件下发生如下反应: 2SO2(g)+ O2(g)2SO3(g),若经2s后测得SO3的浓度为0.6mol/L。下列说法中不正确的是
A. 用SO2表示反应的平均速率为0.3mol/( L·s)
B. 用O2表示反应的平均速率为0.15mol/(L.s)
C. 2s时O2的浓度为0.7mol/L
D. 2s时SO2的转化率为70%
高二化学单选题简单题
将4molSO2和2mol O2在2L的恒容密闭容器中混合,并在一定条件下发生如下反应: 2SO2(g)+ O2(g)2SO3(g),若经2s后测得SO3的浓度为0.6mol/L。下列说法中不正确的是
A. 用SO2表示反应的平均速率为0.3mol/( L·s)
B. 用O2表示反应的平均速率为0.15mol/(L.s)
C. 2s时O2的浓度为0.7mol/L
D. 2s时SO2的转化率为70%
高二化学单选题简单题查看答案及解析
(9分)将4molSO2和2molO2的混合气体置于体积可变的恒压容器中,在一定条件下发生如下反应2SO2(g) + O2(g) 2SO3(g) ΔH<0,该反应达平衡时,测得气体总物质的量为4.2mol,试回答:
(1)在该平衡时,n(SO3)=________mol
(2)若起始时加入1.2molSO2 、0.6molO2 和xmolSO3 ,达到平衡时各气体体积分数与上述平衡状态相同,则x的取值范围是________
(3)若反应开始时v(逆)> v(正),达到上述平衡状态时,气体的总物质的量仍为4.2mol,则起始时n(SO3)的取值范围是________
(4)若反应过程中SO2、O2、SO3物质的量变化如图所示。则反应进行至20min时,曲线发生变化的原因是______________________(用文字表达)。10 min到15 min的曲线变化的原因可能是_________(填写编号)。
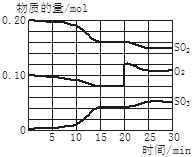
A. 加了催化剂 B. 缩小容器体积
C. 降低温度 D. 增加SO3的物质的量
高二化学填空题简单题查看答案及解析
将4molSO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2(g)+O2(g)2SO3(g) ,测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时SO3的浓度______;
(2)该温度下的平衡常数______;
(3)平衡时SO2的转化率______。
高二化学计算题困难题查看答案及解析
在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g)2SO3(g) △H<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ,则下列分析正确的是
A.在该条件下,反应前后的压强之比为6:5.3
B.若反应开始时容器体积为2L,则v(SO3)=0.35mol/(L·min)
C.若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4mol
D.若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于Q kJ
高二化学选择题中等难度题查看答案及解析
在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ,则下列分析正确的是
A. 在该条件下,反应前后的压强之比为6∶5.3
B. 若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)>1.4mol
C. 若反应开始时容器容积为2L,则v(SO3)=0.35mol·L-1·min-1
D. 若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量小于Q kJ
高二化学单选题困难题查看答案及解析
已知体积为2L的恒容密闭容器中发生反应:2SO2(g) + O2(g)2SO3(g),请根据化学反应的有关原理同答下列问题
(1)一定条件下,充入2mol SO2(g)和2mol O2(g),20s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为_____________________。
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)___________。
①混合气体的密度不变 ②混合气体的平均相对分子质量不变
③ v正(SO2)=2v正(O2) ④各气体的浓度都不再发生变化
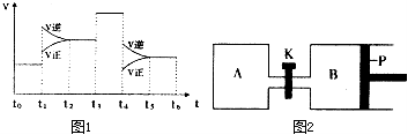
(3)图1表示该反应的速率(v)随时间(t)的变化的关系.则下列不同时间段中,SO3 的百分含量最高的是( )
A、t2→t3 B、t0→t1 C、t5→t6 D、t3→t4
据图分析:你认为t3时改变的外界条件可能是__________;
(4)图2中P是可自由平行滑动的活塞.在相同温度时,向A容器中充入4mol SO3(g),关闭K,向B容器中充入2mol SO3(g),两容器分别发生反应.已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体积
为1.2a L,容器B中SO3转化率为___________。
②若打开K,一段时间后重新达到平衡,容器B的体积为___________L(连通管中气体体积忽略不计,且不考虑温度的影响)。
高二化学填空题困难题查看答案及解析
在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ,则下列分析正确的是( )
A. 在该条件下,反应前后的压强之比为6∶5.3
B. 若反应开始时容器容积为2L,则v(SO3)=0.35mol·L-1·min-1
C. 若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)>1.4mol
D. 若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量小于QkJ
高二化学单选题困难题查看答案及解析
在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ,则下列分析正确的是( )
A. 在该条件下,反应前后的压强之比为6∶5.3
B. 若反应开始时容器容积为2L,则v(SO3)=0.35mol·L-1·min-1
C. 若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)>1.4mol
D. 若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量小于QkJ
高二化学单选题困难题查看答案及解析
在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ,则下列分析正确的是( )
A. 在该条件下,反应前后的压强之比为6∶5.3
B. 若反应开始时容器容积为2L,则0~2min的平均速率v(SO3)=0.35mol·L-1·min-1
C. 若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)>1.4mol
D. 若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量小于Q kJ
高二化学单选题中等难度题查看答案及解析
高二化学解答题中等难度题查看答案及解析