-
碳热还原法广泛用于合金及材料的制备。因答下列问题:
(1)种制备氮氧化铝的反应原理为23Al2O3+15C+5N2=2Al23O27N5+15CO,产物Al23O27N5中氮的化合价为____,该反应中每生成1mol Al23O27N5,转移的电子数为_____________。
(2)真空碳热冶得法包含很多反应,其中的三个反应如下:
Al2O3(s)+3C(s)=Al2OC(s)+2CO(g) ΔH1
2Al2OC(s)+3C(s)=Al4C3(s)+2CO(g) ΔH2
2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) ΔH3
①ΔH3=______(用ΔH1、ΔH2表示)。
②Al4C3可与足量盐酸反应制备种最简单的烃。该反应的化学方程式为_____________。
(3)下列是碳热还原制锰合金的三个反应,CO与CO2平衡分压比的自然对数值(lnK=2.3031gK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数,分压=总压×气体的物质的量分数)。
Ⅰ.Mn3C(s)+4CO2(g) 3MnO(s)+ 5CO(g) Kp(I)
3MnO(s)+ 5CO(g) Kp(I)
Ⅱ.Mn(s)+CO2(g) MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g) 3Mn(s)+2CO(g)Kp(Ⅲ)
3Mn(s)+2CO(g)Kp(Ⅲ)
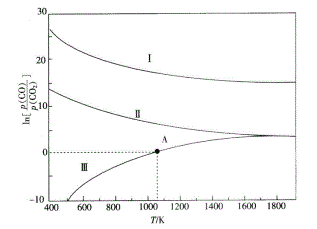
①ΔH>0的反应是______ (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②1200K时,在一体积为2L的恒容密闭容器中有17.7gMn3C(s)和0.4molCO2,只发生反应Ⅰ,5min后达到平衡,此时CO的浓度为0.125mol/L,则0~5min内v(CO2)=_____________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是_____(填标号)。
A.容器的体积不再改变
B.固体的质量不再改变
C.气体的总质量不再改变
③向恒容密闭容器中加入Mn3C并充入0.1molCO,若只发生反应Ⅲ,则在A点反应达到平衡,当容器的总压为akPa时,CO的转化率为______;A点对应温度下的Kp(Ⅲ)=________。
-
碳热还原法广泛用于合金及材料的制备。回答下列问题
(1) 一种制备氮氧化铝的反应原理为23Al2O3+ 15C+5N2=2Al23O27N5+15CO,产物Al23O27N5 中氮的化合价为_____,该反应中每生成 l mol Al23O27N5转移的电子数为_______________ 。
(2) 真空碳热冶铝法包含很多反应.其中的三个反应如下:
Al2O3 (s) +3C(s)=Al2OC(s) +2CO(g) △H1
2Al2OC(s)+3C(s)=Al4C3(s)+2CO(g) △H2
2Al2O3(s) +9C(s)= Al4C3(s)+6CO(g) △H3
①△H3=________ ( 用△H1、△H2表示).
②Al4C3可与足量盐酸反应制备简单的烃。该反应的化学方程式为____________。
(3)下列是碳热还原制锰合金的三个反应 ,CO与CO2平衡分压比的自然对数( ) 与温度的关系如图所示(已知Kp 是用平衡分压代替浓度计算所得的平衡常数,分压=总压 × 气体的物质的量分数)。
) 与温度的关系如图所示(已知Kp 是用平衡分压代替浓度计算所得的平衡常数,分压=总压 × 气体的物质的量分数)。
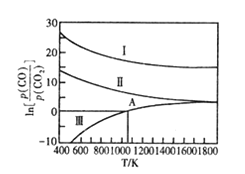
I. Mn3C(s)+4CO2(g)⇌ 3MnO(s)+ 5CO(g) Kp(I)
II. Mn(s) +CO2(g) ⇌MnO(s) +CO(g) Kp (II)
III. Mn3C(s)+CO2(g) ⇌3Mn(s) +2CO(g) Kp(III)
①△H>O的 反应是_________ (填“I ”“II” 或“III”)。
②1200K时在 一体积为 2L 的恒容密闭容器中有17.7gMn3C( s)和0.4molCO2 ,只发生反应I,5min后达到平衡,此时CO的浓度为0.125mol/L,则0~5 min内 v(CO2)=_______。
③在一体积可变的密闭容器中加入一定量的Mn(s )并充入一定量的CO2(g) .只发生反应
II,下列能说明反应II 达到平衡状态的是________ (填标号)。
A. 容器的体积不再改变
B.固体的质量不再改变
C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C并充入0.l molCO2, 若只发生反应III. 则在A点反应达到平衡时,容器的总压为akPa, CO2的转化率为______; A点对应温度下的Kp(III) =______。
-
碳热还原法广泛用于合金及材料的制备。回答下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+15C+5N2=2Al23O27N5+15CO ,产物Al23O27N5中氮的化合价为______,该反应中每生成1 mol Al23O27N5,转移的电子数为________NA。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Ⅰ.Al2O3(s)+3C(s)=Al2OC(s)+2CO(g) ΔH1
Ⅱ.2Al2OC(s)+3C(s)=Al4C3(s)+2CO(g) ΔH2
Ⅲ.2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) ΔH3
①ΔH3=_________(用ΔH1、ΔH2表示)。
②Al4C3可与足量盐酸反应制备一种烃。该反应的化学方程式为________________。
(3)下列是碳热还原法制锰合金的三个反应,CO与CO2平衡分压比的自然对数值与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数)。

Ⅰ.Mn3C(s)+4CO2(g) 3MnO(s)+5CO(g) Kp(Ⅰ)
3MnO(s)+5CO(g) Kp(Ⅰ)
Ⅱ.Mn(s)+CO2(g) MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g) 3Mn(s)+2CO(g) Kp(Ⅲ)
3Mn(s)+2CO(g) Kp(Ⅲ)
①ΔH>0的反应是____(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②1 200 K时,在一体积为2 L的恒容密闭容器中有17.7 g Mn3C(s)和0.4 mol CO2,只发生反应Ⅰ,5 min 后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min内v(CO2)=_________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是____(填字母)。
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
-
碳热还原法广泛用于合金及材料的制备。回答下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+ 15C+5N2==2Al23O27N5+15CO,产物Al23O27N5中氮的化合价为______________________________。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Al2O3 (s)+ 3C(s)==Al2OC(s)+2CO(g) △H1
2Al2OC(s) + 3C(s)==Al4C3(s) + 2CO(g) △H2
2Al2O3 (s)+ 9C(s)== Al4C3 (s) + 6CO(g) △H3
①△H3=_________ (用△H1、△H2 表示)。
②Al4C3可与足量盐酸反应制备一种最简单的烃,该反应的化学方程式为__________________________。(3)下列是碳热还原制锰合金的三个反应,CO 与CO2 平衡分压比的自然对数值(1nK=2.303lgK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数。分压=总压× 气体的物质的量分数)。
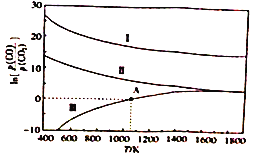
I.Mn3C(s)+4CO2(g)  3MnO(s)+5CO(g) Kp(I)
3MnO(s)+5CO(g) Kp(I)
II.Mn(s)+CO2(g)  MnO(s)+CO(g) Kp(II)
MnO(s)+CO(g) Kp(II)
III.Mn3C(s) + CO2(g)  3Mn(s)+2CO(g) Kp(III)
3Mn(s)+2CO(g) Kp(III)
①△H>0 的反应是__________________ (填“I”“II”或“I”)。
②1200 K时,在一体积为2L的恒容密闭容器中有17.7 gMn3C(s)和0.4molCO2,只发生反应I,5min后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min 内V(CO2)=____________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应II,下列能说明反应II达到平衡的是____________ (填字母 )。
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C 并充入0.1molCO2,若只发生反应III,则在A点反应达到平衡。当容器的总压为a kPa时,CO2的转化率为______________;A点对应温度下的Kp(III)=____________。
-
碳热还原法广泛用于合金及材料的制备。回下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+15C+5N2=2Al23O27N5+15CO ,产物Al23O27N5中氮的化合价为______,该反应中每生成1 mol Al23O27N5,转移的电子数为________NA。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Al2O3(s)+3C(s) =Al2OC(s)+2CO(g) ΔH1
2Al2OC(s)+3C(s) =Al4C3(s)+2CO(g) ΔH2
2Al2O3(s)+9C(s)= Al4C3(s)+6CO(g) ΔH3
①ΔH3=_________(用ΔH1、ΔH2表示)。
②Al4C3可与足量盐酸反应制备一种烃。该反应的化学方程式为____________。
(3)下列是碳热还原法制锰合金的三个反应,CO与CO2平衡分压比的自然对数值与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数)。
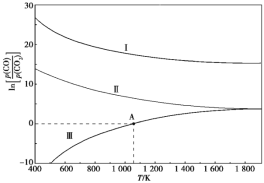
Ⅰ.Mn3C(s)+4CO2(g) 3MnO(s)+5CO(g) Kp(Ⅰ)
3MnO(s)+5CO(g) Kp(Ⅰ)
Ⅱ.Mn(s)+CO2(g) MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g) 3Mn(s)+2CO(g) Kp(Ⅲ)
3Mn(s)+2CO(g) Kp(Ⅲ)
①ΔH>0的反应是____(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②1200 K时,在一体积为2 L的恒容密闭容器中有17.7 g Mn3C(s)和0.4 mol CO2,只发生反应Ⅰ,5 min后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min内v(CO2)=_________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是____(填字母)。
A.容器的体积不再改变
B.固体的质量不再改变
C.气体的总质量不再改变
-
化学知识在生产和生活中有着重要的应用。下列说法中正确的是
A.依据铝热反应原理,能发生反应2Al+3MgO 3Mg+Al2O3
3Mg+Al2O3
B.铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝
C.硫酸铁和明矾都可用于净水
D.Na2CO3可以与胃酸反应,可用Na2CO3治疗胃酸过多
-
化学知识在生产和生活中有着重要的应用。下列说法中正确的是
A.依据铝热反应原理,能发生反应2Al+3MgO 3Mg+Al2O3
3Mg+Al2O3
B.铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝
C.硫酸铁和明矾都可用于净水
D.Na2CO3可以与胃酸反应,可用Na2CO3治疗胃酸过多
-
氮化铝是一种新型的无机非金属材料,被广泛应用于集成电路生产领域.其制备反应原理为:Al2O3+N2+3C═2AlN+3CO.制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质.为测定产品中AlN的质量分数,某同学按如图1装置进行相关实验.可选用的化学试剂为:mg氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精.回答下列问题:
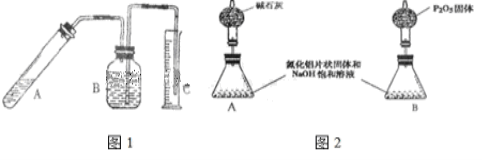
(1)组装完实验装置,使用前第一步应该
(2)图1(B)中试剂最好选用 (填序号):
①煤油 ② 医用酒精 ③水
医用酒精 ③水
已知A 中有NaAlO2生成,并放出有刺激性气味气体,写出A中发生反应的离子方程式 .
(3)读取C(量筒)中液体体积时,应注意下列问题,错误的是 (填序号)
a.C中液面不再上升时立即读数
b.上下移动C,使之液面与B中液面相平
c.A中不再有气泡逸出
d.视线与凹液面最低处相平
(4)mg氮化铝与足量NaOH饱和溶液反应,实验结束后,C中收集到液体的体积为VL(已折算成标准状况),则AlN样品的纯度为 (写计算表达式).
(5)上述实验方案,可能因气体体积测量不准,导致误差较大.有人建议改用下列A、B两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测写,用差量法就可比较准确确定样品中AlN的质量分数.较合理的装置是: (填代号).
-
氮化铝是一种新型的无机非金属材料,被广泛应用于集成电路生产领域。其 制备反应原理为Al2O3+N2+3C
制备反应原理为Al2O3+N2+3C 2AlN+3CO。制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同学按下图装置进行相关实验。可选用的化学试剂:m g氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
2AlN+3CO。制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同学按下图装置进行相关实验。可选用的化学试剂:m g氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
回答下列问题:
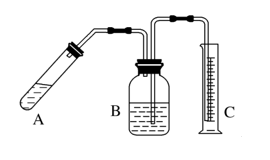
(1)简 述检查该套装置气密性的方法:____________________________________。
述检查该套装置气密性的方法:____________________________________。
(2)上图B中试剂最好选用:__________(填序号)。
①水 ②煤油 ③医用酒精
已知A 中有NaAlO2生成,并放出有刺激性气味的气体,写出A中发生反应的化学方程式:______________________________________________________。
(3)读取C(量筒)中液体体积时,应注意__________(填字母)。
a.C中液面不再上升时立即读数
b.上下移动C,使之液面与B中液面相平
c.A中不再有气泡逸出
d.视线与凹液面最低处相平
(4)m g氮化铝与足量NaOH饱和溶液反应,实验结束后,C中收集到液体的体积为V L(已折算成标准状况),则AlN样品的纯度为__________(写计算表达式)。
(5)上述实验方案,可能因气体体积测量不准,导致误差较大。有人建议改用下列A、B两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测量,用差量法就可比较准确确定样品中AlN的质量分数。较合理的装置是_________(填字母)。

-
氮化铝(AlN)是一种新型的无机非金属材料,工业上制备原理如下:Al2O3+N2+3C 2AlN+3CO,反应中氧化产物与还原产物的物质的量之比为___________;AlN产品中常含有碳等不与NaOH溶液反应的杂质。为了分析某A1N样品中A1N的含量。某实验小组设计了如下三种实验方案。知:A1N+NaOH+H2O=NaAlO2+NH3↑
2AlN+3CO,反应中氧化产物与还原产物的物质的量之比为___________;AlN产品中常含有碳等不与NaOH溶液反应的杂质。为了分析某A1N样品中A1N的含量。某实验小组设计了如下三种实验方案。知:A1N+NaOH+H2O=NaAlO2+NH3↑
【方案1】有人想用下列A、B两个装置中的一种(在通风橱内进行)。只需进行简单而又必要的数据测定,用差量法就可测定样品中A1N的质量分数,较合理的装置是:___________(填代号)。
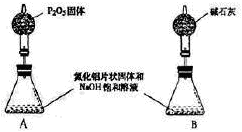
【方案2】取一定量(m1)的样品,用以下装置测定样品中A1N的纯度(夹持装置己略去)。
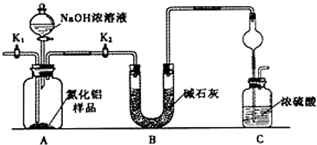
(1)上图C装置中球形干燥管的作用是___________;
(2)完成以下实验步骤:组装好实验装置,首先检查装置气密性:再加入实验药品,接下来关闭K1打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间。
请回答:I、需测定___________(填A、B、C)装置反应前后的质量变化。Ⅱ、通入氮气的目的是____________。
【方案3】按以下步骤测定样品中A1N的含量:

(1)步骤②生成沉淀的离子方程式为___________;
(2)步骤③的操作是___________,A1N的纯度是___________(用m1、m2、m3表示)。

3MnO(s)+5CO(g) Kp(Ⅰ)
MnO(s)+CO(g) Kp(Ⅱ)
3Mn(s)+2CO(g) Kp(Ⅲ)









