-
碳热还原法广泛用于合金及材料的制备。回答下列问题
(1) 一种制备氮氧化铝的反应原理为23Al2O3+ 15C+5N2=2Al23O27N5+15CO,产物Al23O27N5 中氮的化合价为_____,该反应中每生成 l mol Al23O27N5转移的电子数为_______________ 。
(2) 真空碳热冶铝法包含很多反应.其中的三个反应如下:
Al2O3 (s) +3C(s)=Al2OC(s) +2CO(g) △H1
2Al2OC(s)+3C(s)=Al4C3(s)+2CO(g) △H2
2Al2O3(s) +9C(s)= Al4C3(s)+6CO(g) △H3
①△H3=________ ( 用△H1、△H2表示).
②Al4C3可与足量盐酸反应制备简单的烃。该反应的化学方程式为____________。
(3)下列是碳热还原制锰合金的三个反应 ,CO与CO2平衡分压比的自然对数( ) 与温度的关系如图所示(已知Kp 是用平衡分压代替浓度计算所得的平衡常数,分压=总压 × 气体的物质的量分数)。
) 与温度的关系如图所示(已知Kp 是用平衡分压代替浓度计算所得的平衡常数,分压=总压 × 气体的物质的量分数)。
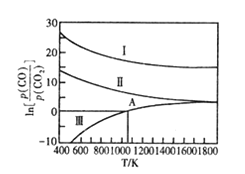
I. Mn3C(s)+4CO2(g)⇌ 3MnO(s)+ 5CO(g) Kp(I)
II. Mn(s) +CO2(g) ⇌MnO(s) +CO(g) Kp (II)
III. Mn3C(s)+CO2(g) ⇌3Mn(s) +2CO(g) Kp(III)
①△H>O的 反应是_________ (填“I ”“II” 或“III”)。
②1200K时在 一体积为 2L 的恒容密闭容器中有17.7gMn3C( s)和0.4molCO2 ,只发生反应I,5min后达到平衡,此时CO的浓度为0.125mol/L,则0~5 min内 v(CO2)=_______。
③在一体积可变的密闭容器中加入一定量的Mn(s )并充入一定量的CO2(g) .只发生反应
II,下列能说明反应II 达到平衡状态的是________ (填标号)。
A. 容器的体积不再改变
B.固体的质量不再改变
C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C并充入0.l molCO2, 若只发生反应III. 则在A点反应达到平衡时,容器的总压为akPa, CO2的转化率为______; A点对应温度下的Kp(III) =______。
-
碳热还原法广泛用于合金及材料的制备。回答下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+15C+5N2=2Al23O27N5+15CO ,产物Al23O27N5中氮的化合价为______,该反应中每生成1 mol Al23O27N5,转移的电子数为________NA。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Ⅰ.Al2O3(s)+3C(s)=Al2OC(s)+2CO(g) ΔH1
Ⅱ.2Al2OC(s)+3C(s)=Al4C3(s)+2CO(g) ΔH2
Ⅲ.2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) ΔH3
①ΔH3=_________(用ΔH1、ΔH2表示)。
②Al4C3可与足量盐酸反应制备一种烃。该反应的化学方程式为________________。
(3)下列是碳热还原法制锰合金的三个反应,CO与CO2平衡分压比的自然对数值与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数)。

Ⅰ.Mn3C(s)+4CO2(g) 3MnO(s)+5CO(g) Kp(Ⅰ)
3MnO(s)+5CO(g) Kp(Ⅰ)
Ⅱ.Mn(s)+CO2(g) MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g) 3Mn(s)+2CO(g) Kp(Ⅲ)
3Mn(s)+2CO(g) Kp(Ⅲ)
①ΔH>0的反应是____(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②1 200 K时,在一体积为2 L的恒容密闭容器中有17.7 g Mn3C(s)和0.4 mol CO2,只发生反应Ⅰ,5 min 后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min内v(CO2)=_________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是____(填字母)。
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
-
碳热还原法广泛用于合金及材料的制备。回答下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+ 15C+5N2==2Al23O27N5+15CO,产物Al23O27N5中氮的化合价为______________________________。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Al2O3 (s)+ 3C(s)==Al2OC(s)+2CO(g) △H1
2Al2OC(s) + 3C(s)==Al4C3(s) + 2CO(g) △H2
2Al2O3 (s)+ 9C(s)== Al4C3 (s) + 6CO(g) △H3
①△H3=_________ (用△H1、△H2 表示)。
②Al4C3可与足量盐酸反应制备一种最简单的烃,该反应的化学方程式为__________________________。(3)下列是碳热还原制锰合金的三个反应,CO 与CO2 平衡分压比的自然对数值(1nK=2.303lgK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数。分压=总压× 气体的物质的量分数)。
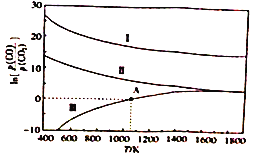
I.Mn3C(s)+4CO2(g)  3MnO(s)+5CO(g) Kp(I)
3MnO(s)+5CO(g) Kp(I)
II.Mn(s)+CO2(g)  MnO(s)+CO(g) Kp(II)
MnO(s)+CO(g) Kp(II)
III.Mn3C(s) + CO2(g)  3Mn(s)+2CO(g) Kp(III)
3Mn(s)+2CO(g) Kp(III)
①△H>0 的反应是__________________ (填“I”“II”或“I”)。
②1200 K时,在一体积为2L的恒容密闭容器中有17.7 gMn3C(s)和0.4molCO2,只发生反应I,5min后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min 内V(CO2)=____________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应II,下列能说明反应II达到平衡的是____________ (填字母 )。
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C 并充入0.1molCO2,若只发生反应III,则在A点反应达到平衡。当容器的总压为a kPa时,CO2的转化率为______________;A点对应温度下的Kp(III)=____________。
-
碳热还原法广泛用于合金及材料的制备。因答下列问题:
(1)种制备氮氧化铝的反应原理为23Al2O3+15C+5N2=2Al23O27N5+15CO,产物Al23O27N5中氮的化合价为____,该反应中每生成1mol Al23O27N5,转移的电子数为_____________。
(2)真空碳热冶得法包含很多反应,其中的三个反应如下:
Al2O3(s)+3C(s)=Al2OC(s)+2CO(g) ΔH1
2Al2OC(s)+3C(s)=Al4C3(s)+2CO(g) ΔH2
2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) ΔH3
①ΔH3=______(用ΔH1、ΔH2表示)。
②Al4C3可与足量盐酸反应制备种最简单的烃。该反应的化学方程式为_____________。
(3)下列是碳热还原制锰合金的三个反应,CO与CO2平衡分压比的自然对数值(lnK=2.3031gK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数,分压=总压×气体的物质的量分数)。
Ⅰ.Mn3C(s)+4CO2(g) 3MnO(s)+ 5CO(g) Kp(I)
3MnO(s)+ 5CO(g) Kp(I)
Ⅱ.Mn(s)+CO2(g) MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g) 3Mn(s)+2CO(g)Kp(Ⅲ)
3Mn(s)+2CO(g)Kp(Ⅲ)
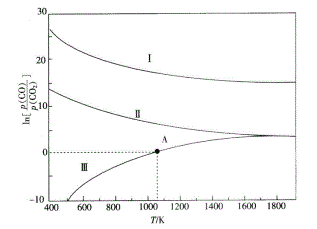
①ΔH>0的反应是______ (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②1200K时,在一体积为2L的恒容密闭容器中有17.7gMn3C(s)和0.4molCO2,只发生反应Ⅰ,5min后达到平衡,此时CO的浓度为0.125mol/L,则0~5min内v(CO2)=_____________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是_____(填标号)。
A.容器的体积不再改变
B.固体的质量不再改变
C.气体的总质量不再改变
③向恒容密闭容器中加入Mn3C并充入0.1molCO,若只发生反应Ⅲ,则在A点反应达到平衡,当容器的总压为akPa时,CO的转化率为______;A点对应温度下的Kp(Ⅲ)=________。
-
碳热还原法广泛用于合金及材料的制备。回下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+15C+5N2=2Al23O27N5+15CO ,产物Al23O27N5中氮的化合价为______,该反应中每生成1 mol Al23O27N5,转移的电子数为________NA。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Al2O3(s)+3C(s) =Al2OC(s)+2CO(g) ΔH1
2Al2OC(s)+3C(s) =Al4C3(s)+2CO(g) ΔH2
2Al2O3(s)+9C(s)= Al4C3(s)+6CO(g) ΔH3
①ΔH3=_________(用ΔH1、ΔH2表示)。
②Al4C3可与足量盐酸反应制备一种烃。该反应的化学方程式为____________。
(3)下列是碳热还原法制锰合金的三个反应,CO与CO2平衡分压比的自然对数值与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数)。
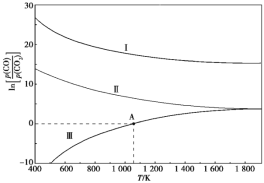
Ⅰ.Mn3C(s)+4CO2(g) 3MnO(s)+5CO(g) Kp(Ⅰ)
3MnO(s)+5CO(g) Kp(Ⅰ)
Ⅱ.Mn(s)+CO2(g) MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g) 3Mn(s)+2CO(g) Kp(Ⅲ)
3Mn(s)+2CO(g) Kp(Ⅲ)
①ΔH>0的反应是____(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②1200 K时,在一体积为2 L的恒容密闭容器中有17.7 g Mn3C(s)和0.4 mol CO2,只发生反应Ⅰ,5 min后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min内v(CO2)=_________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是____(填字母)。
A.容器的体积不再改变
B.固体的质量不再改变
C.气体的总质量不再改变
-
氮化铝是一种新型的无机非金属材料,被广泛应用于集成电路生产领域.其制备反应原理为:Al2O3+N2+3C═2AlN+3CO.制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质.为测定产品中AlN的质量分数,某同学按如图1装置进行相关实验.可选用的化学试剂为:mg氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精.回答下列问题:
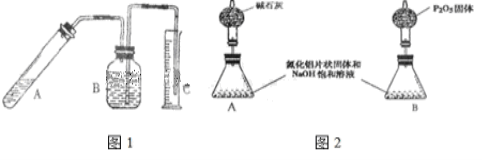
(1)组装完实验装置,使用前第一步应该
(2)图1(B)中试剂最好选用 (填序号):
①煤油 ② 医用酒精 ③水
医用酒精 ③水
已知A 中有NaAlO2生成,并放出有刺激性气味气体,写出A中发生反应的离子方程式 .
(3)读取C(量筒)中液体体积时,应注意下列问题,错误的是 (填序号)
a.C中液面不再上升时立即读数
b.上下移动C,使之液面与B中液面相平
c.A中不再有气泡逸出
d.视线与凹液面最低处相平
(4)mg氮化铝与足量NaOH饱和溶液反应,实验结束后,C中收集到液体的体积为VL(已折算成标准状况),则AlN样品的纯度为 (写计算表达式).
(5)上述实验方案,可能因气体体积测量不准,导致误差较大.有人建议改用下列A、B两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测写,用差量法就可比较准确确定样品中AlN的质量分数.较合理的装置是: (填代号).
-
氮化铝是一种新型的无机非金属材料,被广泛应用于集成电路生产领域。其 制备反应原理为Al2O3+N2+3C
制备反应原理为Al2O3+N2+3C 2AlN+3CO。制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同学按下图装置进行相关实验。可选用的化学试剂:m g氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
2AlN+3CO。制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同学按下图装置进行相关实验。可选用的化学试剂:m g氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
回答下列问题:
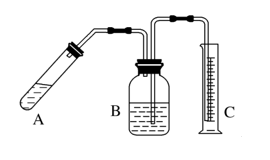
(1)简 述检查该套装置气密性的方法:____________________________________。
述检查该套装置气密性的方法:____________________________________。
(2)上图B中试剂最好选用:__________(填序号)。
①水 ②煤油 ③医用酒精
已知A 中有NaAlO2生成,并放出有刺激性气味的气体,写出A中发生反应的化学方程式:______________________________________________________。
(3)读取C(量筒)中液体体积时,应注意__________(填字母)。
a.C中液面不再上升时立即读数
b.上下移动C,使之液面与B中液面相平
c.A中不再有气泡逸出
d.视线与凹液面最低处相平
(4)m g氮化铝与足量NaOH饱和溶液反应,实验结束后,C中收集到液体的体积为V L(已折算成标准状况),则AlN样品的纯度为__________(写计算表达式)。
(5)上述实验方案,可能因气体体积测量不准,导致误差较大。有人建议改用下列A、B两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测量,用差量法就可比较准确确定样品中AlN的质量分数。较合理的装置是_________(填字母)。

-
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
真空碳热还原-氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)
ΔH=a kJ·mol-1
3AlCl(g)=2Al(l)+AlCl3(g)ΔH=b kJ·mol-1
(1)反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的ΔH=________kJ·mol-1(用含a、b的代数式表示)。
(2)Al4C3是反应过程中的中间产物。Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为______________________________________。
-
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛.
(1)真空碳热还原-氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al2O3(s)+AlC13(g)+3C(s)=3AlCl(g)+3CO(g)△H=a kJ•mol-1
3AlCl(g)=2Al(l)+AlC13(g)△H=b kJ•mol-1
①反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=________kJ•mol-1(用含a、b 的代数式表示).
②Al4C3是反应过程中的中间产物.Al4C3 与盐酸反应(产物之一是含氢量最高的烃) 的化学方程式为________.
(2)镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得.该合金在一定条件下完全吸氢的反应方程式为Mg17Al122+17H2=17MgH2+12Al.得到的混合物Y(17MgH2+12Al)在一定条件下可释放出氢气.
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是________.
②在6.0mol•L-1HCl 溶液中,混合物Y 能完全释放出H2.1mol Mg17 Al12 完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2 的物质的量为________.
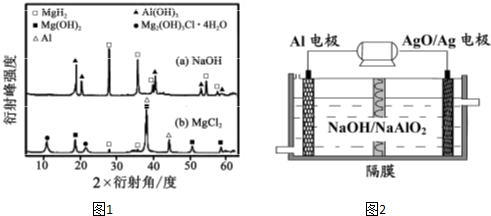
③在0.5mol•L-1NaOH 和1.0mol•L-1 MgCl2溶液中,混合物Y 均只能部分放出氢气,反应后残留固体物质的X-射线衍射谱图如图1所示(X-射线衍射可用于判断某晶态物
质是否存在,不同晶态物质出现衍射峰的衍射角不同).在上述NaOH 溶液中,混合物Y 中产生氢气的主要物质是________
________(填化学式).
(3)铝电池性能优越,Al-AgO 电池可用作水下动力电源,其原理如图2所示.该电池反应的化学方程式为________.
-
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原-氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下Al2O3(s)+AlCl3(g)+3C(s) =3AlCl (g)+3CO(g) △H = a kJ·mol-1
3AlCl(g)=2Al(l)+ AlCl3 (g) △H = b kJ·mol-1
①反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=________kJ·mol-1(用含a、b的代数式表示)。
②Al4C3也是该反应过程中的一种中间产物。Al4C3 与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为_______________。
③甲烷和水反应可以制水煤气(混合气体),在恒温、固定体积为V升的密闭容器中的反应微观示意图如下所示,根据微观示意图得出的结论中,正确的是_____________。
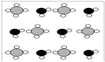
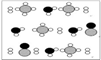
一定条件下经过t分钟达到化学平衡
a. 该反应方程式为:CH4+H2O = CO+3H2
b. 该反应平衡前后压强比为3:4
c. 该反应体系中含氢元素的化合物有3种
d. 该反应中甲烷的平衡转化率为50%
④水煤气中的H2可用于生产NH3,在进入合成塔前常用[Cu(NH3)2]Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
[Cu(NH3)2]Ac(aq) + CO(g) + NH3(g)  [Cu(NH3)3]Ac·CO(aq) △H<0
[Cu(NH3)3]Ac·CO(aq) △H<0
[Cu(NH3)2]Ac溶液吸收CO的适宜生产条件应是____________________。该条件下用气体表示的平衡常数表达式为:K=______________
(2)镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,一般在氩气环境中将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得。该合金在一定条件下可完全吸氢得到的混合物Y(含MgH2 和Al),Y在一定条件下可释放出氢气。
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是_________________。
②写出镁铝合金(Mg17Al12 ) 在一定条件下完全吸氢的化学方程式 _________________。
③在6. 0 mol·L-1 HCl 溶液中,混合物Y 能完全释放出H2。1 mol Mg17 Al12 完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2 的物质的量为_________。
) 与温度的关系如图所示(已知Kp 是用平衡分压代替浓度计算所得的平衡常数,分压=总压 × 气体的物质的量分数)。










