-
铜元素在化合物中其化合价可以呈现 、
、 价。
价。 和
和 是常见的
是常见的 价铜的化合物,
价铜的化合物, 是较为常见的
是较为常见的 价铜的化合物。
价铜的化合物。
(1)铜元素位于周期表的_______区。
A、s B、p C、d D、ds E、f
(2)向 溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式__________________。比较
溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式__________________。比较 和
和 中
中 键角的大小:
键角的大小: ___________
___________ 填“
填“ ”或“
”或“ ”
” 。
。
(3) 中阴离子的空间构型为_______,NO3-中的大π键应表示为______
中阴离子的空间构型为_______,NO3-中的大π键应表示为______
[信息:臭氧分子中,中心氧原子的未杂化的p轨道(含2个电子)与其它两个氧原子的p轨道(各含1个电子)肩并肩形成一个大π键,表示为 ,]
,]
 的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
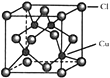
①每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为________________。
②若以铜原子为顶点构成晶胞,面心原子为________(Cu、Cl)
-
铜元素在化合物中其化合价可以呈现 、
、 价。
价。 和
和 是常见的
是常见的 价铜的化合物,
价铜的化合物, 是较为常见的
是较为常见的 价铜的化合物。
价铜的化合物。
(1)铜元素位于周期表的_______区。属于________族。
(2)请写出 的电子排布式__________________,S的价层电子排布图______________
的电子排布式__________________,S的价层电子排布图______________
(3)向 溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式__________________。比较
溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式__________________。比较 和
和 中
中 中键角的大小:
中键角的大小: ___________
___________ (填“
(填“ ” “
” “ ” 或“=”)。
” 或“=”)。
(4) 中阴离子的空间构型为_______
中阴离子的空间构型为_______
(5) 的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
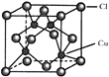
①每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为________________。
②若以铜原子为顶点构成晶胞,面心原子为________(Cu、Cl)
-
铜元素位于元素周期表中第ⅠB族,在化合物中其化合价可以呈现+1、+2 价。铜的单质及其化合物在很多领域有重要的应用。
Ⅰ.CuSO4 和Cu(NO3)2是常见的+2价铜的化合物,有较为广泛的应用。
(1)向CuSO4溶液中滴加氨水,最后可以得到深蓝色的[Cu(NH3)4]SO4溶液。
N、O、S 三种元素的第一电离能由大到小的顺序为______________________________。
(2)制备Cu(NO3)2的一种方法是在N2O4的乙酸乙酯溶液中加入铜,反应一段时间后,加热即可得到Cu(NO3)2。NO3- 的立体构型的名称为_______________,N 原子的杂化方式为________________。NO3- 的一种等电子体为________________________。
Ⅱ.CuCl 是较为常见的十1价铜的化合物。
(3)基态Cu+ 的价层电子排布式为________________________。
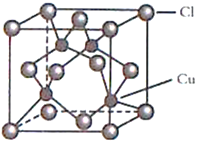
(4)CuCl 的晶胞结构如图所示,C1原子位于立方体的顶点和面心, Cu 原子位于Cl 原子构成的四面体体心。每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为________________。
 。
。
-
下列关于铁的描述中,不正确的是 ( )
A、在FeSO4中滴入KSCN溶液,溶液显红色
B、铁位于元素周期表中第4周期Ⅷ族
C、在化合物中,铁元素常呈现为+2、+3价
D、通常情况下,铁丝在氯气里燃烧时生成FeCl3
-
(15分)元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大。其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g·L—1,C元素原子的最外层电子数是其内层电子数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):

其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、
丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应。请回答下列问题:
(1)写出化合物甲的电子式:________________。
(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式________;
写出均含有F元素的乙与丁在溶液中发生反应的离子方程式 ________________。
(3)由A、C元素组成化合物的戊和A、E元素组成的化合物己,式量均为34。其中戊的熔沸点高于己,其原因是:________。
(4)复盐是指由2种或2种以上阳离子和一种酸根离子组成的盐。请写出由A、B、C、E、F元素组成的一种具有还原性的复盐庚的化学式________。该复盐是一种重要的化学试剂,据中学课本介绍,工业上常用如下方法制取:将一定量的两种盐配成混合溶液,再加热浓缩混合溶液,冷却至室温则析出带有6个结晶水的该复盐晶体。写出相关反应的化学方程式________,析出该复盐晶体的原理是________ ________ 。
-
下列有关元素周期表中的某些推断正确的是
A 位于同一主族的元素的价电子数相同,则各元素的常见化合价也一定相同
B 碱金属族元素同卤族元素一样,其单质的熔沸点随元素原子序数的增大而逐渐升高
C 若x是ⅡB族中元素的原子序数, 那么原子序数为x+1的元素是ⅢA族
D 在周期表中金属和非金属元素的分界线附近的元素是过渡元素
-
X、Y、Z是原子序数依次增大且属于不同周期的三种常见短周期元素,三种元素相互之间可以形成1:1型的化合物M、N、R,常温下M、N为固体,R为液体.M、N遇到水都能产生气体,而且产生的气体相互可以化合,下列说法正确的是( )
A. 三种元素都是非金属元素
B. M、N投入水中所得溶液中溶质相同
C. 三种化合物都是共价化合物
D. Z是地壳中含量最多的元素
-
X、Y、Z是原子序数依次增大且属于不同周期的三种常见短周期元素,三种元素相互之间可以形成1:1型的化合物M、N、R,常温下M、N为固体,R为液体.M、N遇到水都能产生气体,而且产生的气体相互可以化合,下列说法正确的是 ( )
A.三种元素都是非金属元素
B.M、N投入水中所得溶液中溶质相同
C.三种化合物都是共价化合物
D.Z是地壳中含量最多的元素
-
X、Y、Z、W均为短周期主族元素,它们在周期表中相对位置如图所示。Z和Y两元素可以形成常见ZY3型化合物,下列说法正确的是
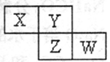
A. X的常见氢化物比Y的常见氢化物稳定
B. X、Z、W的氧化物对应水化物都是常见的强酸
C. W单质不能从盐溶液中置换出Z单质
D. X、Z均可与Y形成原子个数比为1:2的共价化合物
-
A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是_________,基态D原子价电子的轨道表达式为____________。
(2)DA2分子的VSEPR模型是____________。H2A比H2D熔沸点高得多的原因是____________。
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6 在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
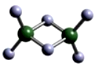
① C2Cl6属于____________晶体(填晶体类型),其中C原子的杂化轨道类型为____________杂化。
② [C(OH)4]-中存在的化学键有___________。
(4)工业上制备B的单质是电解熔融B的氯化物,而不是电解BA,原因是_____________。
(5)B、C的氟化物晶格能分别是2957 kJ·mol-1、5492 kJ·mol-1,二者相差很大的原因是____________。
(6)D与E所形成化合物晶体的晶胞如图所示。
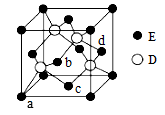
① 在该晶胞中,E的配位数为______________。
② 已知该晶胞的密度为ρ g/cm3,则其中两个D原子之间的距离为_________ pm(列出计算式即可)。
、
价。
和
是常见的
价铜的化合物,
是较为常见的
价铜的化合物。
溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式__________________。比较
和
中
键角的大小:
___________
填“
”或“
”
。
中阴离子的空间构型为_______,NO3-中的大π键应表示为______
,]
的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。


 。
。

