-
胆矾(CuSO4·5H2O)是铜的重要化合物,在工业生产中应用广泛。实验室制备胆矾的流程如下:

(1) 稀硫酸、稀硝酸与铜粉反应生成一种无色气体,该气体是_____(写化学式),制得的胆矾晶体中可能存在的杂质是_____(写名称)。
(2) 实验室可采用沉淀法测定所得胆矾晶体中CuSO4·5H2O的含量,步骤如下:
①取样、称量;②加水充分溶解;③加入BaCl2溶液;④过滤、洗涤、干燥;⑤称量、计算。在过滤前,需要检验SO42-是否沉淀完全,检验方法是____________________________________________
(3) 若改变反应条件可获得化学式为Cux(OH)y(SO4)z·nH2O的晶体,用热重分析仪对Cux(OH)y(SO4)z·nH2O晶体进行分析并推断该晶体的化学式。取3.30 g晶体样品进行热重分析,所得固体质量的变化曲线如下图所示。已知:体系温度在650 ℃及以下时,放出的气体只有水蒸气;实验测得温度在650 ℃时,残留固体的组成可视为aCuO·bCuSO4;温度在1 000 ℃以上时,得到的固体为Cu2O。
请回答下列问题:
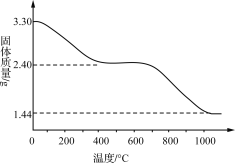
①温度650~1 000 ℃产生的气体中,n(O)∶n(S)____(填“>”“<”或“=”)3。
②通过计算推断Cux(OH)y(SO4)z·nH2O晶体的化学式:__________。
-
胆矾(CuSO4·5H2O)是铜的重要化合物,有着广泛的应用,如用来配制农药波尔多液。以下是CuSO4·5H2O的实验室制备流程图。
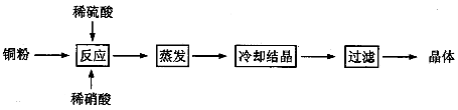
根据题意完成下列填空:
(1)向含有铜粉的稀硫酸中滴加硝酸,在铜粉溶解时最终可以观察到的实验现象: 、 。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是 (填化学式)。
(3)将CuSO4·5H2O与NaHCO3按一定的比例共同投入到150mL沸水中,剧烈搅拌,冷却后,有绿色晶体析出。该晶体的化学组成为Cux (OH) y (CO3) z·nH2O。实验所得的绿色晶体需充分洗涤,检验是否洗涤干净的方法是 。
(4)为了确定晶体的化学式,某实验小组进行如下实验:a.称取3.640g晶体,加入足量的稀盐酸使固体完全溶解,收集到标准状况下的气体448.0 mL;b.称取等质量的晶体,灼烧至完全分解,得到2.400g残余固体。通过计算确定晶体的化学式(写出计算过程)。
-
胆矾(CuSO4·5H2O)是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。

完成下列各题:
Ⅰ.(1)向含铜粉的稀硫酸中滴加浓硝酸,随着铜粉的溶解可能观察到的实验现象 、 。
(2)制得的胆矾晶体(CuSO4·5H2O)中可能存在的杂质是 (写化学式)。
(3)采用重量法测定CuSO4·5H2O的含量时,步骤如下:
①取样,称量 ②加水溶解 ③加氯化钡溶液生成沉淀 ④过滤(其余步骤省略)
在过滤前,需要检验是否沉淀完全,其操作是 。
Ⅱ. 某研究性学习小组用ZRY-1型热重分析仪对12.5克硫酸铜晶体(CuSO4·5H2O)进行热重分析,随温度的升高,硫酸铜晶体依次发生下列反应。
a.CuSO4·5H2O CuSO4+5H2O
CuSO4+5H2O
b.CuSO4 CuO+SO3↑,2SO3
CuO+SO3↑,2SO3 2SO2+O2
2SO2+O2
c.4CuO 2Cu 2 O+O2↑
2Cu 2 O+O2↑
请回答下列问题:
(1)实验过程中热重分析仪测得残留固体质量为3.8 g,试推断该固体的组分是 (写化学式),其对应的物质的量之比是 。
(2)热重分析仪加热晶体至恒重后,将全部气体导出,通入氢氧化钡溶液充分反应,所得沉淀经过滤、洗涤、干燥,质量为 g。
-
(16分)波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料。已知CuSO4·5H2O的部分结构可表示如下:

(1)写出铜原子价电子层的电子排布式____________,与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有__________(填元素符号)。
(2)请在上图中把CuSO4·5H2O结构中的化学键用短线“——”表示出来。
(3)往浓CuSO4溶液中加入过量较浓的NH3·H2O直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液。小心加入约和溶液等体积的C2H5OH并使之分成两层,静置。经过一段时间后可观察到在两层“交界处”下部析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是______________________________________________。
(4)Cu(NH3)4SO4·H2O晶体中呈正四面体的原子团是______________,杂化轨道类型是sp3的原子是____________________________。
(5)如将深蓝色溶液加热,可能得到什么结果?________________________________。
(6)把CoCl2溶解于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]2+。此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示。把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1 mol CoCl3·5NH3只生成2 mol AgCl。请写出表示此配合物结构的化学式(钴的配位数为6)___________,此配合物中的Co化合价为__ ____。
-
(8分)波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料。已知CuSO4·5H2O的部分结构可表示如下:

(1)与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有__________(填元素符号)。
(2)请在上图中把CuSO4·5H2O结构中的化学键用短线“——”表示出来。
(3)往浓CuSO4溶液中加入过量较浓的NH3·H2O直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液。小心加入约和溶液等体积的C2H5OH并使之分成两层,静置。经过一段时间后可观察到在两层“交界处”下部析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是______________________________________。
(4)如将深蓝色溶液加热,可能得到什么结果?________________________________。
-
铁及其化合物在日常生产生活中用途广泛,利用FeSO4制备还原铁粉的工业流程如下:
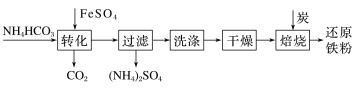
实验室中可用FeSO4(用铁粉和稀硫酸反应制得)和NH4HCO3溶液在如下装置模拟上述流程中的“转化”环节。
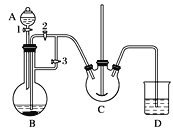
(1)装置A的仪器名称是________,装置B中盛放的药品是________。
(2)实验过程中,欲将生成的FeSO4溶液和NH4HCO3溶液混合,操作方法是____________________。FeSO4溶液要现用现配制的原因是_____________________。
(3)干燥过程的主要目的是脱去产物FeCO3中的游离水,该过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为_________________________________________,取干燥后的FeCO3样品24.98 g,与炭混合后焙烧,最终得到还原铁粉12.32 g,计算样品中FeCO3的质量分数________%(计算结果取整数)。

(4)高铁酸钠(Na2FeO4)是一种新型净水剂.用如图装置可以制取少量高铁酸钠.写出在用电解法制取高铁酸钠时,阳极的电极反应式___________________
(5)25 ℃时,Ksp[Fe(OH)3]=4.0×10-38 ,此温度下,若实验室中配制2.5mol/L 100mL硫酸铁溶液,为使配制过程中不出现浑浊,则至少需要加入10mol/L的硫酸______mL(忽略加入硫酸的体积)。
-
工业上需要利用一批回收的含铜废料制造胆矾(CuSO4·5H2O)。该废料中各种成份含量如下:Cu和CuO约占87%,其它为Mg、Al、Fe、Si及其氧化物,还有少量的难溶物质。工艺流程为:
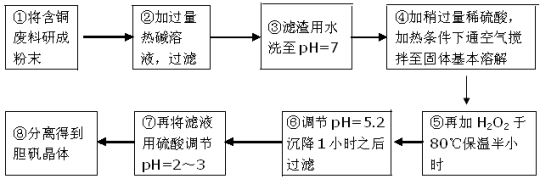
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 | Fe(OH)2 |
| pH | 5.2 | 3.1 | 6.7 | 9.4 | 9.7 |
请回答下列问题:
(1)步骤①中为什么要将含铜废料研磨成粉状? 。
(2)步骤②中的离子方程式(写出2个即可):
、
。
(3)步骤⑤中H2O2参加反应的离子方程式: 。
(4)步骤⑥中调节溶液pH时适宜的物质是 (填序号)。
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Cu(OH)2 E.MgCO3
(5)步骤⑦中用硫酸调节pH=2~3的原因是 。
(6)步骤⑧的分离方法步骤是 。
-
高锰酸钾是锰的重要化合物和常用氧化剂,在实验室和医疗上有非常广泛的应用。以下是工业上用软锰矿(主要含MnO2)制备高锰酸钾晶体的一种工艺流程:
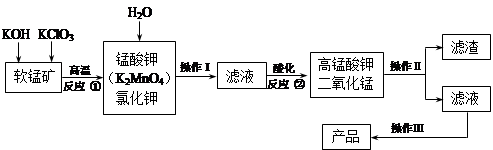
(1)操作Ⅱ的名称是_______,实验室进行该操作须用到的玻璃仪器有 ;
(2)反应②的产物中,氧化产物与还原产物的物质的 量之比是______;
(3)反应②中“酸化”时不能选择下列酸中的______(填字母序号)
a.稀盐酸 b.稀硫酸 c.稀醋酸
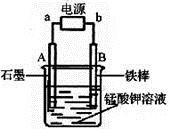
(4)电解锰酸钾溶液也可以制备高锰酸钾,其阴极反应式为:2H2O + 2e-= 2OH-+ H2↑,如图,b为电源的_______极,电解池的阳极反应式是_______;若电解过程中收集到2.24 L H2(标准状况),则得到高锰酸钾______g。(提示:阴离子放电顺序MnO42->OH-)
-
Ⅰ.高锰酸钾是锰的重要化合物和常用氧化剂,在实验室和医疗上有非常广泛的应用。如图1是工业上用软锰矿(主要含MnO2)制备高锰酸钾晶体的一种工艺流程:
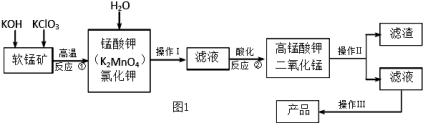
(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是(用化学方程式表示)。写出反应①的离子方程式;
(2)反应②的产物中,氧化产物与还原产物的物质的量的比是
(3)反应②中“酸化”时应选择下列酸中的(填序号)
a.稀盐酸b.稀硫酸c.亚硫酸
(4)操作Ⅱ的名称是,实验室进行该操作需用到的玻璃仪器有
Ⅱ.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质
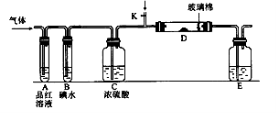
(5)若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?(填“相同”或“不相同”)。
(6)若装置B中装有5.0mL1.0mol/L的碘水,当通入足量C l2完全反应后,共转移了5.0×10-2mol电子,该反应的化学方程式为;
l2完全反应后,共转移了5.0×10-2mol电子,该反应的化学方程式为;
(7)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4∶3。当Cl2与含X的溶液完全反应后,有浅黄色沉淀产生,取少量上层清加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式。
-
孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下:
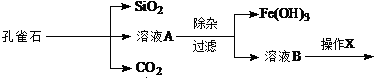

为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
(1)“除杂”时先通入足量H2O2将Fe2+氧化成Fe3+,再加入CuO固体。其中加入CuO作用是
________,需调节溶液pH的范围为________。
(2)操作X包括 蒸发浓缩、冷却结晶、过滤和洗涤等。在进行该操作时,需要将溶液B再
适当酸化目的________。
(3)若向溶液B中逐滴加入NaOH溶液,刚好出现沉淀时,请写出存在的难溶物质的沉淀溶解平衡方程式为 ________
(4) 为准确测定溶液A中含有Fe2+的物质的量浓度,实验如下:
①取出25.00mL溶液A,配制成250 mL 溶液。
②滴定:准确量取25.00ml所配溶液于锥形瓶中,将0.20mol/LKMnO4溶液
装入________,记录数据。重复滴定2次。平均消耗KMnO4溶液V mL。
(反应式: 5Fe2+ + MnO4— +10 H+ = 5Fe3+ + Mn2+ + 5H2O)
③ 计算溶液A中Fe2+的物质的量浓度=________mol/L (只列出算式,不做运算)。












