我国对可呼吸的钠——二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO22Na2CO3+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中)。关于该电池,下列说法错误的是
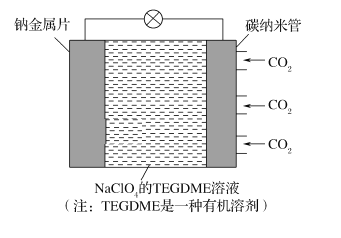
A. 放电时,当转移1 mol电子时负极质量减轻23 g
B. 充电时,Na+从阳极向阴极移动
C. 放电时,正极反应式为3CO2+4Na++4e-=2Na2CO3+C
D. 可以用乙醇代替TEGDME作有机溶剂
高三化学单选题中等难度题
我国对可呼吸的钠——二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO22Na2CO3+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中)。关于该电池,下列说法错误的是

A. 放电时,当转移1 mol电子时负极质量减轻23 g
B. 充电时,Na+从阳极向阴极移动
C. 放电时,正极反应式为3CO2+4Na++4e-=2Na2CO3+C
D. 可以用乙醇代替TEGDME作有机溶剂
高三化学单选题中等难度题
我国对‘可呼吸”的钠-二氧化碳电池的研究取得突破性进展。该电池的总反应式为:4Na+3CO2 2Na2CO3+C,其工作原理如下图所示(放电时产生Na2CO3固体储存于碳纳米管中)。下列说法不正确的是
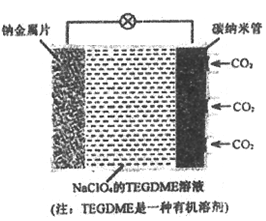
A.放电时,钠金属片作负极,碳纳米管作正极
B.充电时,阳极反应为:2Na2CO3+C-4e-=3CO2↑+4Na+
C.放电时,Na+从负极区向正极区移动
D.该电池的电解质溶液也可使用NaClO4的水溶液
高三化学单选题中等难度题查看答案及解析
我国对‘可呼吸”的钠-二氧化碳电池的研究取得突破性进展。该电池的总反应式为:4Na+3CO2 2Na2CO3+C,其工作原理如下图所示(放电时产生Na2CO3固体储存于碳纳米管中)。下列说法不正确的是
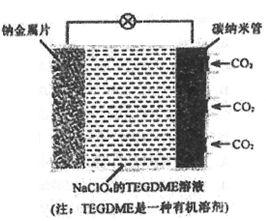
A. 放电时,钠金属片作负极,碳纳米管作正极
B. 充电时,阳极反应为:2Na2CO3+C-4e-=3CO2↑+4Na+
C. 放电时,Na+从负极区向正极区移动
D. 该电池的电解质溶液也可使用NaClO4的水溶液
高三化学选择题中等难度题查看答案及解析
我国对可呼吸的钠——二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO22Na2CO3+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中)。关于该电池,下列说法错误的是

A. 放电时,当转移1 mol电子时负极质量减轻23 g
B. 充电时,Na+从阳极向阴极移动
C. 放电时,正极反应式为3CO2+4Na++4e-=2Na2CO3+C
D. 可以用乙醇代替TEGDME作有机溶剂
高三化学单选题中等难度题查看答案及解析
我国对可呼吸的钠-二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO22Na2CO3+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中)。关于该电池,下列说法错误的是
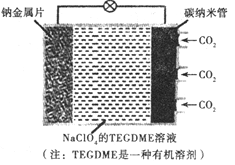
A. 充电时,Na+从阳极向阴极移动
B. 可以用乙醇代替TEGDME做有机溶剂
C. 放电时,当转移1mol电子负极质量减轻23g
D. 放电时,正极反应为3CO2 + 4Na++4e- = 2Na2CO3 + C
高三化学选择题困难题查看答案及解析
我国对可呼吸的钠-二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO22Na2CO3+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中)。关于该电池,下列说法错误的是
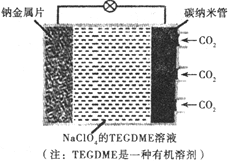
A. 充电时,Na+从阳极向阴极移动
B. 可以用乙醇代替TEGDME做有机溶剂
C. 放电时,当转移1mol电子负极质量减轻23g
D. 放电时,正极反应为3CO2 + 4Na++4e- = 2Na2CO3 + C
高三化学选择题困难题查看答案及解析
我国对可呼吸的钠-二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO22Na2CO3+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中)。关于该电池,下列说法错误的是
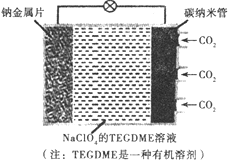
A. 充电时,Na+从阳极向阴极移动
B. 可以用乙醇代替TEGDME做有机溶剂
C. 放电时,当转移1mol电子负极质量减轻23g
D. 放电时,正极反应为3CO2 + 4Na++4e- = 2Na2CO3 + C
高三化学单选题困难题查看答案及解析
“可呼吸”钠-二氧化碳电池的工作原理为4Na+3CO22Na2CO3+C。下列叙述错误的是
A. 放电时,Na+由负极向正极移动
B. 充电时,阴极反应式为Na++ e—= Na
C. 电解质溶液可选NaClO4水溶液
D. 电池放电时把二氧化碳变废为宝,有重要的研发意义
高三化学选择题中等难度题查看答案及解析
据报导,我国已研制出“可充室温钠----二氧化碳电池”,电极材料为钠金属片和碳纳米管,电解液为高氯酸钠四甘醇二甲醚,电池总反应式为4Na+3CO22Na2CO3+C,生成的固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是( )
A.放电时钠金属片发生氧化反应
B.放电时吸收CO2,充电时释放CO2
C.放电时Na+向碳纳米管移动
D.放电时正极的电极反应式为2Na-2e-+CO32-=Na2CO3
高三化学单选题中等难度题查看答案及解析
据报导,我国已研制出“可充室温钠-二氧化碳电池”,电极材料为钠金属片和碳纳米管,电解液为高氯酸钠-四甘醇二甲醚,电池总反应为:4Na+3CO22Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是( )
A. 放电时钠金属片发生氧化反应
B. 充电时碳纳米管接直流电源的正极
C. 放电时每消耗3mol CO2,转移12mol电子
D. 充电时的阳极反应为C+2Na2CO3—4e-===3CO2↑+4Na+
【答案】C
【解析】A. 放电时金属钠失电子,发生氧化反应,故A正确;B. 充电时,碳纳米管失电子,发生氧化反应,所以碳纳米管为阳极,应接电源的正极,故B正确;C. 根据反应方程式可知,放电时,每消耗3 mol CO2,4mol钠失去电子,转移电子4mol,故C错误;D. 充电时,碳失电子在阳极发生氧化反应,电极反应式为C+2Na2CO3-4e-=3CO2↑+4Na+,故D正确;答案选C。
点睛:本题通过新型电源考查原电池及电解池的相关知识。熟练掌握电极判断、电极反应、工作原理等为解答本题的关键,解题时注意电化学知识的应用,对于可充电电池,放电时为原电池,充电时为电解池,且充电时阳极与正极相连、阴极与负极相连。
【题型】单选题
【结束】
13
探究浓度对化学平衡的影响,实验如下:
I.向5mL 0.05mol/L FeCl3溶液中加入5mL 0.05mol/L KI溶液(反应a),平衡后分为两等份
Ⅱ.向一份加入饱和KSCN溶液,变红(反应b);加入CCl4,振荡、静置,下层显极浅的紫色
Ⅲ.向另一份加入CCl4,振荡、静置,下层显紫红色
结合实验,下列说法不正确的是
A. 反应a为:2Fe3++ 2I-2Fe2++I2
B. Ⅱ中,反应a进行的程度大于反应b
C. 比较氧化性:Ⅱ中,I2>Fe3+
D. 比较水溶液中c(Fe2+):Ⅱ<Ⅲ
高三化学单选题困难题查看答案及解析
据报导,我国已研制出“可充室温钠-二氧化碳电池”,电极材料为钠金属片和碳钠蜜管,电解液为高氯酸钠-四甘醇二甲醚,电池总反应为:4Na+3CO22Na2CO3+C,生成固体Na2CO3沉积在碳钠米管上。下列叙述不正确的是
A. 放电时钠金属片发生氧化反应
B. 充电时碳钠米管接直流电源的正极
C. 充电时的阳极反应为C+2Na2CO3-4e-=3CO2↑+4Na+
D. 放电时每消耗3molCO2,转移12mol电子
高三化学选择题中等难度题查看答案及解析