-
铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用。

(1)用铁屑与稀硫酸反应制备FeSO4
①制备原理用离子方程式表示为________。若要提高FeSO4生成速率,采取下列措施中正确的是________。
A.使用浓硫酸与铁屑反应
B.使用磨细的铁粉反应
C.控制温度在50~70℃
D.控制温度在80~100℃
②在上述反应过程中,常会伴随发生反应:4Fe2++O2+4H+ 4Fe3++2H2O
4Fe3++2H2O
若要减少产品FeSO4中Fe3+的含量,采取下列措施中正确的是________。
A.控制稀硫酸的浓度不能太高
B.用去O2蒸馏水注入浓硫酸配制反应所需的稀硫酸
C.反应中保持n(Fe)/n(H2SO4) >1
D.反应中应经常添加Fe2(SO4)3搅拌
③反应结束后,将溶液进行________、冷却、过滤、洗涤即得FeSO4·7H2O晶体。
(2)工业上用含有少量Cu、Al的废铁屑制备Fe2(SO4)3
其反应及操作流程如下:
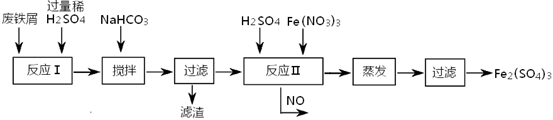
①加入NaHCO3并搅拌,将混合液pH调控至________范围内,使杂质沉淀过滤除去。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 | 4.7 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 | 6.7 |
②反应Ⅱ中反应的离子方程式是:________。
③生产中,将反应Ⅱ产生的NO配比一种气体X,混合后重新通入反应Ⅱ中,该设计的目的是________,气体X与NO配比的比例是________。
(3)用Fe2(SO4)3处理含S2-污水时,有黑色沉淀及淡黄色悬浮物产生,其反应的离子方程式是________。
-
钛被誉为“21世纪的金属”,在工农业生产、医疗、国防、科技等方面中有着极其广泛而重要的用途。四氯化钛是工业上制备金属钛的重要原料。在常温下,它是一种极易水解的无色液体,沸点为136.4℃。工业制备TiCl4的反应原理为:TiO2+2C+2Cl2 =TiCl4+2CO。
=TiCl4+2CO。
下图是实验室模拟工业生产制备四氯化钛的反应装置,其主要操作步骤有(顺序己打乱):
①连接好整套装置,并检査装置的气密性;
②当锥形瓶中的TiCl4的量不再增加时,停止加热,改通CO2气体直至电炉中的瓷管冷却为止;
③将Ti02、炭粉混合均匀后,装入管式电炉中;
④将电炉升温至800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水;
⑤通入干燥的CO2气体并持续一段时间。
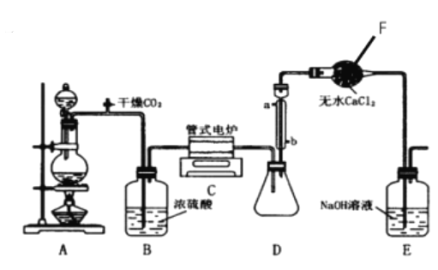
试回答:
(1)仪器F的名称是_______________,装罝A所用的试剂名称是_______________。
(2)正确的操作程序是(填写操作步骤的序号)______________________________。
(3)操作⑤的目的是______________________________。
(4)装置中冷凝管进水口的位置是(填a或b)_______________,装置E的作用_______________。
(5)将少量TiCl4露置于空气中,可能看到的现象是______________________________。
(6)利用化合物TiCl4可制备TiO2,请结合化学用语解释该过程:_______________。
-
(15分)铁、铝及其化合物在生活、生产中有着广泛的应用。
Ⅰ.某研究性学习小组对某硫酸亚铁晶体(FeSO4•xH2O)热分解进行研究。该小组同学称取a g硫酸亚铁晶体样品按下图图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出x的值。
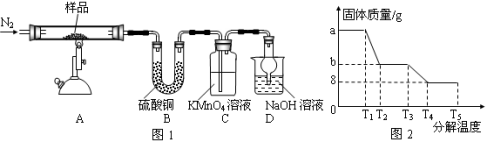
(1)装置B中硫酸铜粉末变蓝,质量增加12.6 g,说明产物中有水,装置C中高锰酸钾溶液褪色,说明产物中还有 。
(2)实验中要持续通入氮气,否则测出的x会 (填“偏大”、“偏小”或“不变”)。
(3)硫酸亚铁晶体完全分解后装置A中还残留红棕色固体Fe2O3。
(4)从理论上分析得出硫酸亚铁分解还生成另一种物质SO3,写出FeSO4分解的化学方程式 。
(5)某研究所利用SDTQ 600热分析仪对硫酸亚铁晶体(FeSO4•xH2O)进行热分解,获得相关数据,绘制成固体质量-分解温度的关系图如上图图2。根据两种热分解实验的有关数据,可计算出FeSO4•xH2O中的x= 。
Ⅱ.铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。
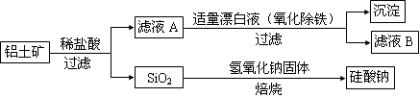
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的操作方法为: 。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为 (填选项编号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:
边滴加浓盐酸边蒸发浓缩、 (填操作名称)、过滤、洗涤。
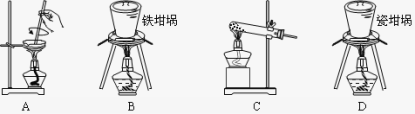
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填选项编号)。
-
(14分)FeSO4·7H2O广泛用于医药和工业领域,以下是FeSO4·7H2O的实验室制备流程图。根据题意完成下列填空:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_____,浸泡后,用____(填操作方法)分离并洗涤铁屑。
(2)操作a为_______________。
(3)最后得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;
②____________________。
(4) FeSO4·7H2O是某些补血剂的主要成分,实验室要测定某补血剂中铁元素的含量。
I.方案一:可用KMn04溶液进行氧化还原滴定。在配制100mL 1.00 × 10 - 2 mol·L-1的KMnO4溶液时,所用的仪器有天平、药匙、烧杯、玻璃棒,还有___________(填仪器名称)。在配制过程中,下列说法正确的是____________(填序号字母)。
A.KMnO4溶于水不放热,可以直接在容量瓶中溶解
B.容量瓶洗涤后不需干燥即可直接用于实验
C.定容后摇匀,凹液面低于刻度线,再加水至凹液面最低点与刻度线相平
D.如果定容时加水超过刻度线必须毓配制
II.方案二:将FeSO4·7H2O最终转化为Fe2O3,测定质量变化,操作流程如下:
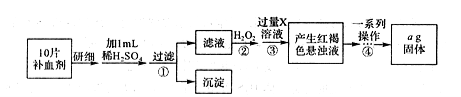
①步骤④中一系列操作依次是:过滤、洗涤、______、冷却、称量。
②假设实验过程中Fe无损耗,则每片补血剂含铁元素的质量______g(用含a的代数式表示)。
③若步骤③加入X溶液的量不足,则最后测出每片补血剂含铁元素的质量将______(填“偏大,’.“偏小”或“不变”)。
-
(19分)FeSO4·7H2O广泛用于医药和工业领域,实验室制备FeSO4·7H2O的流程如下:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_________。
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;②_____________________。
(3)FeSO4·7H2O是某些补血剂的主要成分,实验室用KMnO4溶液通过氧化还原滴定测定某补血剂(1.500 g)中铁元素的含量。
①配制100 mL 1.200 × 10 —2 mol·L—1的KMnO4溶液时,将溶解后的溶液转移至容量瓶中的操作方法是__________________________;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是_________________。
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在__________滴定管中。滴定到终点时的现象为_____________________。滴定完毕,三次实验记录KMnO4标准溶液的读数如下。
| 滴定次数实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
该补血剂中铁元素的质量分数为_____________________。
(4)某实验小组用久置的FeSO4溶液和NaOH溶液制备Fe(OH)2,实验后没有得到预期的白色沉淀,于是采用下列试剂(已煮沸除氧)和装置进行实验:
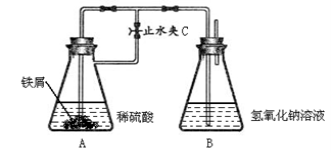
实验开始打开止水夹C,目的是_______________________。一段时间后,关闭止水夹C, B中观察到的现象是______________________。B中发生反应的离子方程式是___________________。
-
FeSO4·7H2O广泛用于医药和工业领域,实验室制备FeSO4·7H2O的流程如下:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_________。
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;②_____________________。
(3)FeSO4·7H2O是某些补血剂的主要成分,将1.5 g某补血剂预处理,配成100mL溶液。实验室用KMnO4溶液通过氧化还原滴定测定该补血剂(1.5 g)中铁元素的含量,①配制100 mL 1.200 × 10 —2 mol·L—1的KMnO4溶液时,将溶解后的溶液转移至容量瓶中的操作方法是__________________________;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是_________________。
a. 稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在__________滴定管中。滴定到终点时的现象为____________。
③滴定完毕,三次实验记录KMnO4标准溶液的读数如下。
| 滴定次数实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
该补血剂中铁元素的质量分数为_____________________。
-
(16分)工业上利用废铁屑(含少量氧化铝、氧化铁等)生产硫酸亚铁溶液,进而可制备绿矾(FeSO4·7H2O)、硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐)等重要试剂。生产硫酸亚铁溶液的工艺流程如下:
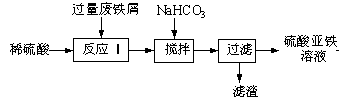
回答下列问题:
(1)加入少量NaHCO3,调节溶液pH的目的是__________________________。
(2)硫酸亚铁溶液在空气中久置容易变质,用离子方程式表示其变质的原因:_____。
(3)若向所得FeSO4溶液中加入少量3 moL• L-1 H2SO4溶液,再加入饱和(NH4)2SO4溶液,经过蒸发浓缩、冷却结晶、过滤等一系列操作后得到硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐)。硫酸亚铁铵较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.352g Cu2S和CuS的混合物在酸性溶液中用40.00 mL0.150 mol•L-1 KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
反应后煮沸溶液,剩余的KMnO4恰好与50.00mL 0.200 mol•L-1 (NH4)2Fe(SO4)2溶液完全反应。
①配平离子方程式: MnO4-+ Fe2++ H+—— Mn2++ Fe3++ H2O
②Cu2S和CuS的混合物在酸性溶液中用0.150 mol•L-1 KMnO4溶液处理后,溶液需煮沸的原因是:_______________________________________________。
③实验室配制500mL 3 moL• L-1 H2SO4溶液,需要质量分数为98%,密度为1.84g• mL-1硫酸的体积为__________ mL。(保留1位小数)
④试计算混合物中CuS的质量分数(写出计算过程)。
-
铁及其化合物在工农业生产、环境保护等领域中有着重要的作用。
(1)硫酸铁铵[NH4Fe(SO4)2·12H2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。写出硫酸铁铵溶液中离子浓度的大小顺序 。
(2)FeSO4/KMnO4工艺与单纯混凝剂[FeCl3、Fe2(SO4)3]相比,大大降低了污水处理后水的浑浊度,显著提高了对污水中有机物的去除率。二者的引入并未增加沉降后水中总铁和总锰浓度,反而使二者的浓度降低,原因是在此条件下(pH约为7)KMnO4可将水中Fe2+、Mn2+氧化为固相的+3价铁和+4价锰的化合物,进而通过沉淀、过滤等工艺将铁、锰除去。已知:Ksp(Fe(OH)3=4.0×10-38,则沉淀过滤后溶液中c(Fe3+)约为 mol·L-1。写出生成+4价固体锰化合物的反应的离子方程式 。
(3)新型纳米材料ZnFe2Ox,可用于除去工业废气中的某些氧化物。制取新材料和除去废气的转化关系如图:

用ZnFe2Ox除去SO2的过程中,氧化剂是 。(填化学式)
(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。先通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2CO+H2S=2[Fe(CN)6]4-+2HCO+S↓。电解时,阳极的电极反应式为 ;电解过程中阴极区溶液的pH (填“变大”、“变小”或“不变”)。

-
铁及其化合物在工农业生产、环境保护等领域中有着重要的作用。
(1)硫酸铁铵[NH4Fe(SO4)2·12H2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。写出硫酸铁铵溶液中离子浓度的大小顺序 。
(2)FeSO4/KMnO4工艺与单纯混凝剂[FeCl3、Fe2(SO4)3]相比,大大降低了污水处理后水的浑浊度,显著提高了对污水中有机物的去除率。二者的引入并未增加沉降后水中总铁和总锰浓度,反而使二者的浓度降低,原因是在此条件下(pH约为7)KMnO4可将水中Fe2+、Mn2+氧化为固相的+3价铁和+4价锰的化合物,进而通过沉淀、过滤等工艺将铁、锰除去。已知:Ksp(Fe(OH)3=4.0×10-38,则沉淀过滤后溶液中c(Fe3+)约为 mol·L-1。写出生成+4价固体锰化合物的反应的离子方程式 。
(3)新型纳米材料ZnFe2Ox,可用于除去工业废气中的某些氧化物。制取新材料和除去废气的转化关系如图:

①用ZnFe2Ox除去SO2的过程中,氧化剂是 。
②用ZnFe2Ox除去NO2的过程中,若x=3,则消除1 mol NO2,需要ZnFe2Ox的质量为 g。
③用ZnFe2O4制取ZnFe2Ox的过程中,若x=3.5,则ZnFe2O4与H2反应的物质的量之比为 。
(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2CO+H2S=2[Fe(CN)6]4-+2HCO+S↓。电解时,阳极的电极反应式为 ;电解过程中阴极区溶液的pH (填“变大”、“变小”或“不变”)。

-
铁及其化合物在生产和生活中有着广泛的应用。
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:回答下列问题:
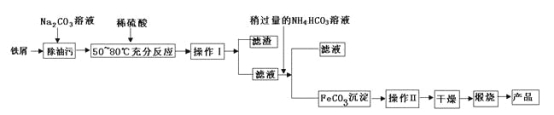
①操作Ⅰ、Ⅱ的名称分别是____、____。
②写出在空气中煅烧FeCO3的化学方程式__________________;
③煅烧如果不充分,产品中将有Fe2+存在,试设计实验检验产品中有无Fe2+______。
(2)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定。称取2.850g绿矾(FeSO4·7H2O)产品,溶解,在250mL容量瓶中定容;量取25.00mL待测溶液于锥形瓶中;用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①写出酸性KMnO4溶液与FeSO4溶液反应的离子方程式_________________________
②计算上述样品中FeSO4·7H2O的质量分数为__________________[已知M(FeSO4·7H2O)=278g/mol]
③滴定达到终点时锥形瓶中溶液颜色变化为______________________________
④下列操作会导致样品中FeSO4·7H2O的质量分数的测定结果偏高的有_____________。
a.未干燥锥形瓶
b.盛装标准液的滴定管没有用标准液润洗
c. 滴定终点时滴定管尖嘴中产生气泡
d.量取待测液,视线注视刻度时开始平视、结束俯视

4Fe3++2H2O















