-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.5 mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出320.8 kJ的热量。
(1)肼的电子式为___________________,过氧化氢的电子式为__________________。
(2)写出反应的热化学方程式:________________________________________________。
(3)在25 ℃、101 kPa时,已知18 g水蒸气变成液态水放出44 kJ的热量。其他相关数据如下表:
| O===O | H—H | H—O(g) |
| 1 mol化学键断裂时 需要吸收的能量/kJ | 496 | 436 | 463 |
写出表示H2燃烧热的热化学方程式___________________________________________;则32 g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是________kJ。
(4)联氨和H2O2可作为火箭推进剂的主要原因为_________________________________。
(5)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为____________(已知:N2H4+H+ N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为_______________。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为_______________。
-
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为__。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为:___。
(3)①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
写出联氨和N2O4作为火箭推进剂反应的热化学方程式(△H用含△H1,△H2,△H3的代数式表示)___。
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题:
(1)联氨分子的电子式为 ,其中氮的化合价为 .
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 .
(3)①2O2(g)+N2(g)═N2O4(l)△H1
②N2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=﹣1048.9kJ•mol﹣1
上述反应热效应之间的关系式为△H4= ,联氨和N2O4可作为火箭推进剂的主要原因为 。
-
Ⅰ.联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
回答下列问题:
(1)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为________________。
(2)①2O2(g)+N2(g)===N2O4(l) ΔH1
②N2(g)+2H2(g)===N2H4(l) ΔH2
③O2(g)+2H2(g)===2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)===3N2(g)+4H2O(g) ΔH4=-1048.9 kJ·mol-1
上述反应热效应之间的关系式为ΔH4=__________________,联氨和N2O4可作为火箭推进剂的主要原因为________________。
Ⅱ.煤燃烧排放的烟气含SO2和NO2,形成酸雨,污染大气。现用NaClO、Ca(ClO)2处理,得到较好的烟气脱硫效果。
(3)已知下列反应:
SO2(g)+2OH-(aq)===SO32- (aq)+H2O(l) ΔH1
ClO-(aq)+SO32- (aq)===SO42- (aq)+Cl-(aq) ΔH2
CaSO4(s)===Ca2+(aq)+SO42- (aq) ΔH3
则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)===CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=________。
Ⅲ.工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25 ℃,101 kPa时:
CaO(s)+H2SO4(l)===CaSO4(s)+H2O(l) ΔH=-271 kJ/mol
5CaO(s)+3H3PO4(l)+HF(g)===Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是__________________。
-
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为__________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2 (g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=________________,联氨和N2O4可作为火箭推进剂的主要原因为____________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 。
-
[2016新课标Ⅱ节选]联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为_____________________。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
(1)联氨分子的电子式为______________,
(2)联氨为二元弱碱,在水中的电离方式与氨相似。写出在水中联氨第一步电离反应的方程式______________________________________________________。
(3)已知12.8 g的液态高能燃料联氨在氧气中燃烧,生成气态N2和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式___________________。
(4)已知①2O2(g)+N2(g)=N2O4(l) ;ΔH1
②N2(g)+2H2(g)=N2H4(l) ;ΔH2
③O2(g)+2H2(g)=2H2O(g) ; ΔH3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ;ΔH4
上述反应热效应之间的关系式为ΔH4=_________________,联氨和N2O4可作为火箭推进剂的主要原因为____________________________________________ (至少答2点)。
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
I、(1)联氨分子的电子式为______________,
(2)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的方程式_______________。联氨与盐酸反应生成的正盐的化学方程式为__________________
II、某探究小组利用下列反应制取水合肼(N2H4·H2O):CO(NH2)2+2NaOH+NaClO===Na2CO3+N2H4·H2O+NaCl
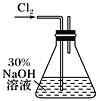
实验一:制备NaClO溶液(实验装置如上图所示)
(1)配制30%NaOH溶液时,所需的玻璃仪器除量筒外,还有________(填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
实验二:制取水合肼(实验装置如右图所示)。
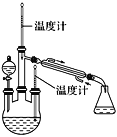
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114 ℃馏分。(已知:N2H4·H2O+2NaClO===N2↑+3H2O+2NaCl)
(2)分液漏斗中的溶液是________(填标号)。
A.CO(NH2)2溶液 B.NaOH和NaClO混合溶液
选择的理由是__________________________________________________
实验三:测定馏分中水合肼的含量。
称取馏分5.000 g,加入适量NaHCO3固体,加水配成250 mL溶液,移取25.00 mL,用0.100 0 mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5 左右。(已知:N2H4·H2O+2I2===N2↑+4HI+H2O)
(3)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是_____________________。
(4)本实验用____________做指示剂,当滴定达到终点时的现象为_____________________。
(5)实验测得消耗I2溶液的平均值为18.00 mL,馏分中水合肼(N2H4·H2O)的质量分数为________。
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________。
(2)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=__________,联氨和N2O4可作为火箭推进剂的主要原因为______________。
(3)联氨为二元弱碱,在水中的电离方式与氨相似,联氨第一步电离方程式为:_________________。
-
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为______________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=____________,联氨和N2O4可作为火箭推进剂的主要原因为________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为_______________。

