近年来,尿素电氧化法处理富含尿素的工业废水和生活污水得到了广泛关注,该法具有操作简易、处理量大、运行周期长等优点,且该过程在碱性条件下产生无毒的C02、N2。电池工作时,下列说法错误的是
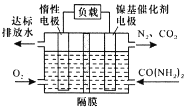
A. 负极发生的反应为:CO(NH2)2+6OH——6e—=N2↑+CO2↑+5H2O
B. 正极附近溶液的pH增大
C. 隔膜只允许阳离子通过
D. 处理掉废水中尿素1.0g时消耗O2 0.56L(标准状况)
高三化学单选题中等难度题
近年来,尿素电氧化法处理富含尿素的工业废水和生活污水得到了广泛关注,该法具有操作简易、处理量大、运行周期长等优点,且该过程在碱性条件下产生无毒的C02、N2。电池工作时,下列说法错误的是

A. 负极发生的反应为:CO(NH2)2+6OH——6e—=N2↑+CO2↑+5H2O
B. 正极附近溶液的pH增大
C. 隔膜只允许阳离子通过
D. 处理掉废水中尿素1.0g时消耗O2 0.56L(标准状况)
高三化学单选题中等难度题
近年来,尿素电氧化法处理富含尿素的工业废水和生活污水得到了广泛关注,该法具有操作简易、处理量大、运行周期长等优点,且该过程在碱性条件下产生无毒的C02、N2.电池工作时,下列说法错误的是( )

A. 负极发生的反应为:
B. 正极附近溶液的pH增大
C. 隔膜只允许阳离子通过
D. 处理掉废水中尿素1.0g时消耗O2 0.56L(标准状况)
高三化学单选题中等难度题查看答案及解析
近年来,尿素电氧化法处理富含尿素的工业废水和生活污水得到了广泛关注,该法具有操作简易、处理量大、运行周期长等优点,且该过程在碱性条件下产生无毒的C02、N2。电池工作时,下列说法错误的是

A. 负极发生的反应为:CO(NH2)2+6OH——6e—=N2↑+CO2↑+5H2O
B. 正极附近溶液的pH增大
C. 隔膜只允许阳离子通过
D. 处理掉废水中尿素1.0g时消耗O2 0.56L(标准状况)
高三化学单选题中等难度题查看答案及解析
三氯化铁是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中,先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(1)将标准状况下的a L氯化氢气体溶于100 g水中,得到的盐酸的密度为b g·mL-1,则该盐酸的物质的量的浓度是________。
(2)向100 mL的FeBr2溶液中通入标准状况下Cl2 3.36 L,反应后的溶液中Cl- 和Br- 的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为________。
(3)FeCl3溶液可以用来净水,其净水的原理为______________________________________(用离子方程式表示),若100mL 2mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数________0.2NA(填“大于”、“等于”或“小于”)。
高三化学填空题中等难度题查看答案及解析
三氯化铁是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中,先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(1)将标准状况下的a L氯化氢气体溶于100 g水中,得到的盐酸的密度为
b g·mL-1,则该盐酸的物质的量的浓度是________。
向100 mL的FeBr2溶液中通入标准状况下Cl2 3.36 L,反应后的溶液中Cl- 和Br- 的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为 ________。
(3)FeCl3溶液可以用来净水,其净水的原理为____________________ _____________________(用离子方程式表示),若100mL 2mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数________0.2NA(填“大于”、“等于”或“小于”)。
高三化学填空题中等难度题查看答案及解析
FeCl3是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中,先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(1)将标准状况下的a L氯化氢气体溶于100 g水中,得到盐酸的密度为b g·mL-1,则该盐酸的物质的量浓度是________。
(2)向100 mL的FeBr2溶液中通入标准状况下Cl2 3.36 L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为________。
(3)FeCl3溶液可以用来净水,其净水的原理为___________________(用离子方程式表示)。用100 mL 2 mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数________(填“大于”“等于”或“小于”)0.2NA。
高三化学计算题简单题查看答案及解析
过氧化氢(H2O2)俗称双氧水。是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业。回答下列问题:
(1) H2O2的电子式为_______________。
(2)用H2O2与稀硫酸的混合溶液可溶出印刷电路板金属粉末中的铜。
已知:Cu(s)+2H+ (aq)==Cu2+(aq) + H2(g) ∆H= +64 kJ/mol
2H2O2(1) ==2H2O(l)+O2(g) ∆H =-196 kJmol
H2(g) + l/2O2(g) ==H2O(l) ∆H =-286 kJ/mol
则在稀硫酸溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为:__________________。
(3)工业上常用电解硫酸氢铵水溶液的方法制备过氧化氢,其原理为:首先2NH4HSO4 (NH4)2S2O8+ H2↑,然后由(NH4)2 S2O8水解得到H2O2和另一产物。则:
①电解时阳极的电极反应式为___________________;
②(NH4)2 S2O8水解时发生反应的化学方程式为 ____________________。
(4)现甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方案。
| 实验编号 | 温度 | 催化剂 | 浓度 |
| 甲组实验I | 25℃ | 三氧化二铁 | 10mL 5% H2O2 |
| 甲组实验II | 25℃ | 二氧化锰 | 10 mL 5% H2O2 |
甲、乙两小组得出如下图数据。
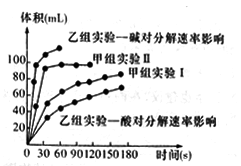
①甲小组实验得出的结论是______________________。
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析,相同条件下H2O2在________(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2固体与硫酸溶液反应制H2O2,其反应的离子方程式为_______________;支持这一方案的理由是_______________________。
③已知过氧化氢还是一种极弱的二元酸:H2O2H++HO2-(Ka1=2.4×10-12)。当稀H2O2溶液在碱性环境下分解时会发生反应H2O2+OH-
HO2-+H2O,该反应中,正反应速率为V正=k正•c(H2O2)• c(OH- ),逆反应速率为v逆=k逆•c(H2O) • c(HO2-),其中k正、k逆为速率常数,则k正与k逆的比值为_________(保留3位有效数字)。
高三化学简答题中等难度题查看答案及解析
近年来,随着人类社会的快速发展,环境污染日益严重,而环境污染中的很多问题是由于氮磷富集化引起的,所以如何降低水体中的氮磷含量问题受到广泛关注。目前有两种较为有效的氨氮废水处理方法。
I.化学沉淀法
利用了Mg2+与PO43-与氨氮生成MgNH4PO4∙6H2O沉淀以达到去除氨氮的效果。
已知:磷在pH=8-10时主要存在形式为HPO42-
Ksp(MgNH4PO4∙6H2O)=2.5×10-13
(1)请写出pH=8时,化学沉淀法去除NH4+的离子方程式为_。
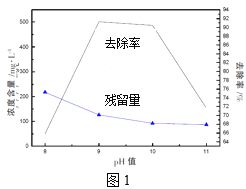
(2)氨氮去除率与含磷微粒浓度随pH变化如图1所示,已知:Ksp[Mg3(PO4)2]=6.3×10-26,请解释pH>10时氨氮去除率随pH变化的原因:__。
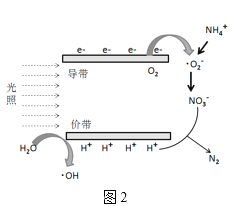
II.光催化法
(3)光催化降解过程中形成的羟基自由基(·OH)和超氧离子(·O2-)具有光催化能力,催化原理如图2所示。请写出NO3-转化为无毒物质的电极反应式:__。
(4)经过上述反应后,仍有NH4+残留,探究其去除条件。
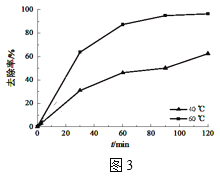
①温度对氨氮去除率影响如图3所示。温度升高,氨氮去除率变化的可能原因是:__;__(请写出两条)。
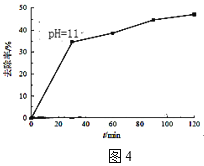
②选取TiO2作为催化剂,已知:TiO2在酸性条件下带正电,碱性条件下带负电。请在图4中画出pH=5时,氨氮去除率变化曲线_____。
(5)为测定处理后废水中(含少量游离酸)残留NH4+浓度,可选用甲醛-滴定法进行测定。取20mL的处理后水样,以酚酞为指示剂,用0.0100mol/LNaOH滴定至酚酞变红,此时溶液中游离酸被完全消耗,记下消耗NaOH的体积V1mL;然后另取同样体积水样,加入甲醛,再加入2-3滴酚酞指示剂,静置5min,发生反应:6HCHO+4NH4+=(CH2)6N4H+ +6H2O+3H+,继续用NaOH滴定,发生反应:(CH2)6N4H++OH-=(CH2)6N4+H2O;H++OH-=H2O。滴定至终点,记录消耗NaOH的体积V2mL,水样中残留NH4+浓度为__mol/L。
高三化学综合题困难题查看答案及解析
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。若酸性FeCl2废液中c(Fe2+)=2.0×10-2 mol·L-1,c(Fe3+)=1.0×10-3 mol·L-1,c(Cl-)=5.3×10-2 mol·L-1,则该溶液的pH约为________。
高三化学填空题困难题查看答案及解析
氯化铁和高铁酸钾都是常见的水处理剂。某兴趣小组以铁屑为原料模拟工业上制备氯化铁及进一步氧化制备高铁酸钾的流程如下:
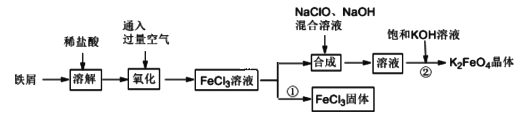
请回答下列问题:
(Ⅰ)(1)“氧化”阶段通入过量空气比用氯气作氧化剂具有的优点是__________________。
(2)“合成”阶段生成Na2FeO4的离子方程式为_______________________________。
(3)为了检验“氧化”过程中所得溶液中是否含有Fe2+,某同学取少量溶液于试管中,选用下列试剂可以达到目的的是_______(填字母)。
a.KSCN 溶液 b.NaOH 溶液 c.K3[Fe(CN)6]溶液 d.苯酚溶液 e.酸性KMnO4溶液
(4)过程①制取FeCl3固体的具体操作步骤是_______________________。若使6.5 mol/LFeCl3饱和溶液不析出Fe(OH)3,需控制溶液的pH 小于_________{已知该实验条件下,Ksp[(Fe(OH)3]=6.5×10-36,Kw=1.0×10-13(水离子积)}
(Ⅱ)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。
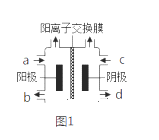
(1)收集到(CH3)4NOH的区域是________(填a、b、c或d)。
(2)写出电解池总反应(化学方程式)__________________________________。
高三化学综合题中等难度题查看答案及解析
(13分)近些年来,世界各地频现种种极端天气。二氧化碳、氮氧化物、二氧化硫等是导致极端天气的重要因素,研究这些化合物的综合处理具有重要意义。
(1)工业上可利用二氧化碳和氨气合成尿素,其总反应如下:
2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(l)
,该反应在 (填“较高温度”或“较低温度”)下能自发进行。
(2)已知合成尿素分两步进行:
第1步:2NH3(g)+CO2(g) NH2COONH4(s)
第2步:NH2COONH4(s) CO(NH2)2(l)+ H2O(l)
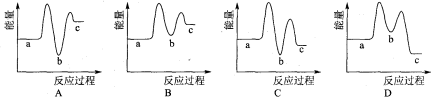
下列示意图中[a表示2NH3(g)+ CO2(g),b表示NH2COONH4(S),c表示CO(NH2)2(l)+ H2O(l)],能正确表示尿素合成过程中能量变化曲线的是(填序号) 。
(3)合成尿素过程中,当NH3与CO2的物质的量之比为1:2时,NH3
的转化率随时间的变化关系如图所示。
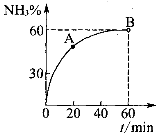
①A点的逆反应速率v逆(CO2) B点的逆反应速率
v逆 (CO2)(填“﹤”“﹥”或“=”)。
②达到平衡时,CO2的转化率为 。
(4)活性炭可用于处理大气污染物NO,在某1L恒容密闭容器中加入 0.100molNO 和2.030mol固体活性炭(无杂质),生成气体E和气体F。当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
|
n/mol T/℃ | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
①请结合上表数据,写出NO与活性炭反应的化学方程式 。
②上述反应在T1℃时的平衡常数为K1,在T2℃时的平衡常数为K2。计算K1= ,根据题给信息判断,T1和T2的关系是 。
A. T1>T2 B. T1<T2 C.无法比较
③若密闭容器为容积可变,根据化学反应原理,分析增加压强对该反应的影响
。
高三化学简答题中等难度题查看答案及解析