-
(1)写出氯碱工业电解饱和食盐水的化学方程式:___________________________
(2)已知:2KMnO4 + 16HCl =2KCl+2MnCl2 +5Cl2↑+8H2O,15.8g KMnO4 与100mL12mol/L浓盐酸充分反应,固体完全溶解,生成标准状况下氯气的体积为________L,转移的电子数为_________个,若向反应后的溶液中加入足量的硝酸银,过滤、洗涤、干燥,可得到固体______g。
(3)将标准状况下6.72L的HCl溶于水形成250mL溶液,取出10mL于锥形瓶中,溶质的物 质的量浓度为______mol/L,向锥形瓶中滴加0.5mol/LBa(OH)2溶液,恰好反应,消耗Ba(OH)2的体积为__________mL。
高一化学综合题中等难度题查看答案及解析
-
(1)写出氯碱工业电解饱和食盐水的化学方程式:___________________________
(2)已知:2KMnO4 + 16HCl =2KCl+2MnCl2 +5Cl2↑+8H2O,15.8g KMnO4 与100mL12mol/L浓盐酸充分反应,固体完全溶解,生成标准状况下氯气的体积为________L,转移的电子数为_________个,若向反应后的溶液中加入足量的硝酸银,过滤、洗涤、干燥,可得到固体______g。
(3)将标准状况下6.72L的HCl溶于水形成250mL溶液,取出10mL于锥形瓶中,溶质的物 质的量浓度为______mol/L,向锥形瓶中滴加0.5mol/LBa(OH)2溶液,恰好反应,消耗Ba(OH)2的体积为__________mL。
高一化学综合题中等难度题查看答案及解析
-
工业上制取氯气大多采用电解饱和食盐水的方法,以此为基础的工业称为“氯碱工业”,它是化学工业的一个重要支柱.电解饱和食盐水可产生氯气、氢气和氢氧化钠.
(1)若电解饱和食盐水消耗NaCl 117g,计算理论上最多可制得氯气的体积(标准状况).
(2)因氯气有毒,制氯气时需用氢氧化钠溶液来吸收尾气,若将7.1g氯气用氢氧化钠溶液完全吸收,需消耗0.5mol/L NaOH溶液的体积为多少?高一化学解答题中等难度题查看答案及解析
-
(12分)氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
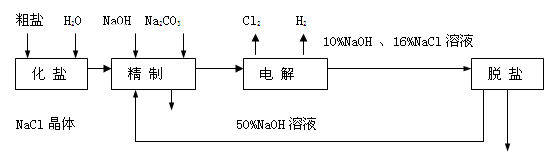
依据上图,完成下列填空:
(1)写出电解饱和食盐水的化学方程式 。
(2)如果粗盐中SO
含量较高,必须添加钡试剂除去SO
,该钡试剂可以是 (选填A、B、C,多选扣分)
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(3)判断钡试剂已经过量的方法是 。
(4)为有效除去Ca2+、Mg2+、SO
,加入试剂的合理顺序为 (选填A,B,C多选扣分)
A.先加NaOH溶液,后加Na2CO3溶液,再加钡试剂
B.先加NaOH溶液,后加钡试剂,再加Na2CO3溶液
C.先加钡试剂,后加NaOH溶液,再加Na2CO3溶液
(5)为检验精盐纯度,需配制150 mL0.2 mol/LNaCl(精盐)溶液,下图是该同学转移溶液的示意图,
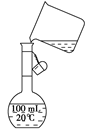
图中的错误是 。
关于该配制过程中,下列说法正确的是________。
A.应称取氯化钠晶体的质量为1.755 g
B.洗涤液不需要转移到容量瓶中
C.定容时,由于同学仰视,将导致所配溶液浓度偏低
D.摇匀后静置,发现液面低于刻度线,应继续加水至凹液面与刻度线相切
高一化学实验题中等难度题查看答案及解析
-
(4分)氯碱工业是以电解食盐水为基础的基本化学工业,电解食盐水同时得到两种气体(气体A是所有气体中密度最小的气体,气体B是制取漂白粉的原料)和一种易溶、易电离的碱。
(1)试写出电解食盐水的化学方程式________(注明反应条件)。
(2)试写出气体B与澄清石灰水反应的离子方程式________。
高一化学填空题中等难度题查看答案及解析
-
氯碱工业是以电解食盐水为基础的基本化学工业,电解食盐水同时得到两种气体(一种是所有气体中密度最小的气体,一种是黄绿色气体)和一种易溶、易电离的碱。
(1)试写出电解食盐水的化学方程式:_______________________________
(2)上述产物彼此之间或与其它物质可以发生有重要工业价值的反应,写出你能想到的其中一个化学方程式________________________________________________________
(3)把Cl2通入NaBr溶液中,并向其中加入少量四氯化碳,振荡后静置,液体分为两层,下层为______色。其中涉及的离子方程式为_____________________________。
高一化学综合题简单题查看答案及解析
-
(8分)氯碱工业上通过电解饱和食盐水可得到氯气和氢气。已知100g 23.4%的饱和食盐水完全电解,问:
(1)生成氯气多少克?
(2)这些氯气中所含的分子数为多少?
(3)这些氯气在标准状况下的体积是多少升?
(4)若反应后溶液的总体积为100ml,则所得NaOH溶液的物质的量浓度是多少mol.L-1?
高一化学计算题简单题查看答案及解析
-
(1)氯碱工业中电解饱和食盐水的原理示意图如下图所示:
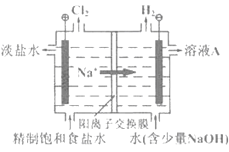
溶液A的溶质名称是__________;电解饱和食盐水的离子方程式为___________。
(2)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2 kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4 kJ/mol
以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_________________。
(3)最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量。根据以上信息和数据,则由N2气体生成1mol气态N4的△H=_____kJ/mol。

(4)以CO为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融Na2CO3。则电池负极电极反应式为_______________;正极的电极反应式为 ____________;放电时,CO32— 移向电池的_______(填“正”或“负”)极。
高一化学综合题中等难度题查看答案及解析
-
(共10分)现有阳离子交换膜、阴离子交换膜、石墨电极,请用氯碱工业中的膜技术原理,回答下列问题。
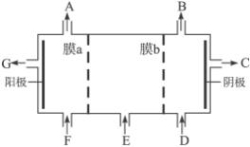
(1)写出氯碱工业中电解饱和食盐水的离子方程式 ;
(2)请利用交换膜技术,根据上图框架,设计一个电解硫酸钠溶液制氢氧化钠溶液和硫酸溶液的装置,标出进出物质的化学式:
A_________;C_________; E_________;膜b为 离子交换膜(填“阳”或“阴”)。
高一化学填空题中等难度题查看答案及解析
-
工业电解饱和食盐水模拟装置的结构如图所示:

(1)写出电解饱和食盐水的化学方程式 ,该工业称为 工业
(2)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.⑤②④③①
(3)在该装置中写出装NaOH溶液试管中所发生的化学反应方程式(并用双线桥表示电子的转移的方向和数目) 。
高一化学填空题中等难度题查看答案及解析