-
(8分)氯碱工业上通过电解饱和食盐水可得到氯气和氢气。已知100g 23.4%的饱和食盐水完全电解,问:
(1)生成氯气多少克?
(2)这些氯气中所含的分子数为多少?
(3)这些氯气在标准状况下的体积是多少升?
(4)若反应后溶液的总体积为100ml,则所得NaOH溶液的物质的量浓度是多少mol.L-1?
高一化学计算题简单题查看答案及解析
-
工业上制取氯气大多采用电解饱和食盐水的方法,以此为基础的工业称为“氯碱工业”,它是化学工业的一个重要支柱.电解饱和食盐水可产生氯气、氢气和氢氧化钠.
(1)若电解饱和食盐水消耗NaCl 117g,计算理论上最多可制得氯气的体积(标准状况).
(2)因氯气有毒,制氯气时需用氢氧化钠溶液来吸收尾气,若将7.1g氯气用氢氧化钠溶液完全吸收,需消耗0.5mol/L NaOH溶液的体积为多少?高一化学解答题中等难度题查看答案及解析
-
(1)氯碱工业中电解饱和食盐水的原理示意图如下图所示:
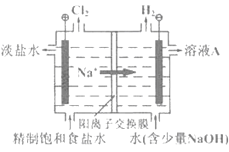
溶液A的溶质名称是__________;电解饱和食盐水的离子方程式为___________。
(2)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2 kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4 kJ/mol
以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_________________。
(3)最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量。根据以上信息和数据,则由N2气体生成1mol气态N4的△H=_____kJ/mol。

(4)以CO为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融Na2CO3。则电池负极电极反应式为_______________;正极的电极反应式为 ____________;放电时,CO32— 移向电池的_______(填“正”或“负”)极。
高一化学综合题中等难度题查看答案及解析
-
关于氯气制取方法的说法中,不正确的是( )
A. 电解饱和食盐水制氯气时,与电源正极相连的石墨棒上方充满黄绿色气体
B. 工业上用电解饱和食盐水的方法制取氯气的同时得到烧碱
C. 实验室制法和电解饱和食盐水的制法的化学方程式是不同的
D. 实验室制取氯气时最好大火加热使温度迅速升高
高一化学单选题简单题查看答案及解析
-
氯碱工业中,通过电解饱和食盐水获得重要的化工原料:氯气、氢气和氢氧化钠.其中氯气用途十分广泛,除用于净水、环境消毒外,还用于生产盐酸、硅、聚氯乙烯、氯苯等.
(1)工业上可用氯气和石灰乳为原料制造漂白粉,漂白粉为________(填“纯净物”或“混合物”),制备漂白粉的化学方程式为________.
(2)工业上生产半导体材料硅的流程如图所示:
①石英砂的主要成分是二氧化硅,在制备粗硅时,焦炭的作用是________.(填“氧化剂”或“还原剂”)
②粗硅与氯气反应后得到沸点较低的液态四氯化硅,其中常混有一些高沸点、难挥发性杂质,必须进行分离提纯.其提纯方法为________.(填字母)
A.蒸馏 B.过滤 C.萃取 D.蒸发
③四氯化硅与氢气在高温条件下反应得到高纯硅和氯化氢气体,写出该反应的化学方程式:________.高一化学填空题中等难度题查看答案及解析
-
氯碱工业中,通过电解饱和食盐水获得重要的化工原料:氯气、氢气和氢氧化钠。其中氯气用途十分广泛,除用于净水、环境消毒外,还用于生产盐酸、硅、聚氯乙烯、氯苯等。
(1)写出工业上制取盐酸的化学反应方程式:________
(2)工业上可用氯气和石灰乳为原料制造漂白粉,写出漂白粉在空气中的漂白原理(用化学方程式表示)________。
(3)工业上生产半导体材料硅的流程如下:

①写出在制备粗硅时反应的化学方程式_____________________________,此反应中焦炭的作用是____________(填“氧化剂”或“还原剂”),若有 0.6mol硅生成,反应中转移电子的物质的量是________mol。
②粗硅与氯气反应后得到沸点较低的液态四氯化硅中常混有一些高沸点,难挥发性杂质,必须进行分离提纯。其提纯方法为____________。(填序号)
A.蒸馏 B.过滤 C.萃取 D.结晶
③由四氯化硅通入氢气得到高纯硅和氯化氢气体,写出该反应的化学方程式:
________________________________________________________________________。
高一化学填空题困难题查看答案及解析
-
下图为教科书中电解饱和食盐水的实验装置。据此,下列叙述不正确的是
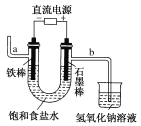
A. 装置中a管能产生氢气
B. b管导出的是氯气
C. 在石墨棒电极区域有NaOH生成
D. 以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”
高一化学单选题简单题查看答案及解析
-
世界上绝大部分卤素都存在于海洋。海水晒盐可以得到粗盐和卤水,对粗盐和卤水进一步加工可以得到氯气、溴以及其他一些重要的化工产品。完成下列填空:
(1)工业上用电解饱和食盐水的方法获取氯气。写出电解饱和食盐水的离子方程式_______。若转移 5mol 电子,生成氯气_______L(标准状况下)。
溴主要以 Br-形式存在于海水中,海水呈弱碱性。工业上制备的 Br2 的操作步骤为:
①一定条件下,将 Cl2 通入浓缩的海水中,生成 Br2
②利用热空气将 Br2 吹出,并用浓 Na2CO3 溶液吸收,生成 NaBr、NaBrO3、CO2
③用硫酸酸化步骤②得到的混合物
(2)先在卤水中加入硫酸酸化,然后再通入氯气,硫酸酸化可以提高氯气的利用率,原因是 _______。
(3)写出步骤②化学方程式 _______。
(4)写出步骤③所发生的化学反应方程式并标出电子转移的方向和数目_______。
(5)用上述方法制得的液溴常溶有少量氯气,除去氯气的方法是_______。
高一化学实验题中等难度题查看答案及解析
-
Ⅰ.工业上常用电解饱和食盐水的方法制备氯气,其装置如图1所示,如果在饱和食盐水中滴加酚酞,通电后________ (填X或Y)极附近溶液变红,写出电解饱和食盐水的化学方程式________.再用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式________.
Ⅱ.请利用图2装置及试剂组装一套装置,其流程是先制取纯净干燥的Cl2(不收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性.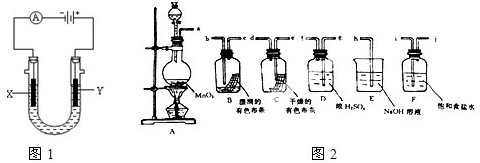
(1)按气体从左向右流向将各装置依次连接起来(填接口标号):a 接________,________接________,________接________,________接________,________接________.
(2)圆底烧瓶中发生反应的化学方程式是________.如果将过量二氧化锰与20mL 12mol•L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol.其主要原因为________.
(3)E装置的作用是________,F装置的作用是________.
(4)装置________(填“B”或“C”)中的有色布条褪色,以上事实说明起漂白作用的物质是________.高一化学填空题中等难度题查看答案及解析
-
如图为教科书中电解饱和食盐水的实验装置。据此,下列叙述不正确的是( )

A.装置中,a管导出的是氢
B.b管导出的是氯气
C.以食盐水为基础原料制取氯气等产品的工业称为“氯碱工业”
D.在石墨棒电极区域有NaOH生成
高一化学选择题简单题查看答案及解析