我国科研人员研制出一种室温Na-CO2电池。该电池吸收CO2的工作原理如图所示。吸收的全部CO2中,有转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法不正确的是
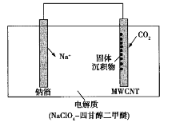
A. 钠箔为负极,发生氧化反应
B. 每吸收22.4 LCO2,转移电子数为mol
C. 正极反应式:4Na++3CO2+4e-=2Na2CO3+C
D. Na+通过电解质移向MWCNT极
高二化学单选题中等难度题
我国科研人员研制出一种室温Na-CO2电池。该电池吸收CO2的工作原理如图所示。吸收的全部CO2中,有转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法不正确的是

A. 钠箔为负极,发生氧化反应
B. 每吸收22.4 LCO2,转移电子数为mol
C. 正极反应式:4Na++3CO2+4e-=2Na2CO3+C
D. Na+通过电解质移向MWCNT极
高二化学单选题中等难度题
我国科研人员研制出一种室温Na-CO2电池。该电池吸收CO2的工作原理如图所示。吸收的全部CO2中,有转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法不正确的是

A. 钠箔为负极,发生氧化反应
B. 每吸收22.4 LCO2,转移电子数为mol
C. 正极反应式:4Na++3CO2+4e-=2Na2CO3+C
D. Na+通过电解质移向MWCNT极
高二化学单选题中等难度题查看答案及解析
2016年我国科研人员研制出一种室温“可呼吸”Na—CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。吸入CO2时,其工作原理如下图所示。吸收的全部CO2中,有2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是
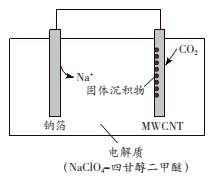
A. “吸入”CO2时,钠箔为正极
B. “呼出”CO2时,Na+向多壁碳纳米管电极移动
C. “吸入”CO2时的正极反应:4Na++3CO2+4e-=2Na2CO3+C
D. 标准状况下,每“呼出”22.4 L CO2,转移电子数为0.75 mol
高二化学单选题简单题查看答案及解析
新型Na-CO2电池工作原理为:4Na+3CO2===2Na2CO3+C,下列说法正确的是
A. Na是氧化剂 B. CO2在反应中失去电子
C. CO2全部被还原 D. 每生成1 molNa2CO3转移2 mol电子
高二化学选择题中等难度题查看答案及解析
全球气候变暖已经成为全世界人类面临的重大问题,研究CO2的利用对促进低碳社会的构建具有重要意义。
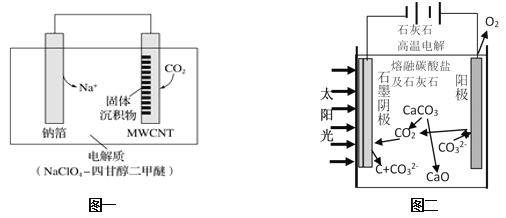
(1)利用“Na﹣CO 2”电池将CO 2变废为宝。我国科研人员研制出的可充电“Na﹣CO 2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2⇌2Na2CO3+C.放电时该电池“吸入”CO 2,其工作原理如图一所示:
①放电时,正极产物全部以固体形式沉积在电极表面,正极的电极反应式为__________________。
②放电时,当转移0.1mol e-时,负极质量减少_____ g。
(2)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图二所示:
①上述生产过程的能量转化方式是____________________________________。
②上述电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极放电的电极反应式为____________________________。
高二化学填空题困难题查看答案及解析
全球气候变暖已经成为全世界人类面临的重大问题,研究CO2的利用对促进低碳社会的构建具有重要意义。

(1)利用“Na﹣CO 2”电池将CO 2变废为宝。我国科研人员研制出的可充电“Na﹣CO 2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2⇌2Na2CO3+C.放电时该电池“吸入”CO 2,其工作原理如图一所示:
①放电时,正极产物全部以固体形式沉积在电极表面,正极的电极反应式为__________________。
②放电时,当转移0.1mol e-时,负极质量减少_____ g。
(2)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图二所示:
①上述生产过程的能量转化方式是____________________________________。
②上述电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极放电的电极反应式为____________________________。
高二化学填空题困难题查看答案及解析
基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂能将工厂排放的CO2以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入Na2CO3溶液,其原理如图所示。

(1)这种微胶囊吸收CO2的原理是_____________(用离子方程式解释),此过程是_______(填“吸收”或“放出”)能量的过程。
(2)在吸收过程中关于胶囊内溶液下列说法正确的是_____________。
a. 吸收前溶液中c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
b. 吸收过程中,体系中所有的含碳微粒是CO32-、HCO3-、H2CO3
c. 当n(CO2):n(Na2CO3)=1:3时,溶液中c(CO32-)<c(HCO3-)
d. 溶液中始终有c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
(3)将吸收的CO2催化加氢可制得乙烯。
已知:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H =-127.8 kJ/mol,如图曲线a表示在体积为2 L的恒容容器中,投料为1 mol CO2和3 mol H2时,测得温度对CO2的平衡转化率的影响,改变投料比测量后得到曲线b。
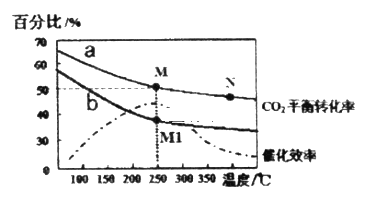
①根据曲线a计算250℃时该反应的化学平衡常数K=_____________(带入数值列出计算式即可)
②b条件下投料比n(H2)/n(CO2)______3(填“>”、“<”或“=”),判断依据是____________________________
③下列说法正确的是_____________。
a. 平衡常数大小:M=M1> N
b. 其他条件不变,b条件时增加催化剂用量,则250℃时CO2的平衡转化率可能达到M
c. 当压强、混合气体的密度或n(H2)/n(CO2)不变时均可视为化学反应已达到平衡状态
d. 工业生产中采取较高温度(250 ℃左右)是为了提高催化剂活性加快反应速率。
高二化学综合题困难题查看答案及解析
我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意如下:则下列说法不正确的是( )
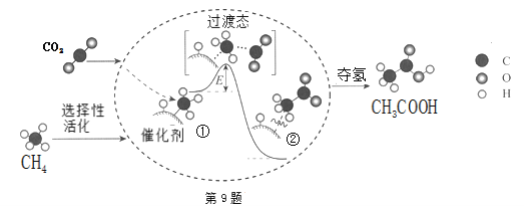
A.生成CH3COOH总反应是化合反应 B.①→②吸收能量
C.CH4→CH3COOH过程中,有C-H键发生断裂 D.①→②过程形成了C-C键
高二化学单选题中等难度题查看答案及解析
我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意如下:则下列说法不正确的是( )
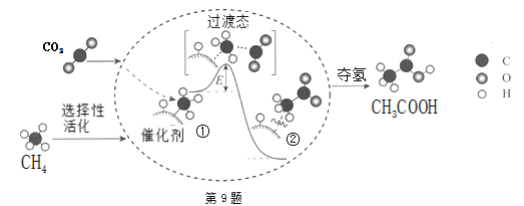
A.生成CH3COOH总反应是化合反应 B.①→②吸收能量
C.CH4→CH3COOH过程中,有C-H键发生断裂 D.①→②过程形成了C-C键
高二化学单选题中等难度题查看答案及解析
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示。下列说法不正确的是
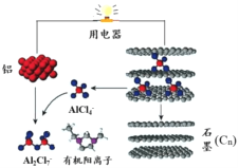
A. 放电时,铝为负极,石墨为正极
B. 放电时的负极反应为:Al-3e-+7AlCl4-===4Al2Cl7-
C. 充电时的阳极反应为:Cx+ AlCl4--e-===CxAlCl4
D. 放电时,有机阳离子向铝电极方向移动
高二化学单选题中等难度题查看答案及解析
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示。下列说法不正确的是
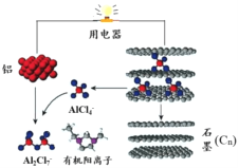
A. 放电时,铝为负极,石墨为正极
B. 放电时的负极反应为:Al-3e-+7AlCl4-===4Al2Cl7-
C. 充电时的阳极反应为:Cx+ AlCl4--e-===CxAlCl4
D. 放电时,有机阳离子向铝电极方向移动
高二化学单选题中等难度题查看答案及解析