-
NaAlH4(四氢铝钠)是有机合成的重要还原剂。某小组以铝合金厂的废边脚料为原料(主要成分为Al,含有少量Al2O3、Fe2O3,MgO和SiO2、等杂质制备四氢铝钠的工艺流程如下:
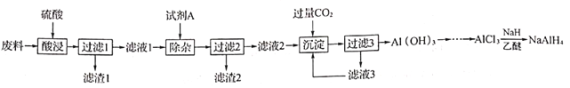
资料显示:NaH、NaAlH4遇水蒸气发生剧烈反应。
请回答下列问题:
(1) NaAlH4中氢元素的化合价为___________。
(2)试剂A中溶质的阴、阳离子所含电子数相等,其电子式为___________。在空气中灼烧滤渣2,得到的固体的主要成分为___________(填化学式)。
(3)滤液3可以循环利用,写出滤液2与滤液3反应的离子方程式:___________。
(4)实验前要保证NaH与AlC13反应的装置干燥,其目的是___________________。
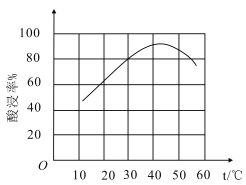
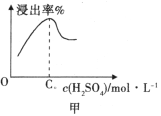
(5)已知废料接触面积、接触时间均相同,“酸浸”中铝元素浸出率与硫酸浓度的关系如图所示。当硫酸浓度大于 C0 mol·L-1时,浸出率降低的原因可能是___________。
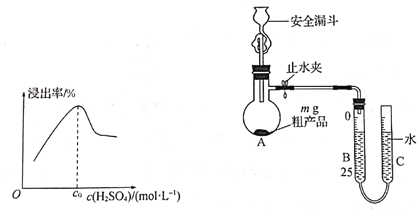
(6)测定NaAlH4粗产品的纯度。
称取 m g NaAlH4粗产品按如图所示装置进行实验,测定产品的纯度。
①“安全漏斗”中“安全”的含义是____________________________________________。
②已知实验前B管读数为xmL,向A中加入足量蒸馏水,当A中反应完全后,冷却至室温B管读数为ymL(均折合成标准状况)。则该产品的纯度为___________(用含m、x和y的代数式表示)。
③若实验前读数时B管和C管液面相平,实验后读数时B管液面低于C管,则测得的结果___________(填“偏高”“偏低”或“无影响”)
-
铝氢化钠(NaAlH4)是重要的还原剂。以铝土矿(主要成分Al2O3,含少量SiO2、Fe2O3等杂质)为原料制备NaAlH4的一种流程如图:
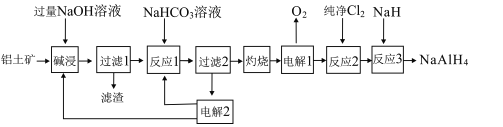
已知:碱浸中SiO2转化成难溶的Na2Al2SixO8
(1)Na2Al2SixO8用氧化物的形式表示为___(x用具体的数值表示)。
(2)过滤1得滤液的主要成分为NaOH和NaAlO2,写出反应1中NaHCO3与NaAlO2反应的离子方程式:___。
(3)电解2生成NaHCO3和NaOH用于循环使用,写出电解2阴极的电极反应式:___。
(4)反应3的化学方程式为___。
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为___。
(6)滤渣主要成分有Na2Al2SixO8和Fe2O3,可以采用如图流程进行分离:
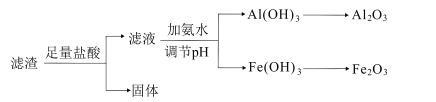
①滤渣溶于盐酸所得的固体物质可能为___(填化学式)。
②滤渣溶于盐酸的“酸浸率”与温度关系如图所示,试解释温度过高,“酸浸率”降低的原因___。
③已知常温下,Ksp[Fe(OH)3]=8.0×10-38,Al3+开始沉淀的pH为4,(溶液中离子的浓度小于1×10-5mol/L为沉淀完全),从滤液中先分离出Fe3+,应调节pH范围为___(lg2≈0.3)。
-
四氢铝锂(LiAlH4)常作有机合成的重要还原剂。以辉锂矿(主要成分是Li2O·Al2O3·4SiO2,含少量Fe2O3)为原料合成四氢铝锂的流程如下:
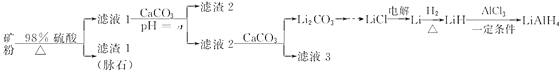
已知:①几种金属氢氧化物沉淀的pH如下表所示:
| 物质 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀的pH | 2.3 | 4.0 |
| 完全沉淀的pH | 3.7 | 6.5 |
②常温下,Ksp(Li2CO3)=2.0×10-3,Li2CO3在水中溶解度随着温度升高而减小。
回答下列问题:
(1)上述流程中,提高“酸浸”速率的措施有______________________________________、______________________________________________________________________________(写两条);加入CaCO3的作用是__________________,“a”的最小值为___________。
(2)设计简单方案由Li2CO3制备LiCl:__________。
(3)写出LiH和AlCl3反应的化学方程式为______________________(条件不作要求)。
(4)用热水洗涤Li2CO3固体,而不用冷水洗涤,其目的是________________;检验碳酸锂是否洗净的实验方法是_____________________。
(5)在有机合成中,还原剂的还原能力通常用“有效氢”表示,其含义是1克还原剂相当于多少克氢气的还原能力。LiAlH4的“有效氢”为_________________(结果保留2位小数)。
-
四氢铝锂(LiAlH4)常作有机合成的重要还原剂。以辉锂矿(主要成分是Li2O·Al2O3·4SiO2,含少量Fe2O3)为原料合成四氢铝锂的流程如下:

已知:①几种金属氢氧化物沉淀的pH如下表所示:
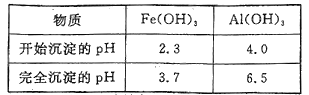
②常温下,Ksp(Li2CO3)=2.0×10-3。Li2CO3在水中溶解度随着温度升高而减小。
回答下列问题:
(1)上述流程中,提高“酸浸”速率的措施有_________(写两条);加入CaCO3的作用是________,“a”的最小值为___________。
(2)设计简单方案由Li2CO3制备LiCl:______。
(3)写出LiH和AlCl3反应的化学方程式:____________(条件不作要求)
(4)用热水洗涤Li2CO3固体,而不用冷水洗涤,其目的是____________;检验碳酸锂是否洗净的实验方法是_______________。
(5)在有机合成中,还原剂的还原能力通常用“有效氢”表示,其含义是1克还原剂相当于多少克氢气的还原能力。LiAlH4的“有效氢”为___________。(结果保留2位小数)
-
工业上常用铝土矿(主要成分为Al2O3,SiO2和Fe2O3等杂质)为原料制备铝氢化钠,铝氢化钠(NaAlH4)是有机合成的重要还原剂,工艺流程如下:
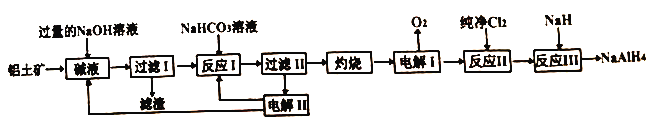 已知:SiO2在“碱液”中转化为铝硅酸钠Na2Al2SixO8)沉淀。
已知:SiO2在“碱液”中转化为铝硅酸钠Na2Al2SixO8)沉淀。
(1)过量NaOH溶液溶解铝土矿时为了提高浸出率可采取的措施是_______。(任写一种)
(2)电解I的化学方程式_______。
(3)“灼烧”操作用到的主要仪器有_______、_______、三脚架、玻璃棒、酒精灯、坩埚钳。
(4)“电解II”是电解Na2CO3溶液,原理如图所示。
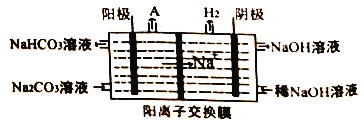
物质A为_______。(填化学式)
(5)反应III的化学方程式为_______,某同学经过分析认为可以再设计一个电解槽,电解_______ (填物质名称)溶液,更能实现副产物的循环利用。
(6)某同学认为该制备工艺也可以先酸溶,再加入NaOH溶液,当溶液中铁离子沉淀完全时,此时溶液pH是_______。(一般认为室温下离子浓度小于10-5mol/L时沉淀完全;Ksp[Fe(OH)3]=1×10-35,Ksp[Al(OH)3]=3×10-34)
-
铝氢化钠(NaAlH4) 是有机合成的重要还原剂。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质) 为原料制备铝氢化钠的一种工艺流程如下:
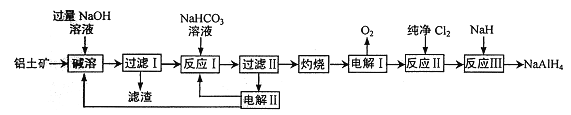
注: SiO2在“碱溶”时转化为铝硅酸钠(Na2Al2SixO8) 沉淀。
(1)铝硅酸钠(Na2Al2SixO8) 可以用氧化物的形式表示其组成,形式为________。
(2) “过滤I”中滤渣主要成分有________(写名称)。向“过滤I”所得滤液中加入NaHCO3溶液,反应的离子方程式为_______________、______________。
(3) “电解I”的另一产物在1000℃时可与N2反应制备AlN,在这种产物中添加少量NH4Cl固体并充分混合,有利于AlN 的制备,其主要原因是__________________。
(4)“电解II”是电解Na2CO3溶液,原理如图所示。
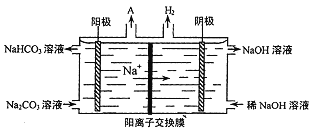
阳极的电极反应式为_________________。
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为_____________,每产生1mol 气体转移电子数为______。
-
铝氢化钠(NaAlH4) 是有机合成的重要还原剂。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质) 为原料制备铝氢化钠的一种工艺流程如下:
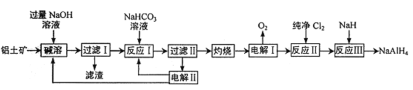
注: SiO2在“碱溶”时转化为铝硅酸钠(Na2Al2SixO8) 沉淀。
(1)铝硅酸钠(Na2Al2SixO8) 可以用氧化物的形式表示其组成,形式为________。
(2) “过滤I”中滤渣主要成分有________(写名称)。向“过滤I”所得滤液中加入NaHCO3溶液,反应的离子方程式为_______________、______________。
(3)“电解I”的另一产物在1000℃时可与N2反应制备AlN,在这种产物中添加少量NH4Cl固体并充分混合,有利于AlN 的制备,其主要原因是__________________。
(4)“电解II”是电解Na2CO3溶液,原理如图所示。
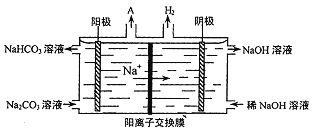
阳极的电极反应式为_________________。
-
铝氢化钠( NaAlH4)是有机合成的重要还原剂。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝氢化钠的一种工艺流程如下图所示:
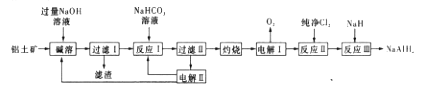
注:SiO2在“碱溶”时转化为铝硅酸钠(Na2Al2SixO8)沉淀。
(1)铝硅酸钠(Na2 Al2SixO4)可以用氧化物的形式表示其组成,形式为_______。
(2)“过滤I”中滤渣的主要成分有_______(填名称)。向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,发生反应的离子方程式为OH-+HCO3—===CO32—+H2O、__________________________。
(3)“电解I”的另一产物在1000℃时可与N2反应制备AIN,在这种产物中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是___________。
(4)“电解Ⅱ”是电解Na2CO3溶液,其原理如图所示。
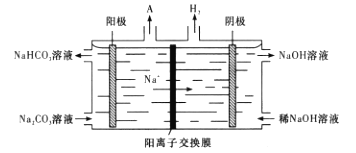
阳极的电极反应式为____________。已知F=96500C/mol,当I=0.5A时,通电80min,理论上阴极获得H2(标准状况下)的体积为_____L(结果保留两位有效数字)。
(5)铝氢化钠遇水发生剧烈反应,且反应产生大量气泡,其反应的化学方程式为_____________________________________。
-
SAH(NaAlH4)还原性非常强。纯的四氢铝钠是白色晶状固体,在干燥空气中相对稳定,遇水发生剧烈反应。以铝合金废边脚料为原料(含有少量Al2O3、Fe2O3、MgO、PbO和SiO2等杂质)制备四氢铝钠:
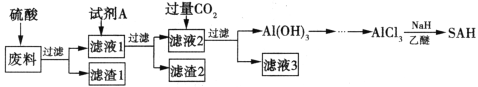
请回答下列问题:
(1)滤渣1的主要成分为__________________(填化学式)。试剂A中溶质的阴、阳离子所含电子数相等,其电子式为_________________________。
(2)已知废料接触面积、接触时间均相同,“酸浸”中铝元素浸出率与硫酸浓度的关系如图甲所示。当硫酸浓度大于C0 mol·L-1时,浸出率降低的原因可能是__________________。
(3)滤液3可以循环利用,写出滤液2与滤液3反应的离子方程式____________________________________。
(4)NaAlH4与水反应的化学方程式为____________________。
(5)测定NaAlH4粗产品的纯度。
称取m g NaAlH4粗产品按如图乙所示装置进行实验,测定产品的纯度。
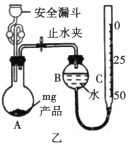
①“安全漏斗”中“安全”的含义是____________________。
②已知实验前C管读数为V1mL,向A中加入适量蒸馏水使NaAlH4完全反应,当A中反应完全后,冷却至室温后C管读数为V2mL(均折合成标准状况)。则该产品的纯度为____________________(用含m、V1和V2的代数式表示,忽略加入蒸馏水的体积)。
③若实验前读数时B中液面和C管液面相平,实验后读数时B中液面低于C管,则测得的结果_____________(填“偏高”“偏低”或“无影响”)。
-
四氯化钛是制取海绵钛和氯化法钛白(二氧化钛)的主要原料,用于制造颜料和钛有机化合物以及国防上用的烟幕剂。同时也是制取航天航空工业材料——钛合金的重要原料,由钛铁矿(主要成分是FeTiO3,含有少量Fe2O3、SiO2、Al2O3等杂质),制备TiCl4等产品的一种工艺流程如下:
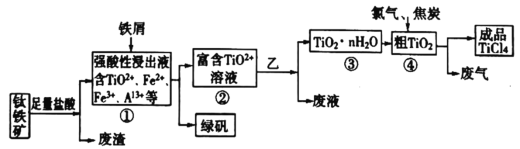
已知:
Ⅰ.①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe===3Fe2+、2TiO2+(无色)+Fe+4H+===2Ti3+(紫色)+Fe2++2H2O、Ti3+(紫色)+ Fe3++ H2O===2TiO2+(无色)+ Fe2++2H+;
Ⅱ.四氯化钛的熔点-25.0℃,沸点136.4℃,SiCl4的熔点-68.8℃,沸点57.6℃。
回答下列问题:
(1)用盐酸酸浸时,为使酸浸速率加快,可采取的措施是:________________(至少写2条),发生主要反应的离子方程式为:___________。
(2)废渣的成分是_______。
(3)如何检验富含TiO2+溶液中是否还含铁元素_____________。
(4)若将制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,该温度下反应 的平衡常数K=____。
的平衡常数K=____。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是_______(只要求写出一项)。
(6)要精制含少量SiCl4杂质的TiCl4,可采用的方法是_______。
(7)用TiCl4水解生成TiO2·nH2O,经过滤、水洗除去其中的Clˉ,再烘干、焙烧除去水分得到粉体TiO2.写出TiCl4水解生成TiO2·nH2O的化学方程式__________________。








 已知:SiO2在“碱液”中转化为铝硅酸钠Na2Al2SixO8)沉淀。
已知:SiO2在“碱液”中转化为铝硅酸钠Na2Al2SixO8)沉淀。









