-
用化学反应原理研究N、S氧化物有着重要的意义。
(1)已知:
2SO2(g)+O2(g)  2SO3(g)ΔH1=-196.6kJ/mol
2SO3(g)ΔH1=-196.6kJ/mol
2NO(g)+O2(g)  2NO2(g)ΔH2=-113.8kJ/mol
2NO2(g)ΔH2=-113.8kJ/mol
NO2(g)+SO2(g) SO3(g)+NO(g)ΔH3
SO3(g)+NO(g)ΔH3
则ΔH3=________,如果上述三个反应方程式的平衡常数分别为K1、K2、K3,则K3=________(用K1、K2表示)。
(2)如下图所示,A是恒容的密闭容器,B是一个体积可变的充气气囊。保持恒温,关闭K2,分别将2 mol NO和1 mol O2通过K1、K3分别充入A、B中,发生的反应为2NO(g)+O2(g) 2NO2(g)[不考虑2NO2(g)
2NO2(g)[不考虑2NO2(g) N2O4(g)],起始时A、B的体积相同均为a L。
N2O4(g)],起始时A、B的体积相同均为a L。
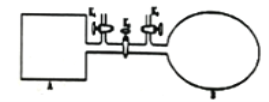
①下列说法和示意图能说明A、B容器均达到平衡状态的是________。
a.A、B容器中气体的颜色均不发生变化
b.A、B容器中NO和O2物质的量浓度比均为2∶1
c.A、B容器中气体的密度不在发生变化
d.A、B容器中气体的平均摩尔质量不再发生变化
e.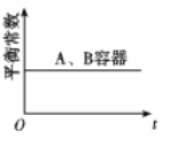
②T ℃时,A容器中反应达到平衡时的平衡常数Kp=0.27(kPa)-1。若A容器中反应达到平衡时p(NO2)=200 kPa,则平衡时NO的转化率为________。(Kp是用平衡分压代替平衡浓度计算所得的平衡常数,分压=总压×物质的量分数)
(3)将0.2 mol SO2和0.15 mol O2通入2 L的密闭容器中,测得SO2的物质的量随时间变化如下图实线所示。
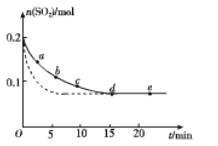
①ab段平均反应速率______________(填“大于”“小于”或“等于”)bc段平均反应速率;de段平均反应速率为________。
②仅改变某一个实验条件,测得SO2的物质的量随时间变化如上图中虚线所示,则改变的条件是________。
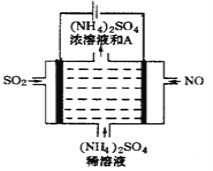
③如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。阴极的电极反应式是_______________。
-
雾霾天气给人们的出行带来了极大的不便,因此研究NO2、SO2等大气污染物的处理具有重要意义。
(1)某温度下,已知:
①2SO2(g)+O2(g) 2SO3(g) △H1=-196.6kJ/mol
2SO3(g) △H1=-196.6kJ/mol
②2NO(g)+O2(g) 2NO2(g)△H2
2NO2(g)△H2
③NO2(g)+SO2(g) SO3(g)+NO(g) △H3=-41.8kJ/mol
SO3(g)+NO(g) △H3=-41.8kJ/mol
则△H2= _____________。
(2)按投料比2:1把SO2和O2加入到一密闭容器中发生反应2SO2(g)+O2(g) 2SO3(g) ,测得平衡时SO2的转化率与温度T、压强p的关系如图甲所示:
2SO3(g) ,测得平衡时SO2的转化率与温度T、压强p的关系如图甲所示:
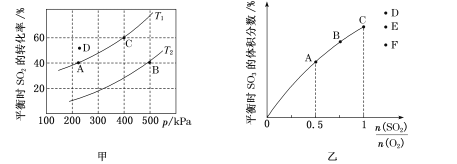
①A、B两点对应的平衡常数大小关系为KA __________(填“>”“<”或“=”,下同)KB;温度为T,时D点vD正与vD逆的大小关系为vD正 _____________vD逆;
②T1温度下平衡常数Kp=______________ kPa-1(Kp为以分压表示的平衡常数,结果保留分数形式)。
(3)恒温恒容下,对于反应2SO2(g)+O2(g) 2SO3(g),测得平衡时SO3的体积分数与起始
2SO3(g),测得平衡时SO3的体积分数与起始 的关系如图乙所示,则当
的关系如图乙所示,则当 =1.5达到平衡状态时,SO2的体积分数是图乙中D、E、F三点中的____________点。A、B两点SO2转化率的大小关系为aA ___(填“>”“<”或“=”)aB。
=1.5达到平衡状态时,SO2的体积分数是图乙中D、E、F三点中的____________点。A、B两点SO2转化率的大小关系为aA ___(填“>”“<”或“=”)aB。
(4)工业上脱硫脱硝还可采用电化学法,其中的一种方法是内电池模式(直接法),烟气中的组分直接在电池液中被吸收及在电极反应中被转化,采用内电池模式将SO2吸收在电池液中,并在电极反应中氧化为硫酸,在此反应过程中可得到质量分数为40%的硫酸。写出通入SO2电极的反应式:____________;若40%的硫酸溶液吸收氨气获得(NH4)2SO4的稀溶液,测得常温下,该溶液的pH=5,则 ___________(计算结果保留一位小数,已知该温度下NH3·H2O的Kb=1.7×10-5);若将该溶液蒸发掉一部分水后恢复室温,则
___________(计算结果保留一位小数,已知该温度下NH3·H2O的Kb=1.7×10-5);若将该溶液蒸发掉一部分水后恢复室温,则 的值将_____(填“变大”“不变”或“变小”)。
的值将_____(填“变大”“不变”或“变小”)。
-
用化学反应原理研究氮的氧化物和硫的氧化物有着重要的意义。
(1)已知:2SO2(g)+ O2(g)  2SO3(g) △H1
2SO3(g) △H1
2NO(g)+ O2(g)  2NO2 (g) △H2
2NO2 (g) △H2
NO2 (g) + SO2(g)  SO3(g) + NO(g) △H3
SO3(g) + NO(g) △H3
则△H3 = (用△H1、△H2 表示),如果上述三个反应方程式的平衡常数分别为K1、 K2、K3,则K3 = (用K1、K2 表示)。
(2)如图所示,A 是恒容的密闭容器,B 是一个体积可变的充气气囊。保持恒温,关闭K2,分别将2mol NO 和1 mol O2 通过K1、K3 分别充入A、B 中,发生的反应为2NO(g)+ O2(g) 2NO2 (g) [不考虑2NO2 (g)
2NO2 (g) [不考虑2NO2 (g)  N2 O4 (g) ],起始时A、B 的体积相同均为a L。
N2 O4 (g) ],起始时A、B 的体积相同均为a L。
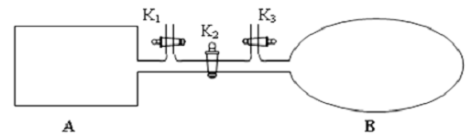
①下列说法和示意图正确,且既能说明A 容器中反应达到平衡状态,又能说明B 容器中反应达到平衡状态的是 。
a. A、B 容器中气体的颜色均不再发生变化
b. A、B 容器中NO 和O2物质的量浓度比均为2:1

② T℃时,A 容器中反应达到平衡时的平衡常数Kp = 8×10﹣2 (kPa) ﹣1 。若A 容器中反应达到平衡时p(NO2) = 200kPa,则平衡时NO的转化率为 。(Kp 是用平衡分压代替平衡浓度计算所得平衡常数,分压=总压×物质的量分数)
(3)将0.2 mol SO2 和0.15 mol O2通入2L 的密闭容器中,测得SO2的物质的量随时间变化如 图实线 所示。
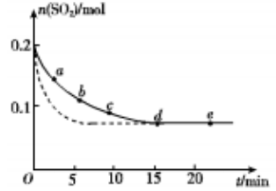
| 编号 | a | b | c | d | e |
| n(SO2)/mol | 0.16 | 0.12 | 0.09 | 0.07 | 0.07 |
| t/min | 2 | 5 | 8 | 15 | 22 |
①ab 段平均反应速率 (填“大于”“小于”或“等于”)bc 段平均反应速率:de 段平均反应速率为 。
②仅改变某一个实验条件,测得SO2 的物质的量随时间变化如图中虚线所示,则改变的条件是 。
-
用化学反应原理研究氮的氧化物和硫的氧化物有着重要的意义。
(1)已知:2SO2(g)+ O2(g) 2SO3(g) △H1
2SO3(g) △H1
2NO(g)+ O2(g) 2NO2 (g) △H2
2NO2 (g) △H2
NO2 (g) + SO2(g) SO3(g) + NO(g) △H3
SO3(g) + NO(g) △H3
则△H3 =__________(用△H1、△H2表示),如果上述三个反应方程式的平衡常数分别为K1、 K2、K3,则K3 =__________(用K1、K2表示)。
(2)如图所示,A 是恒容的密闭容器,B 是一个体积可变的充气气囊。保持恒温,关闭K2,分别将2mol NO 和1 mol O2通过K1、K3分别充入A、B 中,发生的反应为2NO(g)+ O2(g) 2NO2 (g) [不考虑2NO2 (g)
2NO2 (g) [不考虑2NO2 (g) N2 O4 (g) ],起始时A、B 的体积相同均为a L。
N2 O4 (g) ],起始时A、B 的体积相同均为a L。
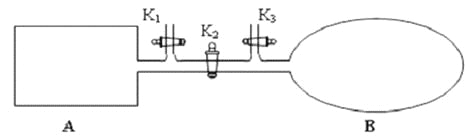
①下列说法和示意图正确,且既能说明A 容器中反应达到平衡状态,又能说明B 容器中反应达到平衡状态的是_________。
a. A、B 容器中气体的颜色均不再发生变化
b. A、B 容器中NO 和O2物质的量浓度比均为2:1

② T℃时,A 容器中反应达到平衡时的平衡常数Kp = 8×10﹣2 (kPa)﹣1。若A 容器中反应达到平衡时p(NO2) = 200kPa,则平衡时NO的转化率为_____________。(Kp 是用平衡分压代替平衡浓度计算所得平衡常数,分压=总压×物质的量分数)
(3)将0.2 mol SO2和0.15 mol O2通入2L 的密闭容器中,测得SO2的物质的量随时间变化如 图实线 所示。
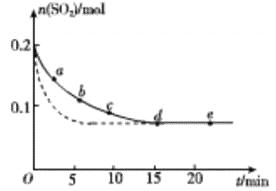
| 编号 | a | b | c | d | e |
| n(SO2)/mol | 0.16 | 0.12 | 0.09 | 0.07 | 0.07 |
| t/min | 2 | 5 | 8 | 15 | 22 |
①ab 段平均反应速率____________(填“大于”“小于”或“等于”)bc 段平均反应速率:de 段平均反应速率为_________________。
②仅改变某一个实验条件,测得SO2的物质的量随时间变化如图中虚线所示,则改变的条件是__________。
-
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol—1,2NO(g)+O2(g)
2SO3(g) ΔH=-196.6 kJ·mol—1,2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol—1,则反应:NO2(g)+SO2(g)
2NO2(g) ΔH=-113.0 kJ·mol—1,则反应:NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol—1
SO3(g)+NO(g)的ΔH= kJ·mol—1
(2)利用反应6NO2+ 8NH3  7N2+12H2O可处理NO2。一定条件下,将该反应设计成如右图所示装置,其中电极均为石墨,使用熔融金属氧化物作电解质,写出负极电极反应式 ;若一段时间内测得外电路中有1.2mol电子通过,则两极共产生的气体产物在标准状况下的体积为 L。
7N2+12H2O可处理NO2。一定条件下,将该反应设计成如右图所示装置,其中电极均为石墨,使用熔融金属氧化物作电解质,写出负极电极反应式 ;若一段时间内测得外电路中有1.2mol电子通过,则两极共产生的气体产物在标准状况下的体积为 L。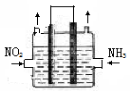
(3)一定条件下,将NO2与SO2以体积比1︰2置于恒容密闭容器中发生下述反应:NO2(g)+SO2(g) SO3(g)+NO(g),下列能说明该反应达到平衡状态的是 。
SO3(g)+NO(g),下列能说明该反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的物质的量比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
(4)CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g) CH3OH(g)。一定温度下,向容积为2L的密闭容器中充入2molCO和2molH2发生上述
CH3OH(g)。一定温度下,向容积为2L的密闭容器中充入2molCO和2molH2发生上述 反应,5min后反应平衡,此时测得CH3OH的浓度为0.3mol/L,计算反应开始至平衡时的平均速率v(H2)= ;该温度下反应的平衡常数为 (保留两位小数)。
反应,5min后反应平衡,此时测得CH3OH的浓度为0.3mol/L,计算反应开始至平衡时的平均速率v(H2)= ;该温度下反应的平衡常数为 (保留两位小数)。
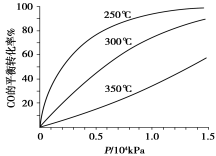
(5)不同温度CO的平衡转化率与压强的关系如上图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
-
(14分)氮及其化合物的转化是资源利用和环境保护的重要研究课题,下面是氮的氧化物的几种不同情况下的转化。
(1)已知:2SO2(g)+ O2 (g) 2SO3 (g) △H =-196.6kJ·mol-1
2SO3 (g) △H =-196.6kJ·mol-1
2NO(g)+ O2 (g)  2NO2 (g) △H =-113.0kJ·mol-1
2NO2 (g) △H =-113.0kJ·mol-1
则SO2气体与NO2气体反应生成SO3气体和NO气体的反应为 (填“放热”或“吸热”)反应。
(2)向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g) SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。
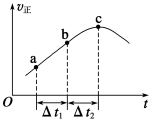
①反应在c点 (填“达到”或“未到”)平衡状态。
②开始时,在该容器中加入:
I:1molSO2(g)和1molNO2(g);
II:1molSO3(g)和1mol NO(g),
则达化学平衡时,该反应的平衡常数I II(填“>”、“=”或“<”)。
(3)用氢氧化钠溶液吸收氮的氧化物时发生下列反应:
2NaOH + NO + NO2 = 2NaNO2 + H2O
2NaOH + 2NO2 = NaNO2 + NaNO2 + H2O
将反应混合液和氢氧化钠溶液分别加到下图所示的电解槽中进行电解,A室产生了N2。

①电极Ⅰ是 极,B室产生的气体是 。
②A室NO2-发生的电极反应是 。
(4)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。现有NO、NO2的混合气6 L,可用同温同压下7 L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为 。
-
氮及其化合物的转化是资源利用和环境保护的重要研究课题,下面是氮的氧化物的几种不同情况下的转化.

(1)已知:2SO2(g)+O2 (g)⇌2SO3 (g)△H=﹣196.6kJ•mol﹣1
2NO(g)+O2 (g)⇌2NO2 (g)△H=﹣113.0kJ•mol﹣1则SO2气体与NO2气体反应生成SO3气体和NO气体的反应为 (填“放热”或“吸热”)反应.
(2)向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)⇌SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图1所示.
①反应在c点 (填“达到”或“未到”)平衡状态.
②开始时,在该容器中加入:
Ⅰ:1molSO2(g)和1molNO2(g);II:1molSO3(g)和1mol NO(g),则达化学平衡时,该反应的平衡常数Ⅰ Ⅱ(填“>”、“=”或“<”).
(3)用氢氧化钠溶液吸收氮的氧化物时发生下列反应:
2NaOH+NO+NO2=2NaNO2+H2O
2NaOH+2NO2=NaNO2+NaNO2+H2O
将反应混合液和氢氧化钠溶液分别加到如图2所示的电解槽中进行电解,A室产生了N2.
①电极Ⅰ是 极,B室产生的气体是 .
②A室NO2﹣发生的电极反应是 ;
(4)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.现有NO、NO2的混合气6L,可用同温同压下7L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为 .
-
氮和硫及其化合物的转化是资源利用和环境保护的重要研究课题。
(1)已知反应I: 2SO2(g)+O2(g) 2SO3(g),△H=-196.6kJ·mol-1
2SO3(g),△H=-196.6kJ·mol-1
反应II: 2NO(g)+O2(g) 2NO2(g),△H=-113.0kJ·mol-1
2NO2(g),△H=-113.0kJ·mol-1
则SO2(g)与NO2(g)反应生成SO3(g)和NO(g)的热反应方程式为________。
(2)①若在绝热恒容密闭容器中通入一定量的SO2和O2,一定条件下发生反应I,一段时间内,正反应速率随时间变化曲线如右图所示,则在a点时,反应______(填“达到”或“未达到”)平衡状态;t1~t3时间内,v正先增大后减小的主要原因是___________。
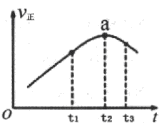
②若在两个相同绝热恒容密闭容器中分别加入A:2molSO2(g)和1molO2(g);B:2molSO3(g),其它条件相同,发生反应I,达到平衡时,则该反应的平衡常数:A _____B(填“>”、“=”、“< ” )。
(3)已知常温下,H2S的电离常数:K1=1.3×10-7, K2=7.1×10-15,则0.lmol/LH2S溶液的pH约为_______(取近似整数值);向浓度均为0.001mol·l-1的AgNO3和Hg(NO3)2混合溶液中通入H2S气体,开始生成沉淀的c(S2-)为_______。(已知:Ksp(Ag2S)=6.3×10-50,Ksp(HgS)=1.6×10-52)
(4)NH3催化还原氮氧物技术(SCR)是目前应用广泛的烟气氮氧化物脱除技术。现有NO、NO2的混合气6L,可用同温同压下7L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为________。
-
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)⇌2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
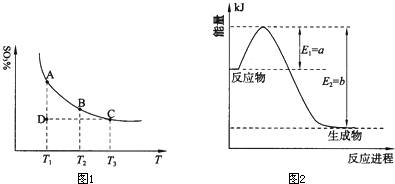
①2SO2(g)+O2(g)⇌2SO3(g)的△H______0(填“>”或“<”);若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡______移动(填“向左”、“向右”或“不”);
②若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1______K2;若反应进行到状态D时,v正______v逆(填“>”、“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
①右图是一定的温度和压强下是N2和H2反应生成1molNH3过程中能量变化示意图,请写出工业合成氨的热化学反应方程式:______.(△H的数值用含字母a、b的代数式表示)
②氨气溶于水得到氨水.在25℃下,将a mol•L-1的氨水与b mol•L-1的盐酸等体积混合,反应后溶液中显中性,则c(NH+4)______c(Cl-)(填“>”、“<”或“=”);用含a和b的代数式表示出氨水的电离平衡常数表达式______.
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在.在25℃下,向0.1mol•L-1的NaCl溶液中逐滴加入适量的0.1mol•L-1硝酸银溶液,有白色沉淀生成.从沉淀溶解平衡的角度解释产生沉淀的原因是______,向反应后的浊液中,继续加入0.1mol•L-1的NaI溶液,看到的现象是______,产生该现象的原因是(用离子方程式表示)______.
-
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)⇌2SO3(g),混合体系中SO3的质量分数和温度的关系如图1所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
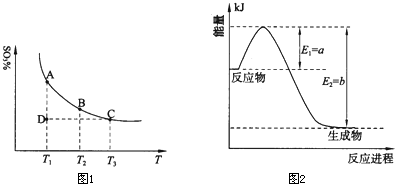
①2SO2(g)+O2(g)⇌2SO3(g)的△H______0(选填“>”或“<”);若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡______移动(选填“向左”、“向右”或“不”);
②若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1______K2;若反应进行到状态D时,v正______v逆(选填“>”、“<”或“=”).
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
①图2是一定的温度和压强下N2和H2反应生成1mol NH3过程中能量变化示意图,请写出合成氨的热化学反应方程式:______、______.(△H的数值用含字母a、b的代数式表示,不必注明反应条件)
②氨气溶于水得到氨水.在25℃下,将xmol•L-1的氨水与ymol•L-1的盐酸等体积混合,所得溶液呈中性.则x______y,所得溶液中c(NH4+)______C(Cl-)(选填“>”、“<”或“=”);用含x和y的代数式表示出一水合氨的电离平衡常数______.
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在.在25℃下,向0.1mol•L-1的NaCl溶液中逐滴加入适量的0.1mol•L-1硝酸银溶液,有白色沉淀生成,向反应后的浊液中,继续加入0.1mol•L-1的NaI溶液,看到的现象是______,产生该现象的原因是(用离子方程式表示)______.
2SO3(g)ΔH1=-196.6kJ/mol
2NO2(g)ΔH2=-113.8kJ/mol
SO3(g)+NO(g)ΔH3
2NO2(g)[不考虑2NO2(g)
N2O4(g)],起始时A、B的体积相同均为a L。


















