以粉煤灰(主要含Al2O3、SiO2,还有少量的Fe2O3)为原料制取Al2O3的流程如下:
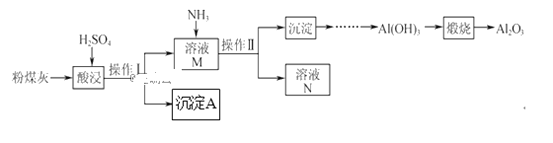
(1)操作Ⅰ的名称是__。
(2)用H2SO4“酸浸”时的离子方程式为__(任写一个)。
(3)简述如何检验酸浸后溶液中是否有Fe3+__。
(4)“煅烧”时的化学方程式为__。
(5)沉淀A与氢氟酸反应的化学方程式为__。
高一化学工业流程中等难度题
以粉煤灰(主要含Al2O3、SiO2,还有少量的Fe2O3)为原料制取Al2O3的流程如下:

(1)操作Ⅰ的名称是__。
(2)用H2SO4“酸浸”时的离子方程式为__(任写一个)。
(3)简述如何检验酸浸后溶液中是否有Fe3+__。
(4)“煅烧”时的化学方程式为__。
(5)沉淀A与氢氟酸反应的化学方程式为__。
高一化学工业流程中等难度题
以粉煤灰(主要含Al2O3、SiO2,还有少量的Fe2O3)为原料制取Al2O3的流程如下:
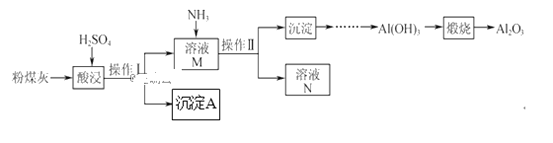
(1)操作Ⅰ的名称是__。
(2)用H2SO4“酸浸”时的离子方程式为__(任写一个)。
(3)简述如何检验酸浸后溶液中是否有Fe3+__。
(4)“煅烧”时的化学方程式为__。
(5)沉淀A与氢氟酸反应的化学方程式为__。
高一化学工业流程中等难度题查看答案及解析
以粉煤灰(主要含Al2O3、SiO2,还有少量的Fe2O3)为原料制取Al2O3的流程如下:

(1)操作Ⅰ的名称是__。
(2)用H2SO4“酸浸”时的离子方程式为__(任写一个)。
(3)简述如何检验酸浸后溶液中是否有Fe3+__。
(4)“煅烧”时的化学方程式为__。
(5)沉淀A与氢氟酸反应的化学方程式为__。
高一化学工业流程中等难度题查看答案及解析
某化学兴趣小组用铁矿石(主要成分为Fe2O3 ,还有较多的SiO2 、Al2O3 及少量的不溶于酸的杂质)提取Fe2O3 。操作过程如下:
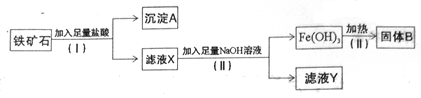
(1)(Ⅰ)和(Ⅱ)步骤中分离溶液和沉淀的操作名称是 ;
(2)写出沉淀A中含量最多的物质与NaOH溶液反应的离子方程式: ;
(3)取少量滤液X于试管中滴入几滴KSCN溶液可观察到溶液变成 色。反应的离子方程式为: ,滤液Y中的阴离子有 种;
(4)写出(Ⅱ)步骤中生成Fe(OH)3 的离子方程式 ;
高一化学填空题困难题查看答案及解析
以冶铝的废弃物铝灰为原料制取超细α氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:

(1)写出铝灰与氢氧化钠溶液反应涉及的化学方程式:_____________________。
(2)图中“滤渣”的主要成分为_______________(填化学式)。
(3)加30%H2O2溶液发生的离子反应方程式为________________。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O] 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
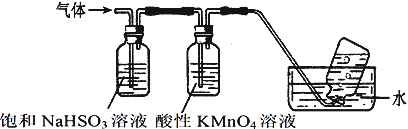
①集气瓶中收集到的气体是___________(填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有____________(填化学式)。
③酸性KMnO4溶液紫色变浅_________(填“能”或“不能”)说明煅烧硫酸铝铵晶体产物中含有SO2气体?理由:_________________________________________________________________。
高一化学综合题中等难度题查看答案及解析
以冶铝的废弃物铝灰为原料制取超细α氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下图:
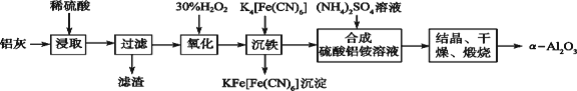
(1)写出铝灰与氢氧化钠溶液反应涉及的化学方程式:_______________________。
(2)加30%H2O2溶液发生的离子反应方程式为______________________________。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
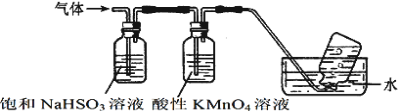
集气瓶中收集到的气体是_______(填化学式)。
②酸性KMnO4溶液紫色变浅_______(填“能”或“不能”)说明煅烧硫酸铝铵晶体产物中含有SO2气体?理由:______。
高一化学实验题中等难度题查看答案及解析
某铝土矿主要含Al2O3和SiO2。某课题组以此为原料回收氧化铝,设计实验流程如下:
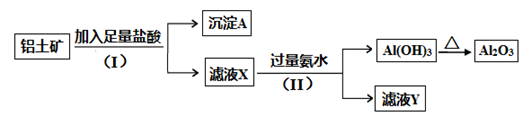
(1)步骤(I)中分离溶液和沉淀的操作名称是 。
(2)沉淀A中一定含有 (用化学式表示),该物质属于 (填“酸性”或“碱性”)氧化物。
(3)写出步骤(Ⅱ)中生成Al(OH)3的离子方程式 。
(4)实验室里用Na[Al(OH)4]溶液制取Al(OH)3最好选用 (填序号)。
A.NaOH溶液 B.稀硫酸 C.二氧化碳
(5)取5.4g铝土矿进行实验,最后得到氧化铝5.1g,则该铝土矿中铝的含量为__________(假设实验过程没有损失)。
高一化学实验题困难题查看答案及解析
以冶铝的废弃物铝灰为原料制取超细a-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程图如下:
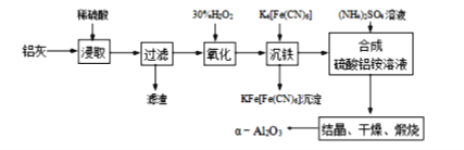
(1)铝灰中氧化铝与硫酸反应的化学方程式为_______。
(2)加30%的H2O2作用为将Fe2+氧化为Fe3+,其发生的离子反应方程式为__________。该反应需控制温度低于40℃,其目的是_____________。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]=2Al2O3+2NH3↑+5SO3↑+3SO2↑+N2↑+53H2O,将产生的气体通过如图所示的装置。

①足量饱和NaHSO3溶液吸收的物质除大部分H2O外还有________(填化学式)。集气瓶中收集到的气体是_______。
②KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子方程式为_____________。
高一化学实验题中等难度题查看答案及解析
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体的工艺流程如图所示:
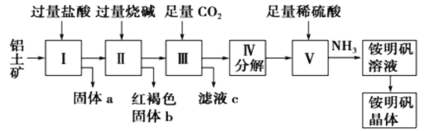
请回答下列问题:
(1)固体a的化学式为___,固体b化学式为___,Ⅲ中通入足量CO2气体发生反应的离子方程式为___。
(2)由Ⅴ制取铵明矾溶液的化学方程式为___。
(3)由I→II→III→IV都要用到的分离方法是___,由铵明矾溶液中制铵明矾晶体的操作是___,___,过滤,洗涤,干燥保存。
(4)向10gFe2O3、SiO2和Al2O3的混合物中,加入100mL稀硫酸,过滤后,向滤液中加入10mol/LNaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示。则混合物中三氧化二铝的质量分数为___。
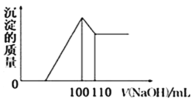
(5)有一种含铁、硅等元素的矿石,其主要成分的化学式为Na2Fe5(OH)2Si8O22,该物质中+2价铁与+3价铁的物质的量之比为___。将mg该矿石用足量的酸溶解后,加入过量铜粉使溶液中的铁元素全部变为Fe2+,过滤后滤液用cmol/L的KMnO4酸性溶液与Fe2+反应,用去VmL溶液。该矿石中铁元素的质量分数为___(用含m、c、V的代数式表示)。
高一化学工业流程中等难度题查看答案及解析
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体的工艺流程如图所示:
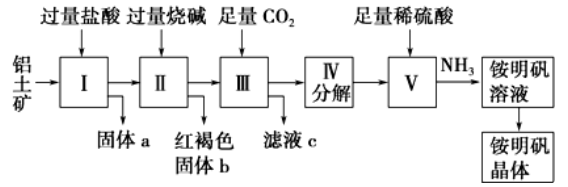
请回答下列问题:
(1)固体a的化学式为____,固体b化学式为____,Ⅲ中通入足量CO2气体发生反应的离子方程式为________________.
(2)由Ⅴ制取铵明矾溶液的化学方程式为______________.
(3)由I→II→III→IV都要用到的分离方法是______,由铵明矾溶液中制铵明矾晶体的操作是______________.
(4)如果先向铝土矿加入过量氢氧化钠,再加入过量盐酸,此时首先出现的固体a是__.
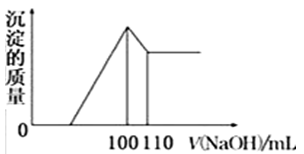
(5)向10gFe2O3、SiO2和Al2O3的混合物中,加入100ml稀硫酸,过滤后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示.则混合物中三氧化二铝的质量分数为______.
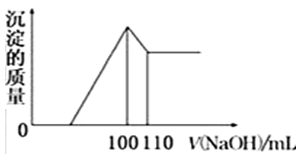
高一化学简答题困难题查看答案及解析
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体的工艺流程如图所示:

请回答下列问题:
(1)固体a的化学式为____,固体b化学式为____,Ⅲ中通入足量CO2气体发生反应的离子方程式为________________.
(2)由Ⅴ制取铵明矾溶液的化学方程式为______________.
(3)由I→II→III→IV都要用到的分离方法是______,由铵明矾溶液中制铵明矾晶体的操作是______________.
(4)如果先向铝土矿加入过量氢氧化钠,再加入过量盐酸,此时首先出现的固体a是__.
(5)向10gFe2O3、SiO2和Al2O3的混合物中,加入100ml稀硫酸,过滤后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示.则混合物中三氧化二铝的质量分数为______.
高一化学简答题困难题查看答案及解析