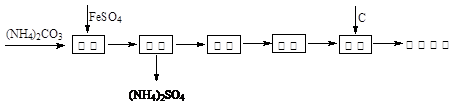-
某硫酸厂产生的烧渣(主要含 、
、 及少量
及少量 )可用于制备
)可用于制备 和还原铁粉,其流程如图:
和还原铁粉,其流程如图:
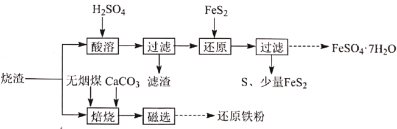
(1)“酸溶”前需粉碎烧渣,其目的是_________、________。
(2)“滤渣”的主要成分是_________(填化学式)。
(3)“还原”时, 被氧化为
被氧化为 的离子方程式是_________。
的离子方程式是_________。
(4)“焙烧”时,烧渣、无烟煤、 的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
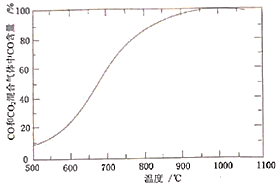
添加 的目的是:①脱除
的目的是:①脱除 等;②_________。
等;②_________。
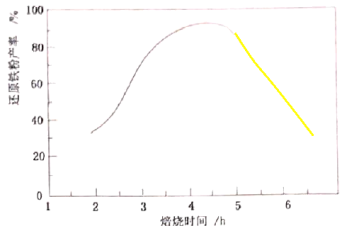
(5)“焙烧”在半封闭装置中进行,投料层表面盖有适当厚度的煤层,“焙烧”时间控制在4~4.5小时(焙烧时间对还原铁粉产率的影响如图所示),超过5小时后还原铁粉产率降低的原因是_______。
-
以高硫铝土矿 主要成分为
主要成分为 、
、 、
、 ,少量
,少量 和金属硫酸盐
和金属硫酸盐 为原料,生产氧化铝并获得
为原料,生产氧化铝并获得 的部分工艺流程如下:
的部分工艺流程如下:
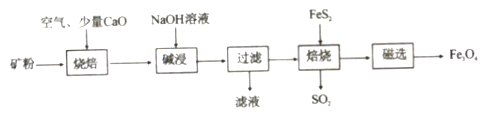
 粉碎高硫铝土矿石的目的是______。
粉碎高硫铝土矿石的目的是______。
 焙烧时发生氧化还原反应:______
焙烧时发生氧化还原反应:______ ______
______ ______
______ ______
______ ,配平该方程式。
,配平该方程式。
 碱浸时发生反应的化学方程式为______。
碱浸时发生反应的化学方程式为______。
 过滤后向滤液中通入过量的
过滤后向滤液中通入过量的 气体,反应的离子方程式为______。
气体,反应的离子方程式为______。
 “过滤”得到的滤渣中含有大量的
“过滤”得到的滤渣中含有大量的 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的 :
: ______。
______。
-
高纯氧化铁是现代电子工业的重要材料.以下是用硫酸厂产生的烧渣 主要成分为
主要成分为 、
、 、FeO、
、FeO、 为原料制备高纯氧化铁
为原料制备高纯氧化铁 软磁
软磁 的生产流程示意图,下列说法不正确的是
的生产流程示意图,下列说法不正确的是
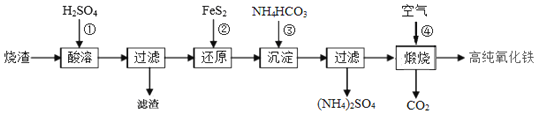
A.酸浸时,常需将烧渣粉碎、并加入过量 ,其目的是提铁元素的浸出率,同时抑制铁离子的水解
,其目的是提铁元素的浸出率,同时抑制铁离子的水解
B.加入 时,发生反应
时,发生反应 的离子方程式为
的离子方程式为
C.加入 为了生成
为了生成 ,检验
,检验 是否洗涤干净的方法是取最后一次洗涤液少量放入试管,滴加盐酸酸化的氯化钡溶液,若无沉淀生成,说明洗涤干净
是否洗涤干净的方法是取最后一次洗涤液少量放入试管,滴加盐酸酸化的氯化钡溶液,若无沉淀生成,说明洗涤干净
D.煅烧时空气中的氧气作氧化剂,所以用氯气代替空气也可得到高纯氧化铁
-
某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3,其流程如下:
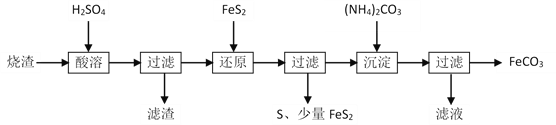
已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:FeS2 + 14Fe3+ + 8H2O =15Fe2+ + 2SO42— + 16H+
下列说法不正确的是
A. “还原”后可以用KSCN检验Fe3+是否反应完全
B. “还原”时反应Ⅱ的离子方程式为2Fe3+ + FeS2 = 2S↓+ 3Fe2+
C. “沉淀”时,可以先将溶液调节成强碱性,再加入(NH4)2CO3
D. 所得FeCO3需充分洗涤,可以用稀盐酸和BaCl2溶液检验FeCO3是否已洗涤干净
-
铬铁矿主要含有亚铬酸亚铁 ,还含有少量
,还含有少量 和
和 。由铬铁矿制备
。由铬铁矿制备 的流程如图1所示:
的流程如图1所示:
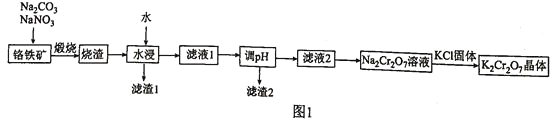
已知:常温下, ,
, 。
。
回答下列问题:
(1)铬铁矿与 、
、 混合煅烧之前应先将其粉碎,目的是_______________。
混合煅烧之前应先将其粉碎,目的是_______________。
(2) “煅烧”过程中主要反应的化学方程式为_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。
。
(3)已知: 和
和 与
与 高温煅烧可生成
高温煅烧可生成 和
和 。“滤渣1”的主要成分为_____________________
。“滤渣1”的主要成分为_____________________ 填化学式
填化学式 ,其一种用途为_____________________
,其一种用途为_____________________
(4)“调pH”的过程即是用酸酸化使pH约为5,其目的是_____________________,“滤渣2”的主要成分为_____________________ 填化学式
填化学式 ,同时
,同时 转化为
转化为 ,此转化过程的离子方程式为____________________________。
,此转化过程的离子方程式为____________________________。
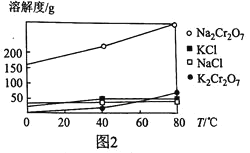
(5)  、KCl、
、KCl、 、NaCl的溶解度曲线如图2所示,结合图象解释向
、NaCl的溶解度曲线如图2所示,结合图象解释向 溶液中加入KCl固体经一系列操作后得到
溶液中加入KCl固体经一系列操作后得到 的理由:_____________________________。
的理由:_____________________________。
(6)该流程产生的含铬废水不能随意排放,可通过电解法处理 装置如图3所示
装置如图3所示 ,电解时,在阴极区可生成
,电解时,在阴极区可生成 和
和 沉淀,电解后溶液中
沉淀,电解后溶液中 ,则溶液中
,则溶液中 ____________
____________ 。
。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁( ),进一步制备高纯度还原铁粉。
),进一步制备高纯度还原铁粉。
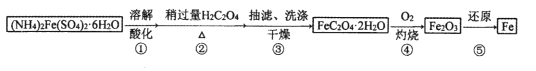
已知: 难溶于水;
难溶于水; 是二元弱酸,溶于水。
是二元弱酸,溶于水。
(1)步骤②中H2C2O4稍过量的目的是:_____________________;
(2)步骤②中得到FeC2O4.2H2O的离子反应方程式为:_________________________。
(3)实现步骤④,必须在 ______(填仪器名称)中进行,该步骤发生的化学反应方程式为:______________
(4)为实现步骤⑤,不宜用碳粉直接还原Fe2O3,理由是________________________。
(5)若将固体 放在一个可称出质量的容器内加热,
放在一个可称出质量的容器内加热, ( Mr=180)首先逐步失去结晶水,温度继续升高时.
( Mr=180)首先逐步失去结晶水,温度继续升高时. (Mr=144)会逐渐转变为铁的各种氧化物。称取18.00g
(Mr=144)会逐渐转变为铁的各种氧化物。称取18.00g ,持续加热,剩余固体的质量随温度变化的部分数据如下表(其中450℃以前是隔绝空气加热,450℃以后是在空气中加热):
,持续加热,剩余固体的质量随温度变化的部分数据如下表(其中450℃以前是隔绝空气加热,450℃以后是在空气中加热):
| 温度/℃ | 25 | 150 | 300 | 350 | 400 | 450 | 500 | 600 | 700 | 800 |
| 固体质量/g | 18.00 | 16.20 | 14.40 | 14.40 | 7.20 | 7.20 | 8.00 | 8.00 | 7.73 | 7.73 |
根据上述数据计算并推断:150℃剩余的固体物质是________________(填化学式,下同);800℃剩余的固体物质是________________。
-
还原铁粉是粉末冶金工业的重要原料,利用生产钛白的副产品绿矾制备还原铁粉的工业流程如下:
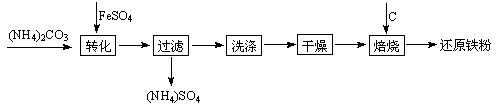
⑴干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3·nH2O被空气氧化为FeOOH,其化学方程式为。
⑵取干燥后的FeCO3样品12.49 g焙烧至600℃,质量变为8.00 g,继续加热最终得到Fe 6.16 g,则600℃产物的可能组成为,计算FeCO3样品中FeCO3与FeOOH的质量。
⑶若将28.12 g还原铁粉(含少量FexC)在氧气流中加热,得到标准状况下的CO2 224 mL;将相同质量的还原铁粉与足量硫酸反应,得到标准状况下的H2 10.752 L,计算FexC的化学式。(假设还原铁粉仅含两种物质)
-
还原铁粉是冶金工业的重要原料,利用绿矾制备还原铁粉的工业流程如下:
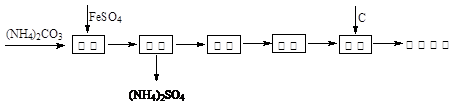
干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3·nH2O被空气氧化为FeOOH,其化学方程式为________。
取干燥后的FeCO3样品12.49 g焙烧至600℃,质量变为8.00 g。所得产物用CO还原可得到Fe 6.16g。则600℃产物的可能组成是________________________________________。
根据以上数据可计算FeCO3样品中FeCO3与FeOOH的质量。FeCO3的质量为_________, FeOOH的质量为________________。
-
马日夫盐 用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为
用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为 及少量的FeO、
及少量的FeO、 和
和 )为原料制备马日夫盐的主要工艺流程如图:
)为原料制备马日夫盐的主要工艺流程如图:
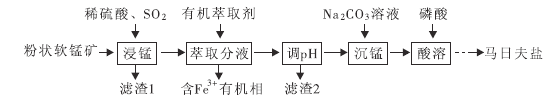
(1)“浸锰”过程中,FeO参与氧化还原反应的离子方程式为_______________。
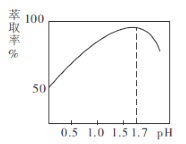
(2) 的萃取率与溶液的pH的关系如图所示,当
的萃取率与溶液的pH的关系如图所示,当 时,
时, 的萃取率急剧下降的原因可能为_______________(用化学用语表示)。
的萃取率急剧下降的原因可能为_______________(用化学用语表示)。
(3)“调pH”的最大范围为________。
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| 
| l. 8 | 3.2 |
| 
| 3.0 | 5.0 |
| 
| 5.8 | 8.8 |
| 
| 7.8 | 9.8 |
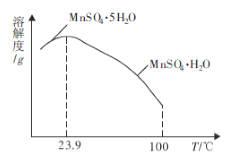
(4)如图为硫酸锰水合物的溶解度曲线,若要用“调pH”所得滤液制备 ,需要控制温度在80℃~90℃之间的原因是_____,采用水浴加热,经蒸发浓缩、_____(填操作名称)、用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥获得。
,需要控制温度在80℃~90℃之间的原因是_____,采用水浴加热,经蒸发浓缩、_____(填操作名称)、用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥获得。
(5)写出检验“沉锰”是否已完成的实验操作_________。
(6)常温下,马日夫盐溶液显________性(填“酸”或“碱”),理由是:____________。(写出计算过程并结合必要的文字说明。已知: 的电离常数
的电离常数 ,
, ,
, )
)
-
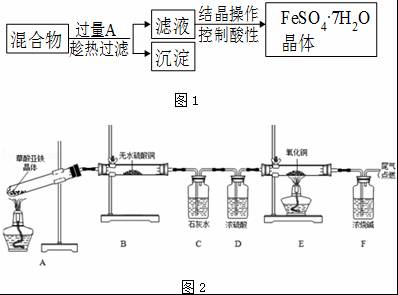
某校化学课外小组用硫酸铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体并进行如下实验.制备硫酸亚铁晶体主要的操作流程如图1
请根据题目要求回答下列问题:
(1)A的化学式为 .
(2)趁热过滤的目的是 .
(3)结晶操作过程中应控制滤液酸性的原因是 .
(4)实验室利用硫酸亚铁铵溶液[(NH4)2Fe(SO4)2]和草酸溶液反应生成草酸亚铁,草酸亚铁晶体(相对分子质量180)受热易分解,某课外小组设计如图2的实验装置来检验其分解产物.
①该装置中最不合理的部分 (填字母),原因是 .
②改用正确装置开始实验,B处变蓝,说明草酸亚铁晶体中有 ;C处有白色沉淀,E处黑色粉末变为红色,说明草酸亚铁分解产生 (填化学式).
、
及少量
)可用于制备
和还原铁粉,其流程如图:

被氧化为
的离子方程式是_________。
的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):

的目的是:①脱除
等;②_________。