天门冬氨酸锌是一种补锌剂,可以用、天门冬氨酸为原料制备。
(1)基态核外电子排布式为_______。
(2)的空间构型为________(用文字描述);与
互为等电子体的一种阳离子的化学式为________。
(3)天门冬氨酸()分子中氮原子的轨道杂化类型为________;天门冬氨酸_______(填“难溶”或“易溶”)于
盐酸。
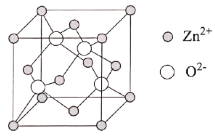
(4)ZnO的晶胞结构如图所示,的配位数为________。
高三化学综合题中等难度题
天门冬氨酸锌是一种补锌剂,可以用、天门冬氨酸为原料制备。
(1)基态核外电子排布式为_______。
(2)的空间构型为________(用文字描述);与
互为等电子体的一种阳离子的化学式为________。
(3)天门冬氨酸()分子中氮原子的轨道杂化类型为________;天门冬氨酸_______(填“难溶”或“易溶”)于
盐酸。
(4)ZnO的晶胞结构如图所示,的配位数为________。

高三化学综合题中等难度题
天门冬氨酸锌是一种补锌剂,可以用、天门冬氨酸为原料制备。
(1)基态核外电子排布式为_______。
(2)的空间构型为________(用文字描述);与
互为等电子体的一种阳离子的化学式为________。
(3)天门冬氨酸()分子中氮原子的轨道杂化类型为________;天门冬氨酸_______(填“难溶”或“易溶”)于
盐酸。
(4)ZnO的晶胞结构如图所示,的配位数为________。

高三化学综合题中等难度题查看答案及解析
A.[物质结构与性质]
Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为____。
(2)的空间构型为____(用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为____(填元素符号)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为____;推测抗坏血酸在水中的溶解性:____(填“难溶于水”或“易溶于水”)。
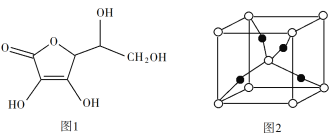
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为____。
高三化学综合题简单题查看答案及解析
Ⅰ、Cu2O 广泛应用于太阳能电池领域。以 CuSO4、NaOH 和抗坏血酸为原料,可制备 Cu2O。
(1)Cu2+基态核外电子排布式为________。
(2)SO4 2﹣的空间构型为_________(用文字描述),Cu2+与 OH-反应能生成[Cu(OH)4 ]2-, [Cu(OH)4]2-中的配位原子为_______(填元素符号)。
(3)抗坏血酸的分子结构如图 1 所示,分子中碳原子的轨道杂化类型为________;推测抗坏血酸在水中的溶解性:_______(填“难溶于水”或“易溶于水”)。
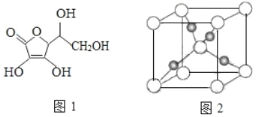
(4)一个 Cu2O 晶胞(如图 2)中,Cu 原子的数目为_________。
Ⅱ、磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 FeCl3、NH4H2PO4、LiCl 和苯胺等作为原料制备。回答下列问题:
(5)在周期表中,与 Li 的化学性质最相似的邻族元素是___,该元素基态原子核外 M层电子的自旋状态_______(填“相同”或“相反”)。
(6)苯胺( )的晶体类型是_________。苯胺与甲苯(
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
高三化学综合题困难题查看答案及解析
[化学——物质结构与性质](13分)
氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节。
Ⅰ.氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是 (填序号)。
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1 mol水分子可形成4 mol氢键
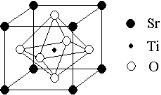
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气。已知钛酸锶晶胞结构如图,则其化学式为 。
Ⅱ.氢气的存储
(3)Ti(BH4)2是一种储氢材料。
①Ti原子在基态时的核外电子排布式是 。
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为 。
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子。
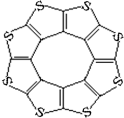
①元素电负性大小关系是:C S(填“>”、“=”或“<”)。
②分子中C原子的杂化轨道类型为 。
③有关键长数据如下:
| C—S | C=S | C16S8中碳硫键 | |
| 键长/pm | 181 | 155 | 176 |
从表中数据可以看出,C16S8中碳硫键键长介于C—S与C=S之间,原因可能是: 。
④C16S8与H2微粒间的作用力是 。
高三化学填空题极难题查看答案及解析
[化学——物质结构与性质](13分)
氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节。
Ⅰ 氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是 (填序号)。
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1 mol水分子可形成4 mol氢键
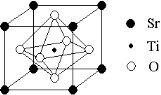
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气。已知钛酸锶晶胞结构如图,则其化学式为 。
Ⅱ 氢气的存储
(3)Ti(BH4)2是一种储氢材料。
①Ti原子在基态时的核外电子排布式是 。
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为 。
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子。
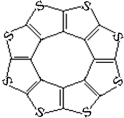
①元素电负性大小关系是:C S(填“>”、“=”或“<”)。
②分子中C原子的杂化轨道类型为 。
③有关键长数据如下:
| C—S | C=S | C16S8中碳硫键 | |
| 键长/pm | 181 | 155 | 176 |
从表中数据可以看出,C16S8中碳硫键键长介于C—S与C=S之间,原因可能是: 。
④C16S8与H2微粒间的作用力是 。
高三化学填空题中等难度题查看答案及解析
由硝酸锰[Mn(NO3)2]制备的一种含锰催化剂,常温下能去除甲醛、氢氰酸(HCN)等有毒气体。
(1) Mn2+基态核外电子排布式是________________。NO3-的空间构型为__________________(用文字描述)
(2) 甲醛分子中,碳原子的杂化方式为________。
(3) HCN分子中σ键与π键的数目比为________。H、C、N三种元素的电负性由大到小的顺序为________。
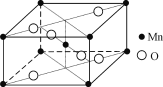
(4) 硝酸锰受热可分解生成NO2和某种锰的氧化物。该氧化物晶胞结构如右图所示。写出硝酸锰受热分解的化学方程式:__________________________。
高三化学解答题中等难度题查看答案及解析
以Fe和BN为原料合成的铁氮化合物在光电子器材领域有广泛应用。
(1)基态Fe原子核外电子排布式为___。
(2)硼在室温下与F2反应生成BF3,BF3的空间构型为__。写出一种与BF3互为等电子体的阴离子:___。
(3)以氨硼烷(NH3BH3)为原料可以获得BN。氨硼烷的结构式为__(配位键用“→”表示),氨硼烷能溶于水,其主要原因是__。
(4)如图为Fe与N所形成的一种化合物的基本结构单元,该化合物的化学式为__。
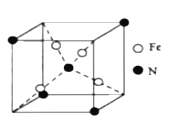
高三化学填空题中等难度题查看答案及解析
黄铁矿(主耍成分为FeS2)是工业制硫酸的主要原料。回答下列问题
(1)基态铁原子的价电子排布图_____________
(2) 制硫酸的过程中会产生SO3, SO3的空间构型是_____ 。
(3) 配合物[Fe(H2N-CH2-CH2-NH2)3]SO4的名称是硫酸三乙二胺合铁(II). 其中的乙二胺 (H2N-CH2-CH2-NH2)是配体.
① [Fe(H2N-CH2-CH2-NH2)3]SO4的晶休类型属于______ ,其 中 C、N、O的电负性由大到小的顺序为______
③乙二胺分于中氮原子的杂化轨道类型是______. 乙二胺和偏二甲肼(CH3)2NNH2互为同分异构休 .乙二胺的沸点117.2 0C,偏二甲肼的沸点63 0C。两者沸点不同的主要原因是_________________
(4)铁和铜的电离能数据如下表:
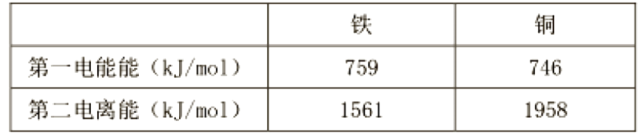
第一电离能与第二电离能之间的差值铜比铁大得多的原因是______
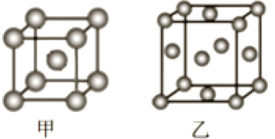
(5)铁原子有两种堆枳方式,相应地形成两种晶胞(如图甲、乙所示),其中晶胞乙的堆积方式是______, 晶胞甲中原子的空间利用率为______(用含的代数式表示)。
高三化学综合题困难题查看答案及解析
四氧化三钴(Co3O4)纳米颗粒可以用于人造光合作用,以水和二氧化碳为原料制得甲醇燃料。回答下列问题:
(1)二氧化碳的水溶液中含有少量CO32-,CO32-的空间构型为____________。
(2)CO2,SiO2为同族元素的氧化物,SiO2熔点高的原因是__________________。
(3)甲醇分子中,中心原子的的杂化轨道类型为__________。甲醇易溶于水,其主要原因是____________________________________________________。
(4)Co3O4晶体结构中,O2-为立方紧密堆积;Co2+为四配位,填充于四面体空隙;Co3+填充于八面体空隙。Co2+的价层电子式为______;Co3O4晶体中Co3+的配位数为______。
(5)氧化亚钴与稀盐酸反应可生成紫红色六水合物(CoCl2·6H2O), 该反应的化学方程式为________________________________________________。
(6)四氧化三钴加热至900℃会分解生成氧化亚钴,氧化亚钴的晶体结构与氯化钠类似。若氧化亚钴晶体的晶胞边长为a pm,则两个紧邻的Co2+之间的距离为__________pm。
高三化学综合题中等难度题查看答案及解析
硒是一种非金属,可以用作光敏材料、电解锰行业催化剂。
(l)Se是元素周期表中第34号元素,其基态原子的核外电子排布式为________。
(2)根据价层电子对互斥理论,可以推知SeO3的分子空间构型为________,其中Se原子采用的轨道杂化形式为________。
(3)CSe2与CO2结构相似,CSe2分子内σ键与π键个数之比为________。CSe2首次是由H2Se与CCl4反应后制取的,CSe2分子内的Se—C—Se键角________(填“大于”,“等于”或“小于”)H2Se分子内的H—Se—H键角。
(4)硒化铷晶体属于反萤石型结构,晶胞结构如图所示。每个晶胞中包含________个Rb2Se单元,其中Se2-周围与它距离最近且相等的Rb+的离子数目为________。
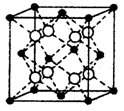
高三化学填空题中等难度题查看答案及解析