-
A.[物质结构与性质]
Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为____。
(2) 的空间构型为____(用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为____(填元素符号)。
的空间构型为____(用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为____(填元素符号)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为____;推测抗坏血酸在水中的溶解性:____(填“难溶于水”或“易溶于水”)。
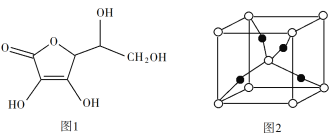
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为____。
-
Ⅰ、Cu2O 广泛应用于太阳能电池领域。以 CuSO4、NaOH 和抗坏血酸为原料,可制备 Cu2O。
(1)Cu2+基态核外电子排布式为________。
(2)SO4 2﹣的空间构型为_________(用文字描述),Cu2+与 OH-反应能生成[Cu(OH)4 ]2-, [Cu(OH)4]2-中的配位原子为_______(填元素符号)。
(3)抗坏血酸的分子结构如图 1 所示,分子中碳原子的轨道杂化类型为________;推测抗坏血酸在水中的溶解性:_______(填“难溶于水”或“易溶于水”)。
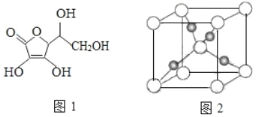
(4)一个 Cu2O 晶胞(如图 2)中,Cu 原子的数目为_________。
Ⅱ、磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 FeCl3、NH4H2PO4、LiCl 和苯胺等作为原料制备。回答下列问题:
(5)在周期表中,与 Li 的化学性质最相似的邻族元素是___,该元素基态原子核外 M层电子的自旋状态_______(填“相同”或“相反”)。
(6)苯胺( )的晶体类型是_________。苯胺与甲苯(
)的晶体类型是_________。苯胺与甲苯(  )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
-
[物质结构与性质]
铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为____________________。
(2)丙酮( )分子中碳原子轨道的杂化类型是_______________,1 mol 丙酮分子中含有σ键的数目为______________。
)分子中碳原子轨道的杂化类型是_______________,1 mol 丙酮分子中含有σ键的数目为______________。
(3)C、H、O 三种元素的电负性由小到大的顺序为________________。
(4)乙醇的沸点高于丙酮,这是因为____________________。
(5)某FexNy的晶胞如题21图-1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如题21图-2 所示,其中更稳定的Cu替代型产物的化学式为___________。
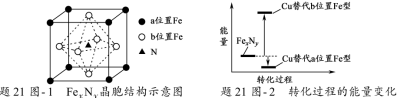
-
环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
环戊二烯可用于制备二茂铁(Fe(C5H5)2,结构简式为 ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
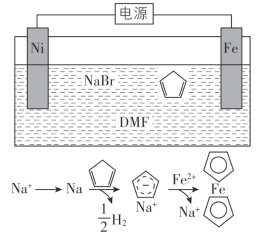
该电解池的阳极为____________,总反应为__________________。电解制备需要在无水条件下进行,原因为_________________________。
-
Cu2O是一种在涂料、玻璃等领域应用非常广泛的红色氧化物。它不溶于水和醇,溶于盐酸、氯化铵、氨水,易被O2、 硝酸等氧化。一种以硫化铜矿石(含CuFeS2、Cu2S 等) 为原料制取Cu2O 的工艺流程如下:

(1) “硫酸化焙烧”时:CuS 与O2反应生成CuSO4等物质的化学方程式为________________;在100℃时,发生反应的离子方程式为________________________________。
(2)加入Na2SO4的作用除减小物料间黏结外,另一主要作用是_____________________。
(3) “浸取”时为提高铜的浸取率,除需控制液固物质的量之比外,还需控制________________ (至少列举两点)。
(4)得到产品Cu2O的一系列操作主要是___________________________________。
(5)下列有关说法正确的是______________
A.焙烧时得到的尾气可用碱液加以处理
B.Cu2O露置至于空气中会变黑
C.经一系列操作得到产品Cu2O后的副产品,经处理后可作净水剂
D.“制备”时,溶液的pH越小,Cu2O 的产率越高
-
SPC(2Na2CO3•3H2O2)具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO4•10H2O)、H2O2等为原料制备SPC的工艺流程如下:

回答下列问题:
(1)步骤I产生的滤渣为__________________(填名称)。
(2)步骤II中发生反应的离子方程式为_________________。其中生成的__________(填化学式)可以循环使用。
(3)步骤V中,合成时需选择温度为15℃,其原因是_____________________。
(4)抽滤后用乙醇洗涤的作用是_______________________________________。
(5)SPC的保存方法是______________________________。
(6)过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600 g样品,置于250 mL锥形瓶中,并用100 mL 0.5 mol•L-1硫酸溶解完全,立即用0.02000mol•L-1KMnO4标准溶液滴定,滴定至终点时溶液颜色为_____,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56 mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24 mL。该样品的活性氧含量为______%。
-
SPC(2Na2CO3∙3H2O2)具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO4∙10H2O)、H2O2等为原料制备SPC的工艺流程如下:

回答下列问题:
⑴步骤Ⅰ中________ 填“有”或“没有”
填“有”或“没有” 发生氧化还原反应。
发生氧化还原反应。
⑵步骤Ⅱ中会生成一种可以循环使用的物质,该物质的化学式为________。
⑶步骤Ⅲ中需要加热,发生反应的化学方程式为_________________________________。
⑷步骤Ⅴ中,合成时需选择温度为15℃,其目的是___________。
⑸SPC的保存方法是_____________________________。
⑹过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600g样品,置于250mL锥形瓶中,并用100mL 0.5 mol·L-1硫酸溶解完全,立即用0.02000mol·L-1 KMnO4标准溶液滴定,滴定至终点时溶液颜色为________,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24mL。该样品的活性氧含量为_______%。
-
SPC(2Na2CO3•3H2O2具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO4•10H2O)、H2O2等为原料制备SPC的工艺流程如下:
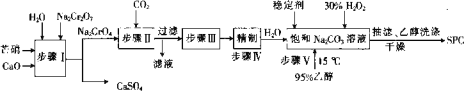
回答下列问题:
(1)步骤I中_____(填“有”或“没有”)发生氧化还原反应。
(2)步骤II中会生成一种可以循环使用的物质,该物质的化学式为_____。
(3)步骤Ⅲ中需要加热,发生反应的化学方程式为______。
(4)步骤Ⅳ中,合成时需选择温度为15℃,其目的是_____,从环境保护的角度看,诙流程中存在的缺点是_______。
(5)SPC的保存方法是________。
(6)过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600 g样品, 置于250 mL锥形瓶中,并用100 mL 0. 5 mol•L-1硫酸溶解完全,立即用0.02000mol•L-1KMnO4标准溶液滴定,滴定至终点时溶液颜色为_____,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56 mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24 mL。该样品的活性氧含量为______%。
-
高铁酸钾广泛应用于净水、电池工业等领域。工业上以钛白粉生产的副产品FeSO4制备高铁酸钾的生产流程如下:
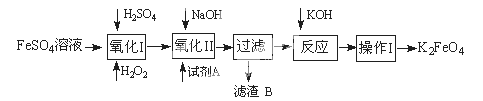
查资料得知K2FeO4的一些性质:
①在碱性环境中稳定,在中性和酸性条件下不稳定
②溶解度很大,难溶于无水乙醇等有机溶剂
③具有强氧化性,能氧化有机烃、苯胺和80%以下乙醇溶液
回答下列问题:
(1)写出“氧化I”中,生成Fe3+的离子反应方程式________。
(2)氧化II中,试剂A为(填“H2O2”或“HNO3”或“NaClO”);过滤操作中,得到的滤渣B中除NaCl还有________
(3)操作I中包括冷却结晶、过滤、洗涤干燥几个步骤。洗涤干燥的目的是脱碱脱水,进行该操作时最好用________洗涤。
(4)净水时高铁酸钾能逐渐与水反应生成絮状的Fe(OH)3,请补充并配平该反应方程式: ________K2FeO4 + ________ H2O = ________Fe(OH)3↓ + ________KOH + ________
(5)将一定量的K2FeO4投入一定浓度的FeCl3溶液中,测得剩余K2FeO4浓度如下图所示,推测产生曲线I和曲线II差异的原因是________。

-
高铁酸钾广泛应用于净水、电池工业等领域。工业上以钛白粉生产的副产品FeSO4制备高铁酸钾的生产流程如下:
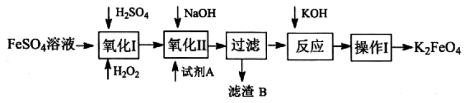
查资料得知K2FeO4的一些性质:
①在碱性环境中稳定,在中性和酸性条件下不稳定。
②在水中溶解度很大,难溶于无水乙醇等有机溶剂。
回答下列问题:
(1)写出氧化I中,生成Fe3+的离子反应方程式:
(2)氧化II中,试剂A为 (填“H2O2”或“HNO3”或“NaC1O”),反应的离子方程式为_____________________。
(3)操作I中包括冷却结晶,过滤洗涤、干燥几个步骤,洗涤干燥的目的是脱碱脱水,进行洗涤操作时应该用 洗涤。
(4)净水时高铁酸钾能逐渐与水反应生成絮状的Fe(OH)3,请补充并配平该反应方程式的系数及产物:
______K2FeO4 + H2O  Fe(OH)3(胶体)+ KOH + 。
Fe(OH)3(胶体)+ KOH + 。
将一定量的K2FeO4投入一定浓度的FeC13溶液中,测得剩余K2FeO4浓度如下图所示,推测产生曲线I和曲线II差异的原因是: 。
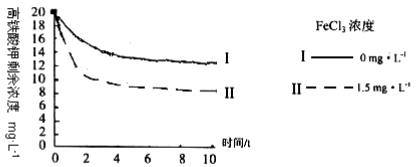
(5)制得的粗K2FeO4产品中常混有少量KCl。取5.0 g粗产品溶于足量稀硝酸,充分反应后,加入足量的硝酸银,过滤得到沉淀,洗涤、干燥,称量得到1.435 g固体,K2FeO4的质量分数为___________。(可能用到的相对原子质量:O 16 Cl 35.5 K 39 Fe 56 Ag 108)
的空间构型为____(用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为____(填元素符号)。











