-
钠和铜的单质及其化合物在社会实际中有着广泛的应用。
(1)NaCl晶体的晶胞结构如图所示,每个NaCl的晶胞中含有的阴离子的个数为__,阳离子周围最近且等距离得阴离子的个数为__。

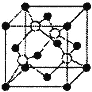
(2)碘化钠溶液和硫酸铜溶液能反应生成一种铜的碘化物A(白色沉淀),A的晶胞如右图所示,则A的化学式是__,A中铜元素的化合价为__。
(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀,该物质中的NH3通过___键与中心离子Cu2+结合,NH3分子中N原子的杂化方式是__。与NH3分子互为等电子体的一种阳离子是__。
-
(12分)钠和铜的单质及其化合物在社会实际中有着广泛的应用。
(1)Cu2+基态的核外电子排布式为_______________。
(2)NaCl晶体的晶胞结构如图所示,在NaCl的晶胞中含有的阴离子的个数为________,阳离子的配位数为________。

(3)钠的有关卤化物的熔点见下表,钠的卤化物熔点按NaF、NaCl、NaBr、NaI顺序降低的原因是______________。
| NaF | NaCl | NaBr | NaI |
| 熔点/℃ | 993 | 801 | 747 | 661 |
(4)碘化钠溶液和硫酸铜溶液能反应生成一种铜的碘化物A(白色沉淀,,A的晶胞如图所示,则A的化学式是______________,A中铜元素的化合价为_____________。

-
铁、铜及其化合物在日常生产、生活中有着广泛的应用。请回答下列问题:
(1)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为__,δ、α两种晶胞中铁原子的配位数之比为__。
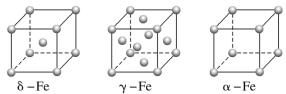
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于__(填晶体类型)。
(3)铜晶体中铜原子的堆积方式为__,晶胞中原子的空间利用率为__。
(4)CuCl2和CuCl是铜的两种常见的氯化物。
①如图表示的是___(填“CuCl2”或“CuCl”)的晶胞,其中Cl-的配位数为__。
②已知铜和Cl的电负性分别为1.9和3.0,则铜与Cl形成的化合物属于__(填“离子”或“共价”)化合物。
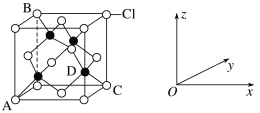
③原子坐标参数表示晶胞内部各原子的相对位置。图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为__。
-
铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
 的熔点为
的熔点为 ,沸点为
,沸点为 的晶体类型是 ______ ;
的晶体类型是 ______ ;
 羰基铁
羰基铁 可用作催化剂、汽油抗爆剂等。1mol
可用作催化剂、汽油抗爆剂等。1mol  分子中含______
分子中含______ 键;
键;
 氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为 ______ ;
氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为 ______ ;
 氧化亚铁晶体的晶胞如图2所示。已知:
氧化亚铁晶体的晶胞如图2所示。已知:

氧化亚铁晶体的密度为 ,
, 代表阿伏加德罗常数的值。在该晶胞中,与
代表阿伏加德罗常数的值。在该晶胞中,与 紧邻且等距离的
紧邻且等距离的 数目为 ______ ;
数目为 ______ ; 与
与 最短核间距为 ______ pm。
最短核间距为 ______ pm。 写出表达式
写出表达式
-
碳族元素的单质和化合物在化工、医药、材料等领域有着广泛的应用。
(1)锗是重要半导体材料,基态Ge原子中,核外电子占据最高能级的符号是______,该能级的电子云轮廓图为________。Ge的晶胞结构与金刚石类似,质地硬而脆,沸点2830℃,锗晶体属于_______晶体。
(2)(CH3)3C+是有机合成重要中间体,该中间体中碳原子杂化方式为_______,(CH3)3C+中碳骨架的几何构型为________。
(3)治疗铅中毒可滴注依地酸钠钙,使Pb2+转化为依地酸铅盐。下列说法正确的是_______。
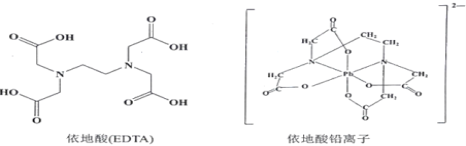
A.形成依地酸铅离子所需n(Pb2+)∶n(EDTA)=1∶4
B.依地酸中各元素的电负性从大到小的顺序为O>N>C>H
C.依地酸铅盐中含有离子键和配位键
D.依地酸具有良好的水溶性是由于其分子间能形成氢键
(4)下表列出了碱土金属碳酸盐的热分解温度和阳离子半径:
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
碱土金属碳酸盐同主族由上到下的热分解温度逐渐升高,原因是:__________。
(5)有机卤化铅晶体具有独特的光电性能,下图为其晶胞结构示意图:
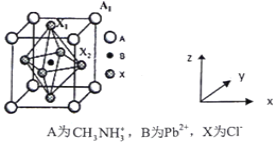
①若该晶胞的边长为anm,则Cl-间的最短距离是________。
②在该晶胞的另一种表达方式中,若图中Pb2+处于顶点位置,则Cl-处于____位置。
-
 晶体的晶胞结构与NaCl晶体的相似
晶体的晶胞结构与NaCl晶体的相似 如图所示
如图所示 ,但因为
,但因为 晶体中含有的哑铃形
晶体中含有的哑铃形 的存在,使晶胞沿一个方向拉长。下列关于
的存在,使晶胞沿一个方向拉长。下列关于 晶体的说法中正确的是
晶体的说法中正确的是
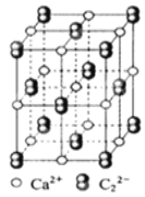
A. 1个 周围距离最近且等距离的
周围距离最近且等距离的 数目为4
数目为4
B. 该晶体中的阴离子和O2是等电子体
C.  克
克 晶体中含阴离子0.2mol
晶体中含阴离子0.2mol
D. 与每个 距离相等且最近的
距离相等且最近的 共有12个
共有12个
-
 晶体的晶胞结构与NaCl晶体的相似
晶体的晶胞结构与NaCl晶体的相似 如图所示
如图所示 ,但因为
,但因为 晶体中含有的哑铃形
晶体中含有的哑铃形 的存在,使晶胞沿一个方向拉长。下列关于
的存在,使晶胞沿一个方向拉长。下列关于 晶体的说法中正确的是
晶体的说法中正确的是
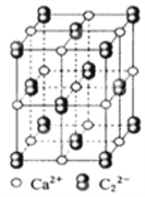
A.1个 周围距离最近且等距离的
周围距离最近且等距离的 数目为4
数目为4
B.该晶体中的阴离子和O2是等电子体
C. 克
克 晶体中含阴离子0.2mol
晶体中含阴离子0.2mol
D.与每个 距离相等且最近的
距离相等且最近的 共有12个
共有12个
-
钡在氧气中燃烧时得到一种钡的氧化物晶体,其晶胞为立方体,结构如图所示,有关说法不正确的是
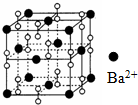
A.晶体的化学式为Ba2O2
B.该晶体属于离子晶体
C.该晶体晶胞结构与NaCl相似
D.与每个Ba2+距离相等且最近的Ba2+共有12个
-
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛。
(1) 分子的晶体中,在晶胞的顶点和面心均含有一个
分子的晶体中,在晶胞的顶点和面心均含有一个 分子,则一个
分子,则一个 晶胞的质量为_______。
晶胞的质量为_______。
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是_____(填字母)。
a.晶体的熔点:干冰>冰
b.晶体中的空间利用率:干冰>冰
c.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的是______(填字母)。
a.金刚石中碳原子的杂化类型为 杂化,石墨中碳原子的杂化类型为
杂化,石墨中碳原子的杂化类型为 杂化
杂化
b.晶体中共价键的键长:金刚石中 <石墨中
<石墨中
C.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
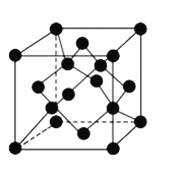
(4)金刚石晶胞结构如下图,立方 结构与金刚石相似,在
结构与金刚石相似,在 晶体中,
晶体中, 原子周围最近的
原子周围最近的 原子所构成的立体图形为_______,
原子所构成的立体图形为_______, 原子与
原子与 原子之间共价键与配位键的数目比为_______,一个晶胞中
原子之间共价键与配位键的数目比为_______,一个晶胞中 原子数目为___________。
原子数目为___________。
(5)已知 单质的晶体密度为
单质的晶体密度为 ,
, 的相对原子质量为
的相对原子质量为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则
,则 的原子半径为_________。
的原子半径为_________。
-
钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是( )
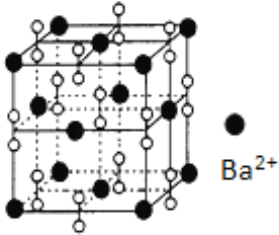
A. 该晶体属于离子晶体
B. 晶体的化学式为Ba2O2
C. 该晶体晶胞结构与NaCl相似
D. 与每个Ba2+距离相等且最近的Ba2+共有12个













