-
25℃时,分别向等体积pH均为a的CH3COOH溶液和HCN溶液中加水稀释,稀释过程中溶液的pH变化与溶液体积的关系如图所示:
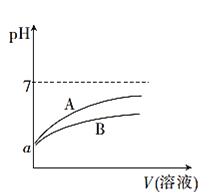
已知25℃时,HCN的电离平衡常数Ka=6.2×10-10,CH3COOH的电离平衡常数Ka=1.7×10-5
(1)表示CH3COOH溶液的pH变化趋势的曲线是____(填“A”或“B”)。
(2)pH均为a的CH3COOH溶液和HCN溶液,溶质的物质的量浓度较大的是____(填化学式)。
(3)25℃时,等浓度的NaCN溶液的pH___填“>”=”或“<”)CH3 COONa溶液的pH。
(4)25℃时,向20mL0.01mol·L-1CH3COOH溶液中逐滴加入0.01mol·L-1KOH溶液,当pH=7时,所加KOH溶液的体积____(填或“<”)20mL。
(5)用相同浓度的AgNO3溶液分别滴定浓度相同的含Cl-、Br-及I-的混合溶液,由图可确定首先沉淀的离子是______。(填离子符号)
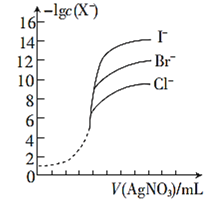
-
常温下,将等体积的盐酸和氨水分别加水稀释,溶液的导电性与溶液体积的变化曲线如图所示,下列说法正确的是
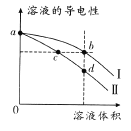
A.曲线II表示氨水加水稀释过程中溶液导电性的变化
B.溶液的pH 大小关系:c>b>d
C.若将bd两点溶液混合,则c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.由水电离出n(OH-):b>c
-
分别向等体积1mol/L盐酸和1mol/L醋酸溶液中加入等量的镁条,反应时间与溶液pH变化关系如右图。下列说法中不正确的是( )

A. Y代表盐酸与镁条的反应
B. a点时反应Y消耗镁条的量少
C. b点表示此时两溶液pH相等
D. c点表示此时反应结束
-
分别向等体积1mol/L盐酸和1mol/L醋酸溶液中加入等量的镁条,反应时间与溶液pH变化关系如右图。下列说法中不正确的是
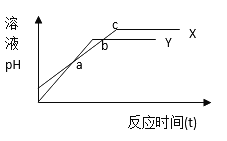
A. Y代表盐酸与镁条的反应 B. a点时反应Y消耗镁条的量少
C. b点表示此时两溶液pH相等 D. c点表示此时反应结束
-
向0.1mol/L CH3COOH溶液中加入CH3COONa晶体或加等体积水稀释时,都会引起( )
A.溶液的pH增大 B.CH3COOH的电离程度增大
C.溶液的导电能力减小 D.溶液的c (OH – )减小
-
常温下,分别向体积相同、浓度均为1 mol/L的HA、HB两种酸溶液中不断加水稀释,酸溶液的pH与酸溶液浓度的对数(lgc)间的关系如图。下列对该过程相关分析正确的是
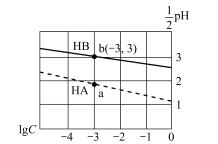
A.HB的电离常数(Ka)数量级为10-3
B.其钠盐的水解常数(Kh)大小关系是:NaB>NaA
C.a、b两点溶液中,水的电离程度b<a
D.当lgc= -7时,两种酸溶液均有pH=7
-
向0.1mol/L CH3COOH溶液中加入CH3COONa晶体或加等体积水稀释时,都会引起
A.溶液的pH增大 B.CH3COOH的电离程度增大
C.溶液的导电能力减小 D.溶液的c ( OH –)减小
-
向0.1mol/L CH3COOH溶液中加入CH3COONa晶体或加等体积水稀释时,都会引起( )
A.溶液的pH增大 B.CH3COOH的电离程度增大
C.溶液的导电能力减小 D.溶液的c (OH–)减小
-
向0.1 mol/L CH3COOH溶液中加入CH3COONa晶体或加等体积水稀释时,都会引起
A.溶液的pH增大 B.CH3COOH的电离程度增大
C.溶液的导电能力减小 D.溶液的c(OH-)减小
-
某温度下,将pH和体积均相同的HCl和CH3COOH溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
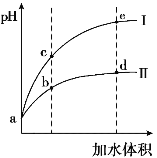
A.曲线II代表HCl的稀释过程
B.溶液中水的电离程度:b点>c点
C.从b点到d点,溶液中 保持不变
保持不变
D.该温度下,b点Kw的数值比e点大






