-
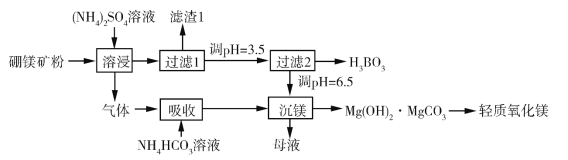
硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
回答下列问题:
(1)在95 ℃“溶侵”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_________。
(2)“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是_________。
(3)根据H3BO3的解离反应:H3BO3+H2O H++B(OH)−4,Ka=5.81×10−10,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
H++B(OH)−4,Ka=5.81×10−10,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
(4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为__________,母液经加热后可返回___________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是_________。
-
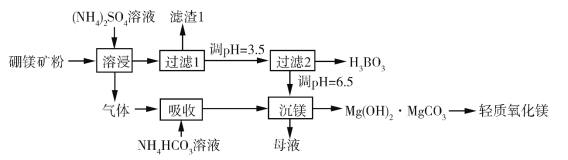
硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
回答下列问题:
(1)在95 ℃“溶侵”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_________。
(2)“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是_________。
(3)根据H3BO3的解离反应:H3BO3+H2O H++B(OH)−4,Ka=5.81×10−10,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
H++B(OH)−4,Ka=5.81×10−10,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
(4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为__________,母液经加热后可返回___________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是_________。
-
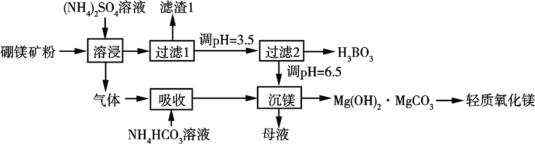
硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含 Mg2B2O5·H 2O、SiO2 及少量 Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
已 知 :H3BO3+H2O H++B(OH)
H++B(OH) ,Ka = 5.81×10 −10
,Ka = 5.81×10 −10
(1)“吸收”过程中反应的化学方程式为_________________________________。
(2)“滤渣 1”的主要成分有_____。
(3)为检验“过滤 1”后的滤液中是否含有 Fe3+离子,可选用的化学试剂是____________________________。
(4)在“过滤 2”前,将溶液 pH 调节至 3.5,目的是_____。
(5)在“沉镁”中生成 Mg(OH)2·MgCO3 沉淀的离子方程式为________________________________________________。
-
硼酸(H3BO3)是一种重要的化工原料。工业上采用以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3。Al2O3)为原料生产硼酸和轻质氧化镁,其工艺流程如下:

下列叙述错误的是
A.“溶浸”中产生的气体是氨气
B.“滤渣1”是SiO2
C.“过滤2”前,将溶液pH调节至3.5,目的是转化为硼酸沉淀
D.“沉镁”中得到的母液经加热后可返回“溶浸”工序循环使用
-
硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO•B2O3•H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:
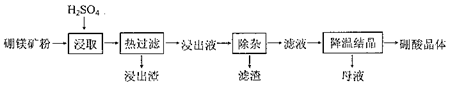
已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g。Fe3 +、Al3+、Fe2 +和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3. 2、5.2、9.7和12.4。
(1)由于矿粉中含CaCO3,“浸取”时容易产生大量泡沫使物料从反应器溢出,故应分批加入稀硫酸。该反应的化学方程式为________。
(2)“浸出液”显酸性,含H3BO3和Mg2+、SO42-,还含有Fe3 +、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是________。H2O2的作用是________ (用离子方程式表示)。
(3)“浸取”后,采用“热过滤”的目的是________。
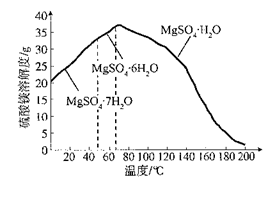
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如下图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4•H2O,应采取的措施是将“母液”蒸发浓缩,________。
-
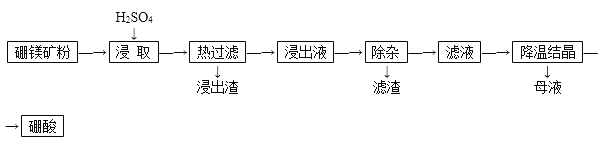
.硼酸(H3BO3:相对分子质量62)大量应用于玻璃制造业,以硼镁矿(2MgO·B2O3·H2O、SiO2及少量Fe3O4、CaCO3, Al2O3)为原料生产硼酸的工艺流程如下:
已知:ⅰ.Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4。
ⅱ.H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g。
(1)为了提高硼镁矿粉的浸出率,可采取的措施有_________________________(至少答两条)
(2)“浸出液”显酸性,含H3BO3和Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, H2O2的作用是_____________(用离子方程式表示),MgO除去的杂质离子是_______。
(3)已知H3BO3与过量的NaOH反应生成Na[B(OH)4],试写出H3BO3在溶液中的电离方程式:__________。
(4)“浸取”后,采用“热过滤”的目的是_________________________,母液中的主要溶质有______________。
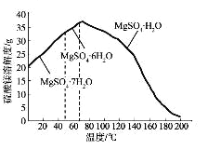
(5)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4·H2O,应采取的 措施是将“母液”蒸发浓缩,____________
(6)测定所得产品的纯度:取ag 硼酸,小心加热使其分解脱去水分(杂质受热不分解),得残留固体bg,则产品的纯度为_____。
-
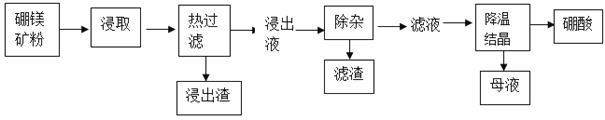
硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO•B2O3•H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如图:
已知:i.Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4.
ⅱ.H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g.
(1)为了提高硼镁矿粉的浸出率,可采取的措施有___________(至少答两条).
(2)“浸出液”显酸性,含H3BO3和Mg2+、SO42﹣,还含有Fe3+、Fe2+、Ca2+、Al3+等杂质.“除杂”时向浸出液中依次加入适量H2O2和MgO,H2O2的作用是_______________________ (用离子方程式表示),MgO除去的杂质离子是____________________.
(3)已知H3BO3与过量的NaOH反应生成Na[B(OH)4],试写出H3BO3在溶液中的电离方程式_______________________.
(4)“浸取”后,采用“热过滤”的目的是______________,母液中的主要溶质有___________、___________(主要由两种).
(5)测定所得产品的纯度:取a g硼酸,小心加热使其分解脱去水分(杂质受热不分解),得残留固体b g,则产品的纯度为__________________.
-
在实验室以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料制备硼酸(H3BO3),其流程如图1所示,硫酸镁和硼酸的溶解度随温度的变化曲线如图2所示。
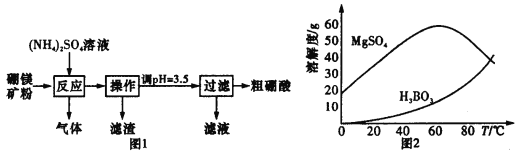
请回答下列问题:
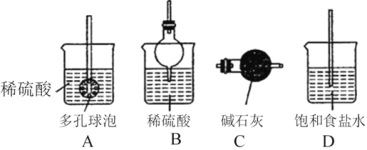
(1)流程中“反应”的实验装置如下图所示:
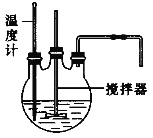
①反应时需控制在95℃进行,控制反应温度的适宜方法是____________________。
②反应产生的气体需要净化处理,请从下图中选择合适的装置__________(填字母代号)。

(2)实验中得到的粗硼酸还需要重结晶进行提纯,重结晶得到的母液可以在下一次重结晶时重复使用,但达到一定次数后必须净化处理,原因是______________________。
(3)实验时若被强碱溅到,先用大量水冲洗,水洗后再涂上硼酸溶液,写出有关离子方程式:____________。
(4)滴定硼酸时不能直接滴定,因为硼酸是很弱的酸,Ka=5.7×10-10。滴定前,须先将硼酸与甘油作用生成甘油硼酸,Ka=8.4×10-6,然后用酚酞作指示剂,再用NaOH标准溶液滴定。已知硼酸的摩尔质量为61.8 g·mol-1,滴定前称取3.00 g硼酸试样,配成250mL溶液,每次取25.00mL于锥形瓶中滴定,消耗0.200 0 mol·L-1 NaOH标准液的平均体积为20.00 mL。
①计算所得硼酸的纯度=__________。
②若用NaOH标准溶液直接滴定硼酸,则硼酸的纯度将__________(填字母代号)。
A.偏大 B.偏小 C.无影响 D.无法确定
-
以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料制备硼酸(H3BO3)。
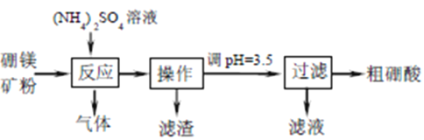
请回答下列问题:
(1)流程中“反应”的实验装置如图所示:
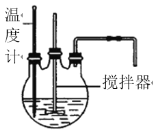
①反应时需控制在95℃进行,控制反应温度的适宜方法是____。
②反应产生的气体需要净化处理,请从图中选择合适的装置____(填字母代号)。
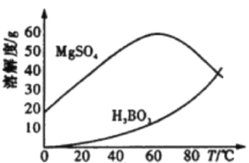
(2)根据如图所示,流程中“过滤”操作的适宜温度是________(填字母代号)。
A.0-20℃ B.20-40℃ C.50-60℃ D. 60-80℃
(3)根据H3BO3的电离反应:H3BO3+H2O H++B(OH)4-,Ka=5.7×10-10,可判断H3BO3是____酸;将溶液pH调解至3.5目的是____。
H++B(OH)4-,Ka=5.7×10-10,可判断H3BO3是____酸;将溶液pH调解至3.5目的是____。
(4)实验时若被强碱溅到皮肤,先用大量水冲洗,水洗后再涂上硼酸溶液,写出有关离子方程式:____。
(5)实验中得到的粗硼酸还需要重结晶进行提纯,重结晶得到的母液可以在下一次重结晶时重复使用,但达到一定次数后必须净化处理,原因是____。
(6)预测定硼酸的纯度,因硼酸酸性过弱不能直接滴定。可先将硼酸与甘油作用生成甘油硼酸(Ka=8.4×10-6),再用NaOH标准溶液滴定(酚酞作指示剂)。已知硼酸的摩尔质量为61.8g·mol-1,滴定前称取3.00g硼酸试样,配成250mL溶液,每次取25.00mL于锥形瓶中滴定,消耗0.2000mol·L-1NaOH标准液的平均体积为20.00mL。
①计算所得硼酸的纯度____
②若用NaOH标准溶液直接滴定硼酸,测得的硼酸的纯度将____(填字母代号)。
A.偏大 B.偏小 C.无影响 D.无法确定
-
硼是动植物所必须的微量元素,其单质和化合物广泛应用于冶金、机械、化工、核工业、医药、农业等部门。利用硼镁矿(主要成分为Mg2B2O3·5 H2O) 制取制硼酸、金属镁及粗硼的工艺流程图如下:
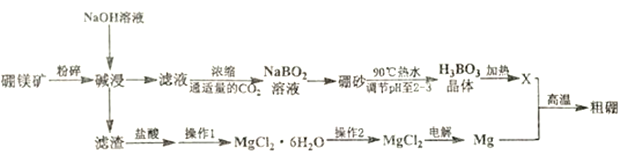
已知:①硼砂为Na2B4O7·10H2O
②硼酸(H3BO3) 是一种可溶于水的一元弱酸,与过量的NaOH 反应生成Na[B(OH)4]
③硼酸在不同温度下的溶解度:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 溶解度(g/100g 水) | 3 | 3 | 5 | 7 | 9 | 11 | 15 | 18 | 23 | 29 |
(1) 粉碎硼铁矿的目的是:______________; Mg2B2O5·H2O 中B 的化合价为: ______价。
(2) 滤渣的主要成分是: ________
(3)硼酸的电子式: ________;写出硼酸在水中电离的方程式: ________________;
(4)X 为硼酸晶体加热完全脱水后的产物,其与Mg反应制取粗硼的化学方程式为: ________;
(5) 硼砂溶于90℃ 热水后,常用稀硫酸调pH 至2~ 3(酸性)制取HBO3晶体,该反应的离子方程式为: ________________;从上述溶液中获得H3BO3 晶体的操作: ________________。

H++B(OH)−4,Ka=5.81×10−10,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。















