-
常温下取0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。HA和HB的1L溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是
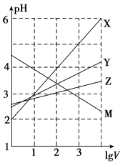
A.X是HA,M是HB
B.常温下pH:NaA溶液>NaB溶液
C.常温下,对于 的值(R代表A或B),一定存在HA>HB
的值(R代表A或B),一定存在HA>HB
D.若常温下浓度均为0.1mol/L的NaA和HA的混合溶液的pH>7,则c(A-)>c(HA)
-
取浓度均为0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。将浓度均为0.1mol/L、体积均为1L的HA溶液和HB溶液分别加水稀释至体积为VL,溶液pH的变化曲线如图所示,则下列说法正确的是
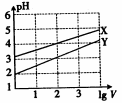
A.HA是强酸,HB是弱酸
B.X是HB,Y是HA
C.常温下,pH相等的NaA溶液与NaB溶液的物质的量浓度:c(NaA)<c(NaB)
D.NaA与NaB的混合溶液中:c(Na+)+c(H+)=c(A-)+c(B-)+c(HA)+c(HB)
-
常温下,取0.1mol/L的NaA和NaB 两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。HA和HB 的1L 溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是
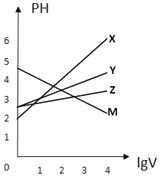
A. 相同条件下,对于c(R-)/[c(HR)·c(OH-)]的值(R代表A或B),一定存在HA>HB
B. 常温下pH: NaA 溶液>NaB 溶液
C. X是HA,M是HB
D. 若常温下浓度均为0.1mol/L 的NaA和HA 的溶液等体积混合,则c(A-)+c(HA)=0.2mol/L
-
常温下,取0.1mol/L的NaA和NaB 两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。HA和HB 的1L 溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是

A. 相同条件下,对于c(R-)/[c(HR)·c(OH-)]的值(R代表A或B),一定存在HA>HB
B. 常温下pH: NaA 溶液>NaB 溶液
C. X是HA,M是HB
D. 若常温下浓度均为0.1mol/L 的NaA和HA 的溶液等体积混合,则c(A-)+c(HA)=0.2mol/L
-
常温下,取0.1mol/L的NaA和NaB 两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。HA和HB 的1L 溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是
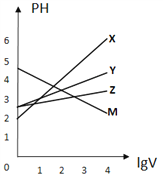
A. 相同条件下,对于c(R-)/[c(HR)·c(OH-)]的值(R代表A或B),一定存在HA>HB
B. 常温下pH: NaA 溶液>NaB 溶液
C. X是HA,M是HB
D. 若常温下浓度均为0.1mol/L 的NaA和HA 的溶液等体积混合,则c(A-)+c(HA)=0.2mol/L
-
常温下取0.1mol/L的NaA和NaB 两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O HA+NaHCO3、2NaB+CO2+H2O
HA+NaHCO3、2NaB+CO2+H2O 2HB+N2CO3。HA和HB 的1L 溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是
2HB+N2CO3。HA和HB 的1L 溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是
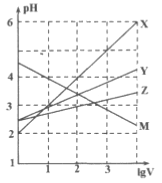
A. X是HA,M是HB
B. 常温下pH: NaA 溶液>NaB 溶液
C. 对于c(R-)/c(HR)·c(OH-)的值(R代表A或B),一定存在HA>HB
D. 若常温下浓度均为0.1mol/L 的NaA和HA 的混合溶液的pH>7,则c(A-)>c(HA)
-
常温下,向等物质的量浓度的两种一元酸的盐溶液中,分别通入少量的CO2,发生如下
反应:NaA+CO2+H2O===HA+NaHCO3 2NaB+CO2+H2O===2HB+Na2CO3,则等物质的量浓度的HA和HB在水中电离出H+的能力大小关系是 ( )
A.HA较强 B.HB较强
C.两者一样 D.无法比较
-
常温下(I)100mL0.1 mol/L的NaA溶液中的离子总物质的量为X,(Ⅱ)100 mL 0.1 mol/L的NaB溶液中的离子总物质的量为Y。下列推断正确的是
A.若X>Y,则酸性:HA>HB
B.若X=Y,则HB一定是强酸
C.若酸性:HA<HB,则X和Y关系不确定
D.若由水电离出的H+的浓度:(I)>(Ⅱ),则是X>Y
-
常温下(I)100mL0.1 mol/L的NaA溶液中的离子总物质的量为X,(Ⅱ)100 mL 0.1 mol/L的NaB溶液中的离子总物质的量为Y。下列推断正确的是
A.若X>Y,则酸性:HA>HB
B.若X=Y,则HB一定是强酸
C.若酸性:HA<HB,则X和Y关系不确定
D.若由水电离出的H+的浓度:(I)>(Ⅱ),则是X>Y
-
常温下,将HC1气体通入到1L浓度均为0.1mol/L的NaA和NaB的混合溶液中,混合溶液的pH与离子浓度变化的关系如图所示(忽略溶液体积的变化)。下列叙述不正确的是
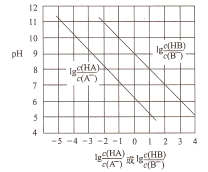
A. Ka(HB)的数量级为10-9
B. 酸性的强弱顺序为HCl>HA>HB
C. 当通入0.1molHC1气体时,c(B-)>c(A-)
D. 当混合溶液呈中性时,c(Na+)=c(Cl-)+c(A-)+c(B-)

的值(R代表A或B),一定存在HA>HB





