-
已知:2H2(g) + O2(g) = 2H2O(l) △H = -571.6 kJ·mol-1 ,CH4(g) + 2O2(g)= CO2(g) + 2H2O(l) △H = -890 kJ·mol-1 ,现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是
A.1:1 B.1:3 C.1:4 D.2:3
高二化学选择题中等难度题查看答案及解析
-
已知:2H2(g) + O2(g) = 2H2O(l) △H = -571.6 kJ·mol-1 ,CH4(g) + 2O2(g)= CO2(g) + 2H2O(l) △H = -890 kJ·mol-1 ,现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是
A.1:1 B.1:3 C.1:4 D.2:3
高二化学选择题困难题查看答案及解析
-
已知下列热化学方程式:
(1)CH4(g) + 2O2(g)== CO2(g) + 2H2O(l) △H= - 890.0kJ/mol
(2)2C2H6(g) + 7O2(g )==4CO2 (g)+ 6H2O(l) △H= - 3119.6kJ/mol
(3) C2H4(g) + 3O2(g) == 2CO2(g) + 2H2O(l) △H= - 1411.0kJ/mol
(4) 2C2H2(g) + 5O2(g)== 4CO2(g) + 2H2O(l) △H= - 2599.2kJ/mol
(5)C3H8(g) + 5O2(g)== 3CO2(g) + 4H2O(l) △H= - 2219.9kJ/mol
现有由上述五种烃中的两种组合成的混合气体2mol,经充分燃烧后放出2970.8kJ热量,则下列哪些组合是不可能的 ( )
A. CH4和C3H8 B. C2H4和C3H8 C. C2H6和C3H8 D. C2H6和CH4
高二化学单选题简单题查看答案及解析
-
下列叙述中,正确的是( )
A.甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g) + 2O2(g) === CO2(g) + 2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应,放热19.3 kJ,其热化学方程式为:
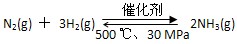 ΔH=-38.6 kJ·mol-1
ΔH=-38.6 kJ·mol-1C.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量
D.常温下,反应C(s) + CO2(g) === 2CO(g)不能自发进行,则该反应的ΔH>0
高二化学选择题简单题查看答案及解析
-
以NA代表阿伏加德罗常数,关于热化学方程式CH4(g) + 2O2 = CO2(g) + 2H2O(l) △H=—890 kJ/mol,下列说法中正确的是( )
A.有4NA个电子转移时,放出890 kJ的能量
B.有NA个C—H共价键断裂时,放出890 kJ的能量
C.有2NA个水分子生成且水为液体时,放出890 kJ的能量
D.有NA个C、O间的共用电子对生成时,放出890 kJ的能量
高二化学选择题中等难度题查看答案及解析
-
下列热化学方程式及有关应用的叙述中,正确的是
A. 甲烷的燃烧热为890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJ•mol-1
B. 已知强酸与强碱在稀溶液里反应的中和热为57.3kJ•mol-1,则1/2H2SO4(aq)+1/2Ba(OH)2(aq)═1/2BaSO4(s)+H2O(l) △H = -57.3kJ•mol-1
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)
2NH3(g) △H = -38.6kJ•mol-1
D. 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJ•mol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJ•mol-1,则O2比O3稳定
高二化学单选题中等难度题查看答案及解析
-
已知: 2H2O(l) = 2H2(g) + O2(g);△H =+571.6kJ/mol
CH4(g) + 2O2(g) = 2H2O(l) + CO2(g);△H =-890.3kJ/mol,
1克氢气和1克甲烷分别燃烧后,放出的热量之比约是 ( )
A.1:3.4 B.1:1.7 C.2.6:1 D.4.6:1
高二化学单选题中等难度题查看答案及解析
-
已知:2H2(g)+ O2(g)=2H2O(l) ΔH= -571.6KJ· mol-1
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH= -890KJ· mol-1
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695KJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1∶3 B.1∶4 C.1∶1 D.2∶3
高二化学单选题中等难度题查看答案及解析
-
已知:2H2(g)+ O2(g)=2H2O(l) ΔH=-571.6kJ· mol-1
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ· mol-1
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是:
A.1∶1 B.1∶3 C.1∶4 D.2∶3
高二化学选择题简单题查看答案及解析
-
已知:2H2(g)+ O2(g)=2H2O(l) ΔH=-571.6KJ· mol-1
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH=-890KJ· mol-1
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695KJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1∶1 B.1∶3 C.1∶4 D.2∶3
高二化学单选题中等难度题查看答案及解析