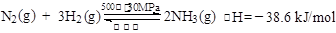-
下列叙述中,正确的是( )
A.甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1
B.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:
N2(g)+3H2(g) 2NH3(g)△H=-38.6 kJ•mol-1
2NH3(g)△H=-38.6 kJ•mol-1
C.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量
D.常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0
-
下列叙述中,正确的是( )
A.甲烷的标准燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2 (g)=CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1
B.500℃、30MPa下,将0.5 molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热193kJ,其热化学方程式为:N2+3H2 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
C.活化能的作用在于使反应物活化,所以化学反应的活化能不可能接近于零或等于零
D.常温下,反应C(s)+ CO2 (g)=2CO(g)不能自发进行,则该反应的△H>0
-
下列叙述中,正确的是
A.甲烷的标准燃烧热为890.3kJ/mol, 则甲烷燃烧的热化学方程式可表示为:
CH4(g)+ 2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ/mol
B.500 ℃ 、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热193kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
C.活化能的作用在于使反应物活化,所以化学反应的活化能不可能接近于零或等于零
D.常温下,反应C(s)+ CO2(g)=2CO(g)不能自发进行,则该反应的△H>0
-
下列叙述中,正确的是( )
A.甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g) + 2O2(g) === CO2(g) + 2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应,放热19.3 kJ,其热化学方程式为: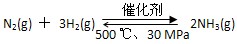 ΔH=-38.6 kJ·mol-1
ΔH=-38.6 kJ·mol-1
C.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量
D.常温下,反应C(s) + CO2(g) === 2CO(g)不能自发进行,则该反应的ΔH>0
-
下列说法正确的是:
A.甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g)ΔH=-38.6kJ·mol-1
2NH3(g)ΔH=-38.6kJ·mol-1
C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH相同
D.HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ/mol
-
下列说法正确的是
A. 甲烷的标准燃烧热为△H=﹣890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为 CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣890.3 kJ•mol-1
B. 从C(石墨)═C(金刚石)△H=+1.9kJ/mol,可知石墨比金刚石更稳定
C. 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0
D. HCl和NaOH反应的中和热 ΔH=-57.3 kJ•mol-1,则H2SO4和 Ba(OH)2 反应的中和热 ΔH=2×(-57.3) kJ•mol-1
-
下列说法正确的是:
A.甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g)ΔH=-38.6kJ·mol-1
2NH3(g)ΔH=-38.6kJ·mol-1
C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH相同
D.HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ/mol
-
下列说法正确的是
A.甲烷的标准燃烧热为-890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)===CO2(g)+2H2O(g) △H= -890.3 kJ/mol
B.500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: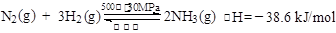
C.已知:2CO(g)+O2(g) ===2CO2(g) ΔH= -566 kJ/mol,下图可表示由CO生成CO2的反应过程和能量关系

D.已知:1mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1mol F-F 、S-F键需吸收的能量分别为160 kJ、330 kJ。已知1个 SF6(g)分子中含有6条S-F键。则:S(s)+3F2(g) ===SF6(g) △H=-1220 kJ/mol
-
下列热化学方程式正确的是
A. 甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 500 ℃、30 MPa 下,将0.5 mol N2 和 1.5 mol H2 置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g)ΔH=-38.6 kJ·mol-1
2NH3(g)ΔH=-38.6 kJ·mol-1
C. 已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为:H2(g)+ O2(g)
O2(g) H2O(g) ΔH=-242 kJ/mol
H2O(g) ΔH=-242 kJ/mol
D. CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)===2CO(g)+O2(g)反应的ΔH=+283.0 kJ·mol-1
-
下列说法正确的是( )
A. 甲烷的标准燃烧热为ΔH=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-890.3 kJ·mol-1
B. 已知H2O(L)=H2O(g) ΔH=+44kJ·mol-1,则2g H2(g)完全燃烧生成液态水比生成气态水多释放22kJ的能量
C. 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH<0
D. 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH相同
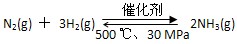 ΔH=-38.6 kJ·mol-1
ΔH=-38.6 kJ·mol-1