我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H将CO2高效还原为重要工业原料之一的甲醇,其反应机理如图所示。则下列有关说法不正确的是( )
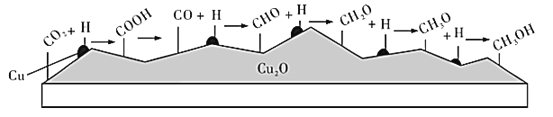
A.CO2生成甲醇是通过多步氧化反应实现的
B.该催化反应过程中涉及了化学键的形成及断裂
C.有可能通过调节控制反应条件获得甲醛等有机物
D.催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
高三化学单选题中等难度题
我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H将CO2高效还原为重要工业原料之一的甲醇,其反应机理如图所示。则下列有关说法不正确的是( )

A.CO2生成甲醇是通过多步氧化反应实现的
B.该催化反应过程中涉及了化学键的形成及断裂
C.有可能通过调节控制反应条件获得甲醛等有机物
D.催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
高三化学单选题中等难度题
我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H原子将CO2高效还原为重要工业原料之一的甲醇,反应机理如下图。下列有关说法不正确的是
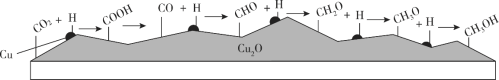
A. CO2生成甲醇是通过多步还原反应实现的
B. 催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
C. 该催化过程中只涉及化学键的形成,未涉及化学键的断裂
D. 有可能通过调控反应条件获得甲醛等有机物
高三化学单选题中等难度题查看答案及解析
我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H原子将CO2高效还原为重要工业原料之一的甲醇,反应机理如下图。下列有关说法不正确的是
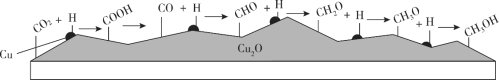
A. CO2生成甲醇是通过多步还原反应实现的
B. 催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
C. 该催化过程中只涉及化学键的形成,未涉及化学键的断裂
D. 有可能通过调控反应条件获得甲醛等有机物
高三化学单选题中等难度题查看答案及解析
我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H将CO2高效还原为重要工业原料之一的甲醇,其反应机理如图所示。则下列有关说法不正确的是( )

A.CO2生成甲醇是通过多步氧化反应实现的
B.该催化反应过程中涉及了化学键的形成及断裂
C.有可能通过调节控制反应条件获得甲醛等有机物
D.催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
高三化学单选题中等难度题查看答案及解析
“一碳化学”是指以研究分子中只含有一个碳原子的化合物(如CO、CO2、CH3OH等)为原料合成一系列化工产品的化学。
(一)工业上,在Cu2O/ZnO作催化剂的条件下发生反应:CO(g)+2H2(g)CH3OH(g) ΔH
(1)已知:CH3OH(l)=CH3OH (g) ΔH=+35.2 kJ·mol-1,根据下表:
| 物质 | H2(g) | CO(g) | CH3OH(l) |
| 燃烧热/kJ·mol-1 | -285.8 | -283.0 | -726.5 |
反应CO(g)+2H2(g)CH3OH(g)的ΔH=_____ kJ·mol-1。
(2)向2L恒容密闭容器中通入1molCO(g)和2molH2(g),发生反应合成甲醇,反应过程中n(CH3OH)与时间(t)及温度的关系如图所示。在500℃恒压条件下,请在图中画出反应体系中n(CH3OH)与时间(t)变化总趋势图________。
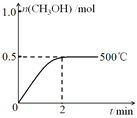
(二)CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应:
反应I:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH1= -48.5kJ·mol-1
反应II:CO2(g)+H2(g)CO(g)+H2O(g) ΔH2= +41.2kJ·mol-1
(3)控制CO2和H2初始投料比为1:3时,温度对CO2平衡转化率及甲醇和CO的产率的影响如图所示:
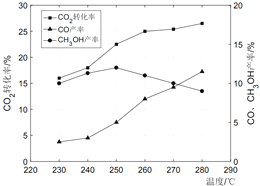
①由图可知温度升高CO产率上升,其主要原因是_____。
②由图可知获取甲醇最适宜的温度是_____。
(4)控制CO2和H2初始投料比为1:1.6,在300℃时,反应I已达到平衡状态,CO2的转化率为50%,甲醇的选择性为60%,此时容器体积为1.0L,若CO2初始加入量为2.0mol,则反应I的平衡常数是_____。
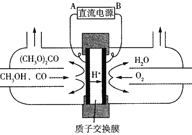
(三)以甲醇为主要原料电化学合成碳酸二甲酯[(CH3O)2CO]的反应原理如下:4CH3OH+2CO+O22(CH3O)2CO+2H2O
(5)由图可知B极为电源_____(填“正”或“负”)极,阳极电极反应式是_____。
高三化学综合题中等难度题查看答案及解析
化学与能源开发、环境保护、资源利用、生产生活密切相关。下列说法错误的是( )
A.研发使用高效催化剂,可提高反应中原料的转化率
B.绿色化学的核心是在化学合成中将原子充分利用,从源头上减少或消除污染
C.高纯硅及其氧化物在太阳能电池及信息高速传输中有重要应用
D.SO2是大气污染物,但葡萄酒中都含有一定量的SO2,SO2既可杀菌又可用来保鲜
高三化学选择题简单题查看答案及解析
化学源于生活,又高于生活。下列说法正确的是
A.绿色化学的核心是在化学合成中将原子充分利用,转化为新的原子
B.研发使用高效催化剂,可提高反应中原料的转化率
C.高纯度的晶体桂可以制备晶体管等半导体、电脑芯片
D.酒精、NaCl溶液、溶液、浓
都可使蛋白质发生变性
高三化学单选题中等难度题查看答案及解析
Cu2O是重要的催化剂和化工原料,工业上制备Cu2O的主要反应如下:
Ⅰ.C(g)+CO2(g)2CO(g) ΔH=+172.5kJ/mol
Ⅱ.CO(g)+2CuO(s)Cu2O(s)+CO2(g)ΔH=-138.0KJ/mol
请回答:
(1)C与CuO反应生成Cu2O和CO的热化学方程式为_____________,一定温度下,该反应在密闭容器中达到平衡后,只增大容器的容积,再次达到平衡时,CO的平衡浓度_________(填“增大”、“减小”或“不变”)。
(2)一定温度下,向5L恒容密闭容器中加入1molCO和2molCuO,发生反应Ⅱ.5min时达到平衡,测得容器中CuO的物质的量为0.8mol。
①0-5min内,用CO2表示的反应速率v(CO2)=___________.
②CO的平衡转化率a=____________.
(3)向5L密闭容器中加入1molC和1molCO2,发生反应Ⅰ。 CO2、CO的平衡体积分数(φ)与温度(T)的关系如图所示。
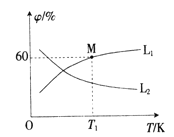
①能表示CO2的平衡体积分数与温度关系的曲线为___________(填"L1”或“L2”),理由为________。
②温度为T1时,该反应的平衡常数K=_____________。
(4)其他条件不变时,若水的分解反应用Cu2O作催化剂,则该反应的活化能_____(填“增大”、“减小”或“不变”,下同), 反应热(ΔH)____________。
高三化学综合题中等难度题查看答案及解析
我国自主研发对二甲苯的绿色合成路线取得新进展,其合成示意图如图。
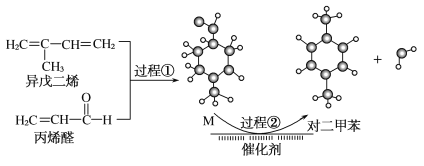
下列说法正确的是( )
A.过程①发生了取代反应
B.中间产物M的结构简式为
C.利用相同原理以及相同原料,也能合成邻二甲苯和间二甲苯
D.该合成路线原子利用率为100%,最终得到的产物易分离
高三化学单选题困难题查看答案及解析
我国自主研发对二甲苯的绿色合成路线取得新进展,其合成示意图如下。
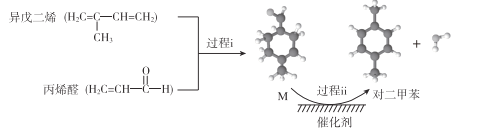
下列说法不正确的是
A. 过程i发生了加成反应
B. 中间产物M的结构简式为
C. 利用相同原理以及相同原料,也能合成邻二甲苯和间二甲苯
D. 该合成路线理论上碳原子100%利用,最终得到的产物易分离
高三化学单选题困难题查看答案及解析
我国自主研发对二甲苯的绿色合成路线取得新进展,其合成示意图如下。
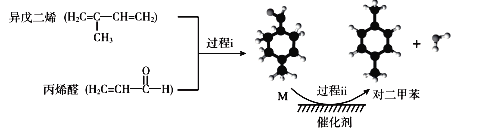
下列说法不正确的是( )
A.过程i发生了加成反应
B.中间产物M的结构简式为
C.利用相同原理以及相同原料,也能合成邻二甲苯和间二甲苯
D.该合成路线理论上碳原子100%利用,最终得到的产物易分离
高三化学单选题困难题查看答案及解析