-
合成氨对化学工业和国防工业具有重要意义。

(1)根据图1请写出合成氨的热化学方程式______ 热量用
热量用 、
、 或
或 表示
表示 。
。
(2)向合成塔中按物质的量之比l:4充入 、
、 进行氨的合成,图2为
进行氨的合成,图2为 时平衡混合物中氨气的体积分数与压强
时平衡混合物中氨气的体积分数与压强 的关系图。
的关系图。
①图2中氨气的体积分数为 时,
时, 的转化率为______。
的转化率为______。
②图3中 ,则温度为
,则温度为 时对应的曲线是______
时对应的曲线是______ 填“a”或“b”
填“a”或“b” 。
。
(3)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为 ,一定温度下,在体积为2L的恒容容器中发生上述反应,各物质的物质的量变化如表:
,一定温度下,在体积为2L的恒容容器中发生上述反应,各物质的物质的量变化如表:
①分析表中数据,判断5min时反应是否处于平衡状态?______ 填“是”或“否”
填“是”或“否” ,前5min反应的平均反应速率
,前5min反应的平均反应速率 ______。
______。
②在相同实验条件下,若改为加入 ,若要求平衡后
,若要求平衡后 在反应混合气中质量分数不变,则还需加入的物质及其物质的量为______。
在反应混合气中质量分数不变,则还需加入的物质及其物质的量为______。
③反应在 内,CO的物质的量减少的原因可能是______
内,CO的物质的量减少的原因可能是______ 填字母
填字母 。
。
 减少
减少 的物质的量
的物质的量  降低温度
降低温度  升高温度
升高温度  充入
充入
④下列方法中可以证明上述已达平衡状态的是______。
 单位时间内生成
单位时间内生成 的同时生成
的同时生成
b.容器内压强不再变化
 混合气体密度不再变化
混合气体密度不再变化
 混合气体的平均相对分子质量不再变化
混合气体的平均相对分子质量不再变化
 的质量分数不再变化
的质量分数不再变化
⑤已知碳的气化反应在不同温度下平衡常数的对数值 如表:
如表:
| 气化反应式 | lgK |
| 700K | 900K | 1200K |
| 
| 
| 
| 
|
| 
| 
| 
| 
|
则反应 在900K时,该反应平衡常数的对数值
在900K时,该反应平衡常数的对数值 ______。
______。
-
根据你学习的有关氨的知识,完成下面的问题。
(1)合成氨对化学工业具有重要意义。写出氨的两种重要用途_________;__________。
(2)实验室制备氨气,下列方法中最适宜选用的是______________。
①固态氯化氨加热分解
②固体氢氧化钠中滴加浓氨水
③氯化氨溶液与氢氧化钠溶液共热
④固态氯化氨与氢氧化钙混和加热
-
可逆反应N2+3H2
 2NH3是工业上合成氨的重要反应.
2NH3是工业上合成氨的重要反应.
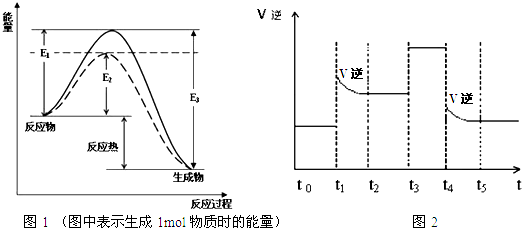
(1)根据图1请写出合成氨的热化学方程式______(热量用E1、E2或E3表示)
(2)图1中虚线部分是通过改变化学反应中的______条件,请解释原因______.
(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率与反应过程的关系,其中表示平衡混合物中NH3的含量最高的一段时间是______
(4)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为______.若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是______(“正向移动”“逆向移动”或“不移动”)
(5)将上述实验中产生的NH3通入到0.04mol•L-1的FeCl3溶液中,要使溶液中Fe3+沉淀较完全(即Fe3+浓度降至原来的千分之一),则溶液的pH为______(已知常温下,Fe(OH)3的溶度积常数Ksp=4×10-38)
-
(14分)可逆反应N2+3H2 2NH3是工业上合成氨的重要反应。
2NH3是工业上合成氨的重要反应。

(1)根据图1请写出合成氨的热化学方程式________(热量用E1、E2或E3表示)
(2)图1中虚线部分是通过改变化学反应中的________条件,请解释原因________
________。
(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率与反应过程的关系,其中表示平衡混合物中NH3的含量最高的一段时间是________
(4)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为________。若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是________(“正向移动”“ 逆向移动”或“不移动”)
(5)将上述实验中产生的NH3通入到0.04mol·L-1的FeCl3溶液中,要使溶液中Fe3+沉淀较完全(即Fe3+浓度降至原来的千分之一),则溶液的pH为________(已知常温下,Fe(OH)3的溶度积常数Ksp=4×10-38)
-
某课外小组在实验室制备氨气,并进行有关氨气的用途及性质的探究。
(1)写出实验室制取氨气的化学方程式:________。
(2)合成氨对化学和国防工业具有重要意义。写出氨的两种重要用途:
①________ ②________。
(3)该小组同学设计下图所示装置探究氨气的还原性。

①氨催化氧化的化学方程式为。
②若实验时通入氨气的速率过快,在烧瓶中会出现白烟,该物质的化学式为________。
(4)该小组同学欲以氨气和二氧化碳为原料制备少量较纯净的碳酸铵溶液设计如下甲 乙两方案。
①甲方案:先将二氧化碳通入水中,充分溶解后,再通入氨气;
乙方案:先将氨气通入水中,充分溶解后,再通入二氧化碳。
合理的方案是:________,理由是________。
②检验产物中有NH4+的方法为________。
③用氢键表示式写出氨水中存在的所有氢键________。
-
化学反应原理在工业生产中具有十分重要的意义.
(1)合成氨用的氢气有多种制取方法:请你写出用C制备水煤气的化学反应方程式______ CO↑+H2↑
-
合成氨工业对国民经济和社会发展具有重要意义,对于密闭容器中的反应:
(1)写出该反应的逆反应的化学平衡常数表达式______,升高温度,该反应化学反应速率______,氢气的转化率______ 以上均填“增大”、“减小”或“不变”
以上均填“增大”、“减小”或“不变” 。实际生产中温度一般控制在
。实际生产中温度一般控制在 ,原因是______。
,原因是______。
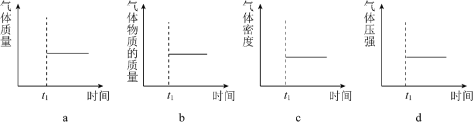
(2)能表示该反应在恒温恒容密闭容器中 时刻后已经达到平衡状态的图示是______。
时刻后已经达到平衡状态的图示是______。
(3)浓度 的氨水,pH为
的氨水,pH为 当用蒸馏水稀释100倍时,则
当用蒸馏水稀释100倍时,则 的电离平衡将向______方向移动
的电离平衡将向______方向移动 填“正”或“逆”
填“正”或“逆” ,溶液的pH将为______
,溶液的pH将为______ “大于”“小于”“等于”
“大于”“小于”“等于” 。
。
设计一个简单实验,证明一水合氨是弱碱:______。
某化学兴趣小组进行了下列关于氯化铵的课外实验:
(实验操作)

浸过氯化钠溶液的布条很快烧光,浸过氯化铵溶液的布条不燃烧,冒出白烟。
(4)氯化铵饱和溶液中离子浓度由大到小的顺序是______。白烟的成分是______。
(5)请推测浸过氯化铵溶液的布条不燃烧、不易着火的主要原因 写出一条即可
写出一条即可 ______
______
-
合成氨工业对国民经济和社会发展具有重要意义,对于密闭容器中的反应:
(1)写出该反应的逆反应的化学平衡常数表达式______,升高温度,该反应化学反应速率______,氢气的转化率______ 以上均填“增大”、“减小”或“不变”
以上均填“增大”、“减小”或“不变” 。实际生产中温度一般控制在
。实际生产中温度一般控制在 ,原因是______。
,原因是______。
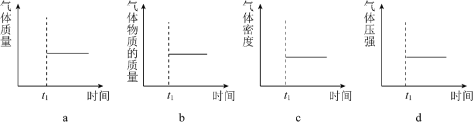
(2)能表示该反应在恒温恒容密闭容器中 时刻后已经达到平衡状态的图示是______。
时刻后已经达到平衡状态的图示是______。
(3)浓度 的氨水,pH为
的氨水,pH为 当用蒸馏水稀释100倍时,则
当用蒸馏水稀释100倍时,则 的电离平衡将向______方向移动
的电离平衡将向______方向移动 填“正”或“逆”
填“正”或“逆” ,溶液的pH将为______
,溶液的pH将为______ “大于”“小于”“等于”
“大于”“小于”“等于” 。
。
设计一个简单实验,证明一水合氨是弱碱:______。
某化学兴趣小组进行了下列关于氯化铵的课外实验:
(实验操作)

浸过氯化钠溶液的布条很快烧光,浸过氯化铵溶液的布条不燃烧,冒出白烟。
(4)氯化铵饱和溶液中离子浓度由大到小的顺序是______。白烟的成分是______。
(5)请推测浸过氯化铵溶液的布条不燃烧、不易着火的主要原因 写出一条即可
写出一条即可 ______
______
-
合成氨工业对化学工业和国防工业具有重要意义.
(1)常温下氨气极易溶于水,其水溶液可以导电.
①用方程式表示氨气溶于水的过程中存在的可逆过程______
②氨水中水电离出的c(OH-)______10-7mol/L(填写“>”、“<”或“=”)
③将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大到依次为______.
(2)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B.A为铵盐,B在标准状况下为气态.在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96L氨气(标准状况),同时生成0.3molA.
①写出氨气和氟气反应的化学方程式______ NF3+3NH4F(催化剂要注明是铜)
-
合成氨工业对国民经济和社会发展具有重要意义,对于密闭容器中的反应:N2(g)+3H2(g) 2NH3(g)+Q
2NH3(g)+Q
(1)写出该反应的逆反应的化学平衡常数表达式_____,升高温度,该反应化学反应速率_____,氢气的转化率____(以上均填“增大”、“减小”或“不变”)。实际生产中温度一般控制在500℃,原因是__________。
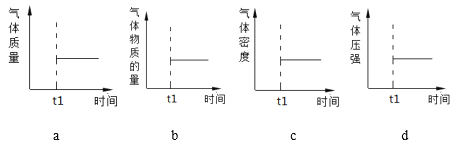
(2)能表示该反应在恒温恒容密闭容器中t1时刻后已经达到平衡状态的图示是________。
(3)浓度0.1mol/L的氨水,pH为11。当用蒸馏水稀释100倍时,则NH3·H2O的电离平衡将向______方向移动(填“正”或“逆”),溶液的pH将为____9(“大于”“小于”“等于”)。设计一个简单实验,证明一水合氨是弱碱:____________。

热量用
、
或
表示
。
、
进行氨的合成,图2为
时平衡混合物中氨气的体积分数与压强
的关系图。
时,
的转化率为______。
,则温度为
时对应的曲线是______
填“a”或“b”
。
,一定温度下,在体积为2L的恒容容器中发生上述反应,各物质的物质的量变化如表:
填“是”或“否”
,前5min反应的平均反应速率
______。
,若要求平衡后
在反应混合气中质量分数不变,则还需加入的物质及其物质的量为______。
内,CO的物质的量减少的原因可能是______
填字母
。
减少
的物质的量
降低温度
升高温度
充入
单位时间内生成
的同时生成
混合气体密度不再变化
混合气体的平均相对分子质量不再变化
的质量分数不再变化
如表:
在900K时,该反应平衡常数的对数值
______。







