-
滴定法不仅适合于酸碱中和滴定,还可以用于氧化还原滴定和沉淀滴定。
I. 甲同学根据反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O,进行测定H2C2O4溶液的物质的量浓度的实验。实验步骤如下:
①取待测H2C2O4溶液25.00 mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1 mol/L KMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00 mL。请回答:
(1)滴定时,将KMnO4溶液装在 __________(填“酸式”或“碱式”)滴定管中。
(2)滴定过程中眼睛注视 __________。
(3)计算H2C2O4溶液的物质的量浓度为 ________mol/L。
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 _________(填字母代))。
A 滴定终点读数时俯视 B 取用待测液的滴定管水洗后未用待测液润洗
C 锥形瓶水洗后未干燥 D 装标准液的滴定管尖嘴部分有气泡,滴定后消失
II. 已知:
AgCl
AgBr
AgSCN
Ag2CrO4
AgCN
溶解度(mol/L)
1.34×10-6
7.1×10-7
1.0×10-6
6.5×10-5
1.1×10-8
颜色
白
淡黄
白
砖红
白
(5)①乙同学参照上表已知信息用硝酸银标准溶液滴定氯离子含量时可以作指示剂的是_______(填字母代号)。
a CaCl2 b NaBr c NaCN d K2CrO4
②滴定达终点的现象是___________。
高二化学实验题简单题查看答案及解析
-
滴定法是解决化学分析问题的常用方法。滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
I.如图为某浓度的NaOH溶液滴定10.00mL一定浓度的盐酸的示意图。根据图像分析:
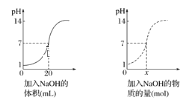
(1)HCl溶液的浓度是__________;NaOH溶液的浓度是_______;
(2)x=________。
(3)若向20mL稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是________(填字母)。
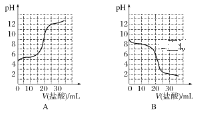

ΙΙ.氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。
(4)人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度,抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
滴定的实验数据如下所示:
实验编号
待测血液的体积/mL
滴入KMnO4溶液的体积/mL
1
20.00
11.95
2
20.00
13.00
3
20.00
12.05
①滴定时,盛放高锰酸钾溶液的仪器名称为_________确定反应达到终点的现象_____________。
②草酸跟酸性KMnO4溶液反应的离子方程式为:2MnO42-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,根据所给数据计算血液样品中Ca2+离子的浓度为__________mg/cm3
高二化学实验题中等难度题查看答案及解析
-
滴定法是化学上常用的定量分析的方法,滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
Ⅰ.甲化学兴趣小组取20.00 mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用0.200 0 mol·L-1的标准NaOH溶液进行滴定,重复上述滴定操作3次,并记录数据。
(1)滴定时边滴边摇动锥形瓶,眼睛应观察________。(填标号)
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)判断滴定终点的现象是_________________。
(3)根据表中数据,计算待测盐酸溶液的浓度为________ mol·L-1。
滴定次数
待测液体积(mL)
标准NaOH溶液读数记录(mL)
滴定前读数
滴定后读数
第一次
20.00
0.40
20.40
第二次
20.00
4.00
24.00
第三次
20.00
2.00
24.10
Ⅱ.乙化学兴趣小组利用氧化还原反应滴定,测定了某工厂废水中游离态氯的含量。实验如下:
①取水样10.0 mL于锥形瓶中,加入10.0 mL的KI溶液(足量),滴入指示剂2~3滴。
②将自己配制的0.01 mol·L-1标准Na2S2O3溶液装入滴定管中,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,试回答下列问题:
(4)步骤①发生的化学反应方程式为__________;加入的指示剂是____________。
(5)步骤②应使用________式滴定管。
(6)氯的所测浓度比实际浓度会偏大,造成误差的原因可能是________。(填标号)
A.配制标准Na2S2O3溶液定容时,加水超过刻度线
B.锥形瓶水洗后直接装待测水样
C.装标准Na2S2O3溶液的滴定管水洗后没有润洗
D.滴定到达终点时,俯视读出滴定管读数
E.滴定前尖嘴部分有气泡,滴定后消失
高二化学实验题中等难度题查看答案及解析
-
滴定法是化学上常用的定量实验的方法。滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
I.甲化学兴趣小组取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用0.2000 mol/L的标准NaOH溶液进行滴定。重复上述滴定操作3次,并记录数据。
(1)滴定时边滴边摇动锥形瓶,眼睛应观察___________。(填序号)
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)判断滴定终点的现象是:________________________。
(3)根据下列数据:请计算待测盐酸溶液的浓度为___________mol/L。
滴定次数
待测液体积(mL)
标准NaOH溶液读数记录(mL)
滴定前读数
滴定后读数
第一次
20.00
0.40
20.40
第二次
20.00
4.00
24.00
第三次
20.00
2.00
24.10
II.乙化学兴趣小组利用氧化还原反应滴定,测定了某工厂废水中游离态氯的含量。实验如下:
①取水样10.0 ml于锥形瓶中,加入10.0 ml的KI溶液(足量),滴入指示剂2~3滴。
②将自己配制的0.01mol·L-1标准Na2S2O3溶液装入滴定管中,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+ 2Na2S4O6。
试回答下列问答:
(1)步骤①发生的化学反应的离子方程式为:_____________;加入的指示剂是_____________。
(2)步骤②应使用_________式滴定管。
(3)氯的所测浓度比实际浓度会偏大,造成误差的原因可能是_________(填序号)
A 配制标准Na2S2O3溶液定容时,加水超过刻度
B 锥形瓶水洗后直接装待测水样
C 装标准Na2S2O3溶液的滴定管水洗后没有润洗
D 滴定到达终点时,俯视读出滴定管读数;
E 滴定前尖嘴部分有气泡,滴定后消失
III.沉淀滴定所用的指示剂本身就是一种沉淀剂。已知一些银盐的颜色和Ksp(20℃)如下,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定。
化学式
①AgCl
②AgBr
③AgI
④Ag2S
⑤Ag2CrO4
颜色
白色
浅黄色
黄色
黑色
红色
Ksp
2.0×10-10
5.4×10-13
8.3×10-17
2.0×10-48
2.0×10-12
(1)滴定时,你认为该滴定适宜选用的指示剂是下列中的__________。
A.KBr B.KI C.K2S D.K2CrO4
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
=_______________ 。
高二化学实验题困难题查看答案及解析
-
滴定法是化学上常用的定量分析的方法。滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
I.甲化学兴趣小组取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用0.2000 mol·L-1的标准NaOH溶液进行滴定。重复上述滴定操作3次,并记录数据。
(1)滴定时边滴边摇动锥形瓶,眼睛应观察________。(填序号)
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)判断滴定终点的现象是:_____________________。
(3)根据下列数据:请计算待测盐酸溶液的浓度为________mol/L。
滴定次数
待测液体积(mL)
标准NaOH溶液读数记录(mL)
滴定前读数
滴定后读数
第一次
20.00
0.40
20.40
第二次
20.00
4.00
24.00
第三次
20.00
2.00
24.10
II.乙化学兴趣小组利用氧化还原反应滴定,测定了某工厂废水中游离态氯的含量。实验如下:
①取水样10.0 ml于锥形瓶中,加入10.0 ml的KI溶液(足量),滴入指示剂2~3滴。
②将自己配制的0.01mol·L-1标准Na2S2O3溶液装入滴定管中,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+ 2Na2S4O6。试回答下列问答:
(1)步骤①发生的化学反应方程式为:_______________;加入的指示剂是_______。
(2)步骤②应使用_________式滴定管。
(3)氯的所测浓度比实际浓度会偏大,造成误差的原因可能是______(填序号)
A 配制标准Na2S2O3溶液定容时,加水超过刻度线
B 锥形瓶水洗后直接装待测水样
C 装标准Na2S2O3溶液的滴定管水洗后没有润洗
D 滴定到达终点时,俯视读出滴定管读数;
E 滴定前尖嘴部分有气泡,滴定后消失
III.沉淀滴定所用的指示剂本身就是一种沉淀剂。已知一些银盐的颜色和Ksp(20℃)如下表,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定。
化学式
AgCl
AgBr
AgI
Ag2S
Ag2CrO4
颜色
白色
浅黄色
黄色
黑色
红色
Ksp
2.0×10-10
5.4×10-13
8.3×10-17
2.0×10-48
2.0×10-12
(1)滴定时,你认为该滴定适宜选用的指示剂是下列中的___________。(填序号)
A.KBr B.KI C.K2S D.K2CrO4
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
=__________。
高二化学实验题困难题查看答案及解析
-
滴定实验是化学学科中最重要的定量实验之一。常见的滴定实验有酸碱中和滴定、氧化还原反应滴定、沉淀滴定等。
(1)酸碱中和滴定:
某学生用0.1000mol/LNaOH溶液测定醋酸的浓度,滴定前滴定管内液面读数为1.10mL,滴定后液面如图,则标准液VNaOH为____________。
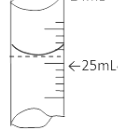
(2)氧化还原滴定:
葡萄酒常用Na2S2O5作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:(注:实验中加入盐酸是将Na2S2O5全部转化成SO2)

①滴定时,I2溶液应装在_______________ (“酸”或“碱”)式滴定管中。
②用离子方程式表示上述滴定过程中的原理___________________________________,滴定终点时滴定现象是__________________________________________________。
③下列情形会造成测定结果偏高的是_________________________。
A.滴定持续时间稍长,溶液中部分HI被空气氧化
B.滴定前平视,滴定后俯视
C.盛装标准I2溶液的滴定管用蒸馏水洗净后,未润洗
D.滴定前滴定管尖嘴有气泡,滴定后气泡消失
(3) 沉淀滴定:滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是_______________(选填字母)。

A.NaCl B.NaBr C.NaCN D.Na2CrO4
高二化学实验题困难题查看答案及解析
-
滴定实验是化学学科中最重要的定量实验之一。常见的滴定实验有酸碱中和滴定、氧化还原反应滴定、沉淀滴定等等。
(1)酸碱中和滴定——用0.1000mol/LHCl标准溶液测定某NaOH溶液的物质的量浓度(用酚酞作指示剂),做了三组平行实验,数据记录如下:
实验序号
待测NaOH溶液的体积/mL
0.1000mol/LHCl溶液的体积/mL
滴定前刻度
滴定后刻度
1
25.00
0.00
25.01
2
25.00
1.56
26.56
3
25.00
0.21
25.20
计算出待测NaOH溶液的物质的量浓度为 _____________________________(小数点后保留四位)。
(2)氧化还原滴定——葡萄酒中抗氧化剂残留量的测定,葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
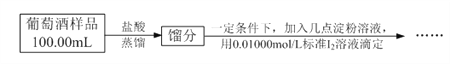
注:实验中加入盐酸的目的是将Na2S2O5全部转化成SO2;滴定过程中发生的反应是:I2 + SO2 + 2H2O
2HI + H2SO4
①滴定时,I2溶液应装在__________(“酸”或“碱”)式滴定管中,判断滴定终点的方法是:当滴入最后一滴碘溶液时,溶液由_________________________,且保持30s不变。
②实验消耗标准I2溶液25.00mL,所测样品中抗氧化剂的残留量(以游离SO2计算)为___________g/L。
③下列情形会造成测定结果偏高的是_____________。
A.滴定持续时间稍长,溶液中部分HI被空气氧化 B.滴定前平视,滴定后俯视
C.盛装标准I2溶液的滴定管用蒸馏水洗净后,未润洗
D.滴定前滴定管尖嘴有气泡,滴定后气泡消失
(3)沉淀滴定——滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是_____________(填选项字母)。
难溶物
AgCl
AgBr
AgCN
Ag2CrO4
AgSCN
颜色
白
浅黄
白
砖红
白
Ksp
1.77×10-10
5.35×10-13
1.21×10-16
1.12×10-12
1.0×10-12
A.NaCl B.NaBr C.NaCN D.Na2CrO4
高二化学实验题中等难度题查看答案及解析
-
滴定实验是化学学科中最重要的定量实验之一。常见的滴定实验有酸碱中和滴定、氧化还原反应滴定、沉淀滴定等等。
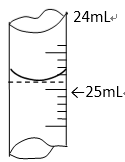
(1)酸碱中和滴定—用0.1000mol·L-1 HCl标准溶液测定某NaOH溶液的物质的量浓度(用酚酞作指示剂),请回答下列问题:
①若某学生在实验过程中,记录滴定前滴定管内液面读数为1.10mL,滴定后液面如图,则此时消耗标准溶液的体积为 ;
②该学生做了三组平行实验,数据记录如下:实验序号待测NaOH溶液的体积/mL 0.1000mol·L-1HCl溶液的体积/mL滴定前刻度 滴定后刻度
1 25.00 0.00 25.02
2 25.00 1.56 31.30
3 25.00 0.22 25.20
选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为 (小数点后保留四位);
(2)氧化还原滴定——葡萄酒中抗氧化剂残留量的测定葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

注:实验中加入盐酸的目的:将Na2S2O5全部转化成SO2。
①滴定时,I2溶液应装在 (“酸”或“碱”)式滴定管中,滴定终点时滴定现象是 。
②实验消耗标准I2溶液25.00mL,所测样品中抗氧化剂的残留量(以游离SO2计算)为 g/L。
③上述滴定过程中的原理为 (用离子方程式表示),下列情形会造成测定结果偏高的 。
A.滴定持续时间稍长,溶液中部分HI被空气氧化
B.滴定前平视,滴定后俯视
C.盛装标准I2溶液的滴定管用蒸馏水洗净后,未润洗
D.滴定前滴定管尖嘴有气泡,滴定后气泡消失
(3) 沉淀滴定——滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是 (填选项字母)。
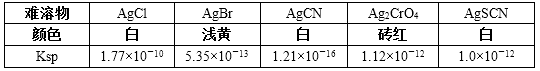
A.NaCl B.NaBr C.NaCN D.Na2CrO4
高二化学实验题困难题查看答案及解析
-
用中和滴定法测定某烧碱的纯度。将2.5g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成250mL溶液。根据实验回答下列问题:
I.滴定前的准备
检漏→用蒸馏水清洗→用待装溶液润洗→装液→①→调节液而在“0”刻度或“0”刻度以下→记录初始读数
II.滴定
分别取20.00mL待测液于3个洁净的锥形瓶中,滴加2滴酚酞试液,然后用0.2000mol·L-1盐酸标准液进行滴定至终点,记录最终读数。数据如下:
滴定序号
待测液体积(mL)
滴定前(mL)
滴定后(mL)
1
20.00
0.50
20.70
2
20.00
6.00
26.00
3
20.00
5.00
25.10
III.实验数据处理
(1)将步骤I中的操作补充完整:
①___________
(2)如图所示为___________ (填“酸式”或“碱式”)滴定管的一部分,若该滴定管漏水或转动不灵活,可采取的措施是___________
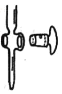
(3)滴定终点的现象是_______
(4)计算:NaOH溶液的浓度为_______mol·L-1烧碱样品的纯度为________
(5)试判断以下几种情况对烧碱纯度测定结果的影响(填“偏大”、“偏小”或“无影响”)
①若用蒸馏水冲洗锥形瓶,使测定结果_____________
②若滴定前滴定管尖嘴有气泡,滴定后气泡消失,使测定结果_____________
③若刚见到指示剂局部的颜色有变化就停止滴定,使测定结果_____________
④读数时,若滴定前仰视,滴定后俯视,使测定结果_____________
高二化学实验题简单题查看答案及解析
-
中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO4•7H2O)]中铁元素的含量。
①下列滴定装置中(夹持部分略去),最合理的是:__________(填字母序号)。
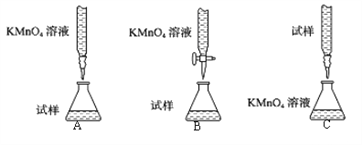
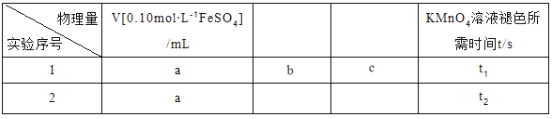
②该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10mol∙L-1FeSO4、0.02mol∙L-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。_____________、_____________、_____________、_____________。
(2)常温下,探究小组乙将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如图所示。
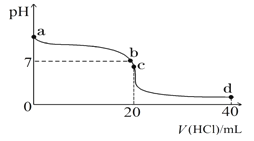
①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)=__________________。
②取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释:___________________________________。
③d点所示溶液中离子浓度由大到小的排序是_______________________________。
高二化学实验题中等难度题查看答案及解析