-
如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
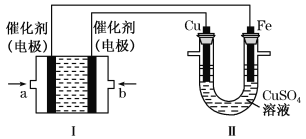
①a处应通入______(填“CH4”或“O2”),a处电极上发生的电极反应式是______________;
②电镀结束后,装置Ⅰ中溶液的pH _________ (填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度____________________;
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有________________ ;
④在此过程中若完全反应,装置Ⅱ中阴极质量变化6.4 g,则装置Ⅰ中理论上消耗甲烷__________L(标准状况下)。
-
甲烷是非常重要的能源和化工原料,请回答下列问题.
(1)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为H2SO4溶液),通过装置Ⅱ实现铁棒镀铜。
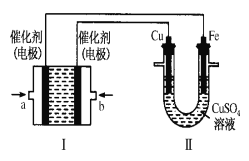
①a处应通入______(填“CH4”或“O2”),b处电极上发生的电极反应式是___________;
②电镀结束后,装置Ⅰ中溶液的pH______(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度_______;
③若实验过程中Ⅱ中的铜片质量减少了2.56g,则Ⅰ中理论上消耗CH4的体积(标准状况)______L。
(2)若将装置Ⅱ中的两电极均改为石墨惰性电极:
①写出装置Ⅱ中发生的总化学反应方式________________________________。
②若用Ⅱ电解200 mL 0.05 mol·L-1的CuSO4溶液,一段时间后溶液中的Cu2+恰好完全析出,恢复至室温,溶液pH=__________(忽略电解过程中溶液体积变化);若想将上述电解后的溶液恢复为与电解前的溶液相同,可以加入一定质量的__________(填序号);
a.Cu b.CuO c.Cu(OH)2 d.CuSO4
-
乙烷(C2H6)作为一种新能源在化学领域应用广泛,请回答下列问题:(如图所示,装置Ⅰ为乙烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。

①a处应通入______(填“C2H6”或“O2”),a处电极上发生的电极反应式是____________________________________;
②电镀结束后,装置Ⅰ中溶液的pH______(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度______;
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有___________(忽略水解);在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8 g,则装置Ⅰ中理论上消耗乙烷________L(标准状况下)。
-
用碱性氢氧燃料电池为电源进行电解的实验装置示意图如下所示。下列说法中正确的
是( )

A、燃料电池工作时,负极反应为:H2 – 2e-= 2H+
B、若要实现铁上镀铜,则a极是铁,b极是铜
C、若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D、a、b两极均是石墨时,在相同条件下当电池中消耗H2 22.4 L(标准状况)时,a极析出铜64 g
-
用碱性氢氧燃料电池为电源进行电解的实验装置示意图如下所示。下列说法中正确的是
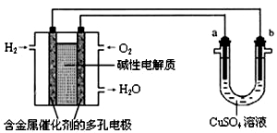
A.燃料电池工作时,负极反应为:H2-2e- = 2H+
B.若要实现铁上 镀铜,则a极是铁,b极是铜
镀铜,则a极是铁,b极是铜
C.若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D.a、b两极均是石墨时,在相同条件下当电池中消耗H222.4L(标准状况)时,a极析出铜64g
-
燃料电池是燃料(如CO、H2、CH4等)跟氧气(或空气)反应将化学能转变为电能的装置。下面关于甲烷燃料电池(KOH溶液为电解质溶液)的说法正确的是
A. 负极的电极反应式为O2+2H2O+4e-=4OH-
B. 随着放电的进行,溶液的pH不变
C. 负极的电极反应式为CH4+8OH--8e-=CO2+6H2O
D. 放电时溶液中的OH-向负极移动
-
燃料电池是燃料(如CO、H2、CH4)等跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,下列关于甲烷燃料电池的说法中不正确的是( )
A.通入氧气的一极发生还原反应,通入甲烷的一极发生氧化反应
B.负极的电极反应式为CH4+10OH--8e-=CO32—+7H2O
C.随着反应的进行,电解质溶液的pH保持不变
D.甲烷燃料电池的能量利用率比甲烷燃烧的大
-
燃料电池是燃料(如CO、H2、CH4)等跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,下列关于甲烷燃料电池的说法中不正确的是( )
A.通入氧气的一极发生还原反应,通入甲烷的一极发生氧化反应
B.负极的电极反应式为CH4+10OH--8e-===CO +7H2O
+7H2O
C.随着反应的进行,电解质溶液的pH保持不变
D.甲烷燃料电池的能量利用率比甲烷燃烧的大
-
燃料电池是燃料(如CO、H2、CH4等)跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,下列关于甲烷燃料电池的说法中不正确的是( )
A.通入氧气的一极发生还原反应,通入甲烷的一极发生氧化反应
B.负极的电极反应式为CH4+10OH--8e-═CO +7H2O
+7H2O
C.随着不断放电,电解质溶液的pH保持不变
D.甲烷燃料电池的能量利用率比甲烷燃烧的大
-
燃料电池是燃料(例如CO、H2、CH4等)跟氧气或空气反应,将此反应的化学能转化为电能的装置,电解质通常是KOH溶液,则下列关于甲烷燃料电池的说法正确的是
A. 负极反应式为:CH4+6OH--8e-===CO32-+5H2O
B. 正极反应式为:O2+4H++4e-===2H2O
C. 该电池的总反应与甲烷燃烧的反应方程式相同,反应式为:CH4+2O2===CO2+2H2O
D. 随着反应地进行,KOH溶液物质的量浓度减小




