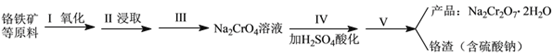-
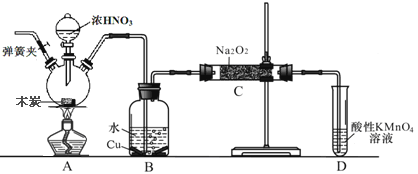
亚硝酸钠在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示(部分夹持装置略)。已知:
① 3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
② 酸性条件下,NO与NO2-都能与MnO4-反应生成NO3-和Mn2+;
(1)盛浓硝酸仪器的名称是___________________________。
(2)为避免B中逸出的气体中混有的杂质气体与Na2O2反应,应在B、C装置间增加一个装置,则该装置中盛放的药品名称为__________________。
(3)写出NO与Na2O2在常温下生成NaNO2的化学反应方程式__________________;当该反应中转移0.1mole-时,理论上吸收标准状况下NO的体积为_______L。
(4)将11.7g过氧化钠完全转化成亚硝酸钠,理论上至少需要木炭_______g。
(5)NO2易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。
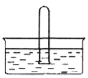
① NO2溶于水的化学方程式是______________________________________。
② 使试管中NO2完全被水吸收的操作是______________________________。
-
亚硝酸钠在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示(部分夹持装置略)。已知:

① 3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
② 酸性条件下,NO与NO2-都能与MnO4-反应生成NO3-和Mn2+;
(1)盛浓硝酸仪器的名称是___________________________。
(2)为避免B中逸出的气体中混有的杂质气体与Na2O2反应,应在B、C装置间增加一个装置,则该装置中盛放的药品名称为__________________。
(3)写出NO与Na2O2在常温下生成NaNO2的化学反应方程式__________________;当该反应中转移0.1mole-时,理论上吸收标准状况下NO的体积为_______L。
(4)将11.7g过氧化钠完全转化成亚硝酸钠,理论上至少需要木炭_______g。
(5)NO2易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。
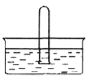
① NO2溶于水的化学方程式是______________________________________。
② 使试管中NO2完全被水吸收的操作是______________________________。
-
亚硝酸钠在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如右图所示(部分夹持装置略)。已知:
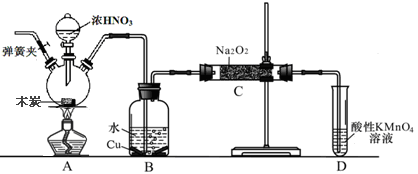
①3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
②酸性条件下,NO与NO3-都能与MnO4-反应生成NO3-和Mn2+;
完成下列填空:
(1)写出a仪器的名称___________________________。
(2)为避免B中逸出的气体中混有的杂质气体与Na2O2反应,应在B、C装置间增加一个装置,则该装置中盛放的药品名称为__________________。
(3)写出NO与Na2O2在常温下生成NaNO2的化学反应方程式______________________;当该反应中转移0.1mole-时,理论上吸收标准状况下NO的体积为__________L。
(4)将11.7g过氧化钠完全转化成亚硝酸钠,理论上至少需要木炭__________g。
(5)NO2易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见右图。
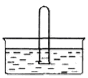
①NO2溶于水的化学方程式是_________________________。
②使试管中NO2完全被水吸收的操作是______________________________。
-
亚硝酸钠被称为工业盐,在漂白、电镀等方面应用广泛。NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸。
(1)写出亚硝酸的电离方程式___;
(2)酸性条件下,NaNO2与KI按物质的量1:1恰好完全反应,且I-被氧化为I2,则产物中含氮物质的化学式为__;
(3)请你设计一个实验方案鉴别氯化钠和亚硝酸钠(提示AgNO2呈白色,在溶液中以沉淀形式存在)___;
(4)工业废水中NO2-可用铝粉除去,产生无毒无味的气体。若反应过程中转移6mol电子,则生成该气体在标准状况下的体积为___L。
-
(本小题满分13分)碳酸钠俗称纯碱,在日常生活和生成中有着广泛的应用。某化学兴趣小组想根据所学知识模拟制备碳酸钠,方法如下:先以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3(反应的化学方程式为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl),然后再将NaHCO3制成Na2CO3。
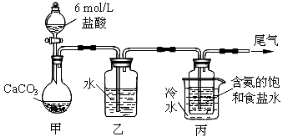
(1)装置乙的作用是 。
为防止污染空气,尾气中含有的 需要进行吸收处理。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有 、 、 。NaHCO3转化为Na2CO3的化学方程式为 。
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品19g完全溶于水制成溶液,然后向此溶液中不断滴加1mol·L-1的稀盐酸直到不再产生气泡,共消耗300ml稀盐酸。请回答下列问题:
根据实验的需要,用11.9mol·L-1的浓盐酸配制1mol·L-1的稀盐酸时,主要用到的玻璃仪器有烧杯、玻璃棒、①量筒、胶头滴管和 (填仪器名称);需要量取的浓盐酸体积为: mL。
②该样品中NaHCO3和Na2CO3的物质的量之比是 。
-
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。ClO2是一种黄绿色的气体,易溶于水。实验室以NH4C1、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
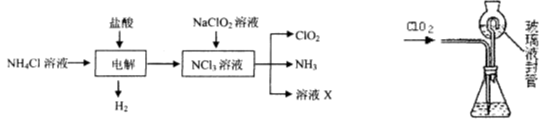
⑴ 写出电解时发生反应的化学方式: 。
⑵ 测定ClO2(如右图)的过程如下:在锥形瓶中加入足最的碘化钾,用100 mL水溶解后,再加3 mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去V mL硫代硫酸钠溶液。
① ClO2通入锥形瓶与酸性碘化钾溶液反应,反应的离子方程式为: 。
② 装置中玻璃液封管的作用是 、 。
③ 滴定至终点的现象是 。
④ 测得ClO2的质量m(ClO2)= 。(用含c、V的代数式表示)
-
碳酸钠俗称纯碱,在日常生产和生活中有着广泛的应用.某化学兴趣小组想根据所学知识模拟制备碳酸钠,方法如下:先以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3(反应的化学方程式为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl),然后再将NaHCO3制成Na2CO3.
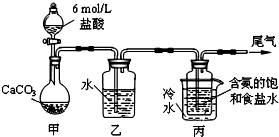
(1)装置乙的作用是__________.为防止污染空气,尾气中含有的__________需要进行吸收处理.
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有__________、__________、__________.
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了以下探究。取加热了t1min的NaHCO3样品19g完全溶于水制成溶液,然后向此溶液中不断滴加1mol•L﹣1的稀盐酸直到不再产生气泡,共消耗300ml稀盐酸.问该样品中NaHCO3和Na2CO3的物质的量之比是__________.
-
红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛。
实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。
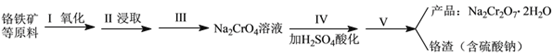
(1)步骤I中反应的化学方程式为:4FeO·Cr2O3(s)+8Na2CO3(s)+7O2 (g) 8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) △H<0该反应的化学平衡常数的表达式为__________________________。
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) △H<0该反应的化学平衡常数的表达式为__________________________。
(2)在常温下该反应速度极慢,下列措施中能使反应速率增大的是_____________________________ 。
a.升高温度 b.及时转移生成CO2 c.将原料粉碎 d.增加纯碱的用量
(3)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是__________________________、____________________________。
(4)步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是_____________________________________。
(5)步骤Ⅳ酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:_________________。
-
铝是应用广泛的金属,以铝土矿(主要成分为A12O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如图:
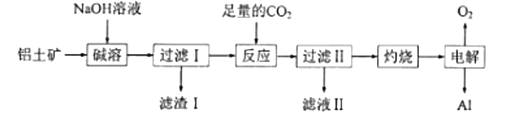
已知:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为__。
(2)“滤渣Ⅰ”的成分有___。
(3)向“过滤Ⅰ”所得滤液中通入足量的CO2,反应的离子方程式为___。
(4)“滤液Ⅱ”中加入足量的CaO,生成的__(填化学式)可循环利用。
(5)“灼烧”的化学方程式为___。
-
铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
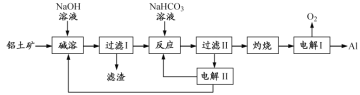
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为___________________________________________。
(2)“过滤Ⅰ”中所用到的玻璃仪器有___________________________________________。
(3)“过滤Ⅱ”中得到的固体中混有杂质,需要对沉淀进行洗涤,请你叙述如何洗涤?_______。