-
NO、NO2是常见的氧化物。用H2或CO催化还原NO可达到消除污染的目的。
已知:2NO(g)=N2(g)+O2(g) △H= -180.5 kJ⋅mol−1,2H2O(l)=2H2(g)+O2(g) △H=+571.6 kJ⋅mol−1。
(1)则用H2催化还原NO消除污染的热化学方程式是_______________。
(2)苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是:C8H10 (g) C8H8(g)+H2(g) △H=+120 kJ⋅mol−1,某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内气体物质的量,得到数据如表:
C8H8(g)+H2(g) △H=+120 kJ⋅mol−1,某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内气体物质的量,得到数据如表:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(C8H8)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
①当反应进行到20min时,该段时间内H2的平均反应速率是__________。
②该温度下,该反应的化学平衡常数是__________。
③若保持其他条件不变,用0.4molH2(g)和0.4molC8H8(g)合成C8H10(g),当有12kJ热量放出时,该反应中H2的转化率是______.此时,该合成反应是否达到了平衡状态?______(填“是”或“否”)。
-
汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应:N2(g) + O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。
2NO(g),是导致汽车尾气中含有NO的原因之一。
(1)已知H2或CO可以催化还原NO以达到消除污染的目的。N2(g) + O2(g) = 2NO(g) △H= +180.5 kJ·mol-1,2H2(g) + O2(g) = 2H2O(l) △H=-571.6 kJ·mol-1,则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是_________________________,判断该反应自发进行的条件:_______________(填“高温自发”或“低温自发”)。
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应:2NO(g) + 2CO(g) 2CO2(g) + N2(g)中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g) + N2(g)中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
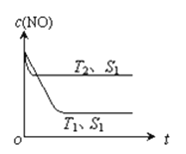
①则该反应的△H___0(填“>”或“<”)。
②若催化剂的表面积S1>S2 ,在该图中画出c(NO)在T1、S2条件下达到平衡过程中的变化曲线___。
(3)某小组往一恒温恒压容器充入9mol N2和23mol H2模拟合成氨反应,图C为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图.若体系在T2、60MPa下达到平衡.
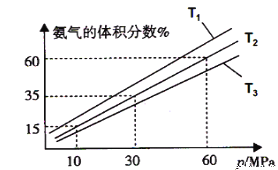
①能判断N2(g)+3H2(g)⇌2NH3(g)达到平衡的是___(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(N2)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②此时N2的平衡分压为_________MPa.(分压=总压×物质的量分数)。计算出此时的平衡常数Kp=__________(用平衡分压代替平衡浓度计算,结果保留2位有效数字)。
-
H2或CO可以催化还原NO以达到消除污染的目的。已知一定温度下
①N2(g)+O2(g)=2NO(g) ΔH1=+180.5kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1
③2CO(g)+O2(g)=2CO2(g) ΔH3=-566kJ·mol-1
下列有关说法错误的是( )
A.H2催化还原NO生成氮气和液态水的热化学方程式为:2H2(g)+2NO(g)=N2(g)+2H2O(l) ΔH=-752.1kJ·mol-1
B.汽车排气筒内安装尾气催化转化器可大大降低氮氧化物的排放
C.硝酸厂产生的尾气只要通入一定量氢气即可达到排放标准
D.CO催化还原NO生成无污染的气体33.6L(标准状况),放出热量为373.25kJ
-
用NH3催化还原NxOy可以消除氮氧化物的污染。
已知:反应I: 4NH3(g)+6NO(g)  5N2(g)+6H2O(l) ΔH1
5N2(g)+6H2O(l) ΔH1
反应II: 2NO(g)+O2(g)  2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
反应III:4NH3(g)+6NO2(g)  5N2(g)+3O2(g)+6H2O(l) ΔH3
5N2(g)+3O2(g)+6H2O(l) ΔH3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 |
| 398 | K1′ | K2′ |
(1)ΔH3=____________(用ΔH1、ΔH2的代数式表示);推测反应III是________反应(填“吸热”或“放热”)。
(2)相同条件下,反应I在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①计算0~4分钟在A催化剂作用下,反应速率v(NO)=______________。
②下列说法不正确的是_______。
A.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如右。溶液中OH−向电极____移动(填a或b),负极的电极反应式为________________。

-
用NH3催化还原NxOy可以消除氮氧化物的污染。
已知:反应I:4NH3(g)+6NO(g) 5N2(g)+6H2O(l) ΔH1
5N2(g)+6H2O(l) ΔH1
反应II:2NO(g)+O2(g) 2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
2NO2(g) ΔH2(且|ΔH1|=2|ΔH2|)
反应III:4NH3(g)+6NO2(g) 5N2(g)+3O2(g)+6H2O(l) ΔH3
5N2(g)+3O2(g)+6H2O(l) ΔH3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 |
| 398 | K1′ | K2′ |
(1)ΔH3=_________(用ΔH1、ΔH2的代数式表示);推测反应III是________反应(填“吸热”或“放热”)。
(2)相同条件下,反应I在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。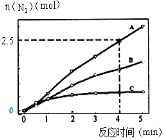
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=______________。
②下列说法不正确的是__________。
A.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如右。溶液中OH−向电极___________移动(填a或b),负极的电极反应式为________________。

-
汽车尾气中含有一氧化氮和一氧化碳,消除这两种物质产生的大气污染的方法是安装催化转换器,使它们发生反应生成CO2和N2。反应方程式为:2CO+2NO2 CO2+N2,其中NO2是
CO2+N2,其中NO2是
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
-
为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量.
(1)用CH4催化还原煤燃烧产生的氮氧化物,可以消除污染.
已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol
NO2(g)═ N2O4(g) △H=-28.5kJ/mol
N2O4(g) △H=-28.5kJ/mol
写出CH4催化还原N2O4(g)生成CO2、N2和H2O(g)的热化学方程式_____________。
(2)一定条件下,将2mol NO2与4molSO2置于恒温体积为2L的恒容密闭容器中,发生:NO2(g)+SO2(g)═SO3(g)+NO(g),10s时反应达到平衡,测得平衡时c(NO2)=0.25mol/L,则10s内反应的平均速率v(SO2)=____________;达到平衡时NO2转化率=____________;计算该温度下该反应的化学平衡常数K= _____________(填数值)。
(3)将CO2与NH3混合,在一定条件下反应合成尿素,可以保护环境、变废为宝,反应原理为:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H
CO(NH2)2(s)+H2O(g) △H
该反应在一定条件下能自发进行的原因是____________;若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是_____________(填序号)。
a.CO2与H2O(g)浓度相等 b.容器中气体的压强不再改变
C.2v(NH3)正=v(H2O)逆 d.容器中混合气体的密度不再改变
(4)研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。有人利用如图所示装置(均为惰性电极)从海水中提取CO2(海水中无机碳95%以HCO3-存在),有利于减少环境中温室气体含量。
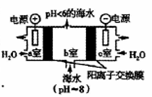
①a室的电极反应式为___________________。
②b室中提取CO2的反应的离子方程式为 ___________________。
③b室排出的海水(pH <6)不可直接排回大海,需用该装置中产生的物质对b室排出的海水进行处理,合格后才能排回大海。处理的方法是___________________。
-
氮的氧化物是严重的大气污染物,可以通过以下方法处理:
Ⅰ.催化还原法:如在汽车排气管上安装一个催化转化器,发生如下反应: 2NO(g)+2CO(g)⇌N2(g)+2CO2(g)
(1)已知N2(g)+O2(g)⇌2NO(g) △H=+180kJ/mol
| 化学键 | O=O | C=O | C≡O |
| 键能(kJ/mol) | 497 | 803 | 1072 |
则反应:2NO(g)+2CO(g) ⇌N2(g)+2CO2(g) △H=_____kJ/mol。
(2)在一定温度下,向体积为1L的密闭容器中充入2molNO、1molCO,10分钟时反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图所示:
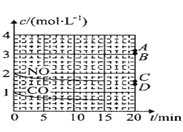
①该反应的平衡常数 K 的计算式为_____;前 10 分钟内用氮气表示的反应速率为_____。
②若保持温度不变,15 分钟时再向该容器中充入1.6molNO、0.4molCO2,则此时反应的ν正______ν逆(填“>”、“=”或“<”)。
③若保持其他条件不变,15min 时压缩容器的体积至 0.5L,20 分钟时反应重新达到平衡,NO 的浓度对应的点应是图中的_____(填字母)。
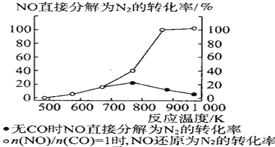
④某科研小组研究发现以 Ag-ZSM-5 为催化剂,NO 转化为 N2 的转化率随温度变化情况如图所示。若不使用 CO,温度超过775K,发现NO的分解率降低,其可能的原因是__________________
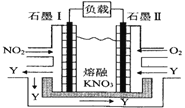
Ⅱ.利用电化学原理,将 NO2、O2和熔融 KNO3制成燃料电池,其原理如图,该电池在工作过程中NO2转变成绿色硝化剂Y,Y是一种氧化物,可循环使用,石墨Ⅰ附近发生的反应电极反应式为_____相同条件下,消耗的 O2和 NO2的体积比为_____
-
(5分)H2可以催化还原NO以达到消除污染的目的:
(1)已知:①

②

则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式为: ________________。
(2)一定条件下,在体积为2 L的容器中通入1 mol H2和l mol NO气体生成N2(g)和H2O(l),该反应达平衡时,容器内的压强是反应起始时的40%。保持其它条件不变,只往容器中再通入1 mol H2,计算反应再达新平衡时,化学平衡常数为__________。
-
消除氮氧化物(主要为NO和NO2)污染是“蓝天计划”的重要内容之一。
(1)甲烷还原方法是在催化剂作用下可消除氮氧化物(主要为NO和NO2)污染, NO、O2和CH4的混合物反应体系主要发生如下反应:
2NO(g) + O2(g) 2NO2(g) ΔH=-113.0 kJ•mol-1 ①
2NO2(g) ΔH=-113.0 kJ•mol-1 ①
CH4(g) + 2O2(g) CO2(g) +2H2O (g) ΔH=-802. 3 kJ•mol-1 ②
CO2(g) +2H2O (g) ΔH=-802. 3 kJ•mol-1 ②
CH4(g) + 4NO(g) 2N2(g) + CO2(g) + 2H2O (g) ΔH=-1160 kJ•mol-1 ③
2N2(g) + CO2(g) + 2H2O (g) ΔH=-1160 kJ•mol-1 ③
① 则反应CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O (g) 的ΔH= ______。
N2(g)+CO2(g)+2H2O (g) 的ΔH= ______。
② 反应CH4(g) + 2O2(g) CO2(g) +2H2O (l) ΔH=-a kJ•mol-1,则a ____ 802. 3(填“>”、“<”或“=”)。
CO2(g) +2H2O (l) ΔH=-a kJ•mol-1,则a ____ 802. 3(填“>”、“<”或“=”)。
③ 在一定温度下,提高反应③中NO 转化率可采取的措施是 _____。
(2)利用电化学装置可消除氮氧化物污染,变废为宝。
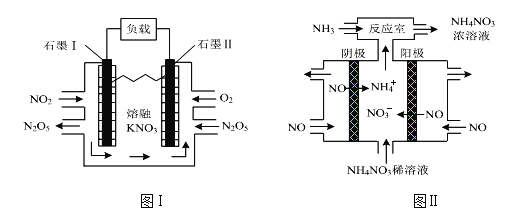
① 图Ⅰ装置实现的能量转化形式是_____。石墨Ⅱ电极上发生的电极反应方程式为_____。相同条件下,放电过程中消耗的NO2和O2的体积比为_____。
② 图Ⅱ为电解NO制备NH4NO3的装置。该装置中阳极的电极反应式为_____。“反应室”中发生反应的离子方程式为_____。
C8H8(g)+H2(g) △H=+120 kJ⋅mol−1,某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内气体物质的量,得到数据如表:










