-
环戊烯是生产精细化工产品的重要中间体,其制备涉及的反应如下:
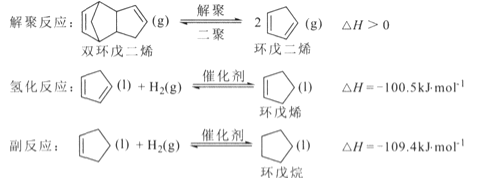
回答下列问题:
(l)反应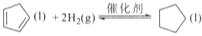 的△H= _________ kJ/mol 。
的△H= _________ kJ/mol 。
(2)解聚反应在刚性容器中进行。
①其他条件不变,有利于提高双环戊二烯平衡转化率的条件是 ____ (填标号).
A.升高温度 B.降低温度 C.增大压强 D.减小压强
②实际生产中常通入水蒸气以降低双环戊二烯的沸点。某温度下,通入总压为l00kPa的双环戊二烯和水蒸气,达到平衡后总压为160kPa,双环戊二烯的转化率为8 0%,则 pH2O=___kpa,平衡常数Kp=______kPa (Kp为以分压表示的平衡常数)
(3) 一定条件下,将环戊二烯溶于有机溶剂中进行氢化反应,反应过程中保持氢气压力不变,测得环戊烯和环戊烷的产率(以环戊二烯为原料计)随时间变化如下图所示。
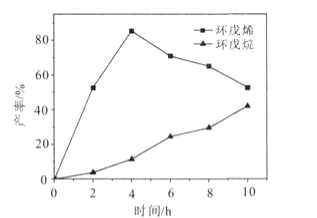
①将环戊二烯溶于有机溶剂中可减少二聚反应的发生,原因是____,
②最佳的反应时间为__h。活化能较大的是__(填“氢化反应”或“副反应”)。
(4)已知氢化反应平衡常数为1.6 × 1012,副反应的平衡常数为2.0×10l2。在恒温恒容下,环戊二烯与氢气按物质的量之比为1:1进行反应,则环戊二烯的含量随时间变化趋势是____(不考虑环戊二烯的二聚反应)。
-
环戊烯是生产精细化工产品的重要中间体,其制备涉及的反应如下:
氢化反应: (l)+H2(g)
(l)+H2(g)
 (环戊烯)(l) ∆H=-100.5 kJ/mol
(环戊烯)(l) ∆H=-100.5 kJ/mol
副反应: (l)+H2(g)
(l)+H2(g)
 (环戊烷)(l) ∆H=-109.4 kJ/mol
(环戊烷)(l) ∆H=-109.4 kJ/mol
解聚反应: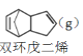
 2
2 (g) ∆H>0
(g) ∆H>0
回答下列问题:
(1)反应 (l)+2H2(g)
(l)+2H2(g)
 (l)的△H=_________ kJ/mol。
(l)的△H=_________ kJ/mol。
(2)一定条件下,将环戊二烯溶于有机溶剂进行氢化反应(不考虑二聚反应),反应过程中保持氢气压力不变,测得环戊烯和环戊烷的产率(以环戊二烯为原料计)随时间变化如图所示:
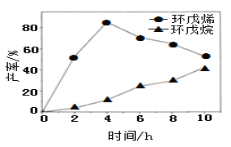
①0~4 h氢化反应速率比副反应快的可能原因是___________________。
②最佳的反应时间为_________h。若需迅速减慢甚至停止反应,可采取的措施有__________________(写一条即可)。
③一段时间后,环戊烯产率快速下降的原因可能是_____________________。
(3)解聚反应在刚性容器中进行(不考虑氢化反应和副反应)。
①其他条件不变,有利于提高双环戊二烯平衡转化率的是________(填标号)。
A.增大双环戊二烯的用量 B.使用催化剂 C.及时分离产物 D.适当提高温度
②实际生产中常通入水蒸气以降低双环戊二烯的温度(水蒸气不参与反应)。某温度下,通入总压为300 kPa的双环戊二烯和水蒸气,达到平衡后总压为500 kPa,双环戊二烯的转化率为80%,则 p(H2O)=________kPa,平衡常数Kp=__________kPa (Kp为以分压表示的平衡常数)。
-
环戊烯是生产精细化工产品的重要中间体,其工业制备原理如图1。以Pd/Al2O3为催化剂,在相同反应时间内,测得不同温度下(其他条件相同)环戊二烯转化率与环戊烯产率的变化曲线如图2。下列说法正确的是()
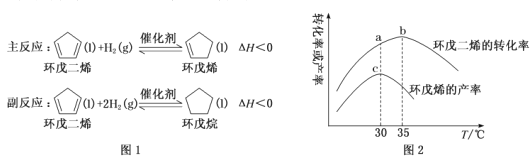
A.环戊二烯的转化率越大,越有利于环戊烯的生成
B.a点是主反应的平衡转化率,b点是副反应的平衡转化率
C.30℃~35℃之间环戊烯产率变化趋势与环戊二烯转化率不一致,原因是主反应被抑制,使环戊烯产率降低
D.30℃时催化剂的选择性最好,有利于提高生成环戊烯的平衡转化率
-
环戊二烯是重要的有机化工原料,制备环戊烯涉及的反应如下:
ⅰ.解聚反应: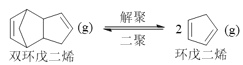 ΔH>0
ΔH>0
ⅱ.氢化反应: ΔH=-100.5kJ·mol-1
ΔH=-100.5kJ·mol-1
ⅲ.副反应: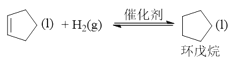 ΔH=-109.4kJ·mol-1
ΔH=-109.4kJ·mol-1
(1)反应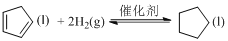 的∆H=__kJ·mol-1。
的∆H=__kJ·mol-1。
(2)解聚反应ⅰ在刚性容器中进行。
①其它条件不变时,有利于提高双环戊二烯平衡转化率的条件是__,__。
②实际生产中常通入水蒸气以降低双环戊二烯的沸点。某温度下,通入总压为70kPa的双环戊二烯和水蒸气,达到平衡后总压为115kPa,双环戊二烯的转化率为90%,则体系中PH2O=__kPa。
(3)研究环戊二烯氢化制备环戊烯在不同温度下催化剂的活性。下表是以Pd/Al2O3为催化剂,相同反应时间测得不同温度的数据(其它条件相同)。
| 温度/℃ | 25 | 30 | 35 | 40 | 45 |
| 环戊二烯转化率/% | 84.9 | 93.9 | 100.0 | 100.0 | 100.0 |
| 环戊烯选择性/% | 81.3 | 88.6 | 75.5 | 60.6 | 51.3 |
说明:选择性= ×100%,收率=
×100%,收率= ×100%,
×100%,
常用收率来衡量催化剂的活性。
①最佳的反应温度为__,选择该温度的原因是__。
②表中实验数据表明,升高温度,环戊二烯转化率提高而环戊烯选择性降低,其原因是__。
-
环戊二烯是重要的有机化工原料,制备环戊烯涉及的反应如下:
ⅰ.解聚反应: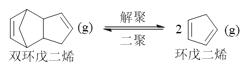 ΔH>0
ΔH>0
ⅱ.氢化反应: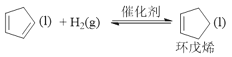 ΔH=-100.5kJ·mol-1
ΔH=-100.5kJ·mol-1
ⅲ.副反应: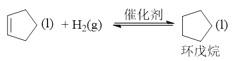 ΔH=-109.4kJ·mol-1
ΔH=-109.4kJ·mol-1
(1)反应 的∆H=__kJ·mol-1。
的∆H=__kJ·mol-1。
(2)解聚反应ⅰ在刚性容器中进行。
①其它条件不变时,有利于提高双环戊二烯平衡转化率的条件是__,__。
②实际生产中常通入水蒸气以降低双环戊二烯的沸点。某温度下,通入总压为70kPa的双环戊二烯和水蒸气,达到平衡后总压为115kPa,双环戊二烯的转化率为90%,则体系中PH2O=__kPa。
(3)研究环戊二烯氢化制备环戊烯在不同温度下催化剂的活性。下表是以Pd/Al2O3为催化剂,相同反应时间测得不同温度的数据(其它条件相同)。
| 温度/℃ | 25 | 30 | 35 | 40 | 45 |
| 环戊二烯转化率/% | 84.9 | 93.9 | 100.0 | 100.0 | 100.0 |
| 环戊烯选择性/% | 81.3 | 88.6 | 75.5 | 60.6 | 51.3 |
说明:选择性= ×100%,收率=
×100%,收率= ×100%,
×100%,
常用收率来衡量催化剂的活性。
①最佳的反应温度为__,选择该温度的原因是__。
②表中实验数据表明,升高温度,环戊二烯转化率提高而环戊烯选择性降低,其原因是__。
-
环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
环戊二烯可用于制备二茂铁(Fe(C5H5)2,结构简式为 ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
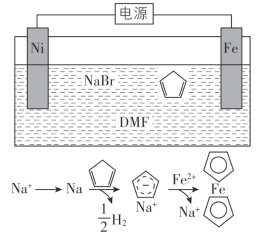
该电解池的阳极为____________,总反应为__________________。电解制备需要在无水条件下进行,原因为_________________________。
-
氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取。反应原理、实验装置图(加热装置都已略去)如下:
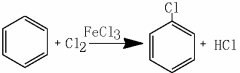
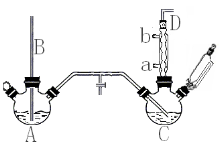
已知:氯苯为无色液体,沸点132.2℃。
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是 。冷凝管中冷水应从 (填“a”或“b”) 处通入。
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯。
①对C加热的方法是 (填序号)
酒精灯加热 b.油浴加热 c.水浴加热
②D出口的气体成分有HCl、 和 。
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏。碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本。写出用10%氢氧化钠碱洗时可能发生的化学反应方程式: ; (写两个即可)。
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是 。
(5)工业生产中苯的流失情况如下:
| 项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
则1t苯可制得成品为 t(只要求列式)。
-
呋喃酚是生产呋喃丹、好安威等农药的主要中间体,是高附加值的精细化工产品.一种以邻氯苯酚(A)为主要原料合成呋喃酚(F)的流程如下:

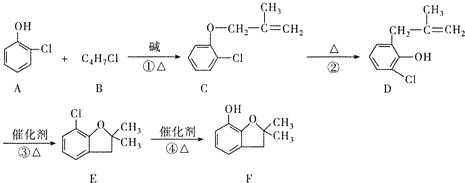
回答下列问题:
(1)A 物质核磁共振氢谱共有 个峰,④的反应类型是 ,C和D中含有的相同官能团的名称是 .
(2)下列试剂中,能和D反应的有 (填标号).
A.溴水 B.酸性K2Cr2O7溶液 C.FeC12溶液 D.纯碱溶液
(3)写出反应①的化学方程式是 (有机物用结构简式表示,下同).
(4)有机物B可由异丁烷经三步反应合成:异丁烷 X
X Y
Y
 有机物B条件a为 ,Y生成B的化学方程式为 .
有机物B条件a为 ,Y生成B的化学方程式为 .
(5)呋喃酚的同分异构体很多,写出符合下列条件的所有同分异构体的结构简式
①苯环上的一氯代物只有一种
②能发生银镜反应的芳香酯.
-
呋喃酚是生产呋喃丹、好安威等农药的主要中间体,是高附加值的精细化工产品.一种以邻氯苯酚(A)为主要原料合成呋喃酚(F)的流程如下:

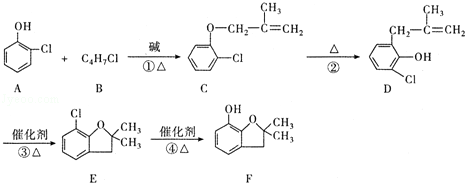
回答下列问题:
(1)A 物质核磁共振氢谱共有 个峰,④的反应类型是 ,C和D中含有的相同官能团的名称是  .
.
(2)下列试剂中,能和D反应的有 (填标号).
A.溴水 B.酸性K2Cr2O7溶液 C.FeC12溶液 D.纯碱溶液
(3)写出反应①的化学方程式是 (有机物用结构简式表示,下同).
(4)有机物B可由异丁烷经三步反应合成:异丁烷 X
X Y
Y
 有机物B条件a为 ,Y生成B的化学方程式为 .
有机物B条件a为 ,Y生成B的化学方程式为 .
(5)呋喃酚的同分异构体很多,写出符合下列条件的所有同分异构体的结构简式
①苯环上的一氯代物只有一种
②能发生银镜反应的芳香酯.
-
乙烯是一种重要的化工原料,以乙烯为原料衍生出部分化工产品的反应如下(部分反应条件已略去,本题涉及的有机物类别有:烯烃;环氧烷;醇;羧酸;酯;另提示:D→E是开环加成反应)
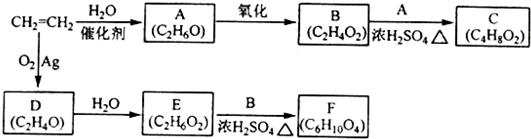
请回答下列问题:
(1)A的化学名称是______;
(2)B和A反应生成C的化学方程式为______,该反应的类型为______;
(3)D的结构简式为______;
(4)F的结构简式为______;
(5)D的同分异构体的结构简式为______.
(l)+H2(g)
(环戊烯)(l) ∆H=-100.5 kJ/mol
(l)+H2(g)
(环戊烷)(l) ∆H=-109.4 kJ/mol

2
(g) ∆H>0
(l)+2H2(g)
(l)的△H=_________ kJ/mol。


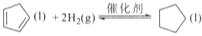 的△H= _________ kJ/mol 。
的△H= _________ kJ/mol 。

 ΔH>0
ΔH>0 ΔH=-100.5kJ·mol-1
ΔH=-100.5kJ·mol-1 ΔH=-109.4kJ·mol-1
ΔH=-109.4kJ·mol-1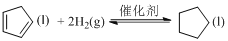 的∆H=__kJ·mol-1。
的∆H=__kJ·mol-1。 ×100%,收率=
×100%,收率= ×100%,
×100%, ΔH>0
ΔH>0 ΔH=-100.5kJ·mol-1
ΔH=-100.5kJ·mol-1 ΔH=-109.4kJ·mol-1
ΔH=-109.4kJ·mol-1 的∆H=__kJ·mol-1。
的∆H=__kJ·mol-1。 ×100%,收率=
×100%,收率= ×100%,
×100%,




