-
工业上常用亚硝酸钠 作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备
作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备 并探究NO、
并探究NO、 的某一化学性质
的某一化学性质 中加热装置已略去
中加热装置已略去 。请回答下列问题:
。请回答下列问题:
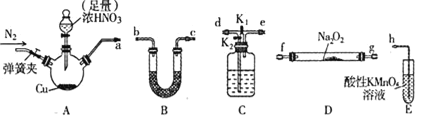
已知:①2NO+Na2O2=2NaNO2
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+
(1)装置A三颈烧瓶中发生反应的化学方程式为____________。
(2)用上图中的装置制备 ,其连接顺序为:
,其连接顺序为: ___
___ ____
____ ___
___ ___
___ ___
___ ___
___ 按气流方向,用小写字母表示
按气流方向,用小写字母表示 ,此时活塞
,此时活塞 、
、 如何操作____________。
如何操作____________。
(3) 装置发生反应的离子方程式是________________。
装置发生反应的离子方程式是________________。
(4)通过查阅资料, 或NO可能与溶液中
或NO可能与溶液中 发生反应。某同学选择上述装置并按
发生反应。某同学选择上述装置并按 顺序连接,E中装入
顺序连接,E中装入 溶液,进行如下实验探究。
溶液,进行如下实验探究。
| 步骤 | 操作及现象 |
| ① | 关闭K2,打开K1,打开弹簧夹通一段时间的氮气,夹紧弹簧夹,开始A中反应,一段时间后,观察到E中溶液逐渐变为深棕色。 |
| ② | 停止A中反应,打开弹簧夹和K2、关闭K1,持续通入N2一段时间 |
| ③ | 更换新的E装置,再通一段时间N2后关闭弹簧夹,使A中反应继续,观察到的现象与步骤①中相同 |
步骤②操作的目的是___________;步骤③C瓶中发生的化学方程式为_________________;通过实验可以得出:___________ 填“
填“ 、NO中的一种或两种”
、NO中的一种或两种” 和溶液中
和溶液中 发生反应使溶液呈深棕色。
发生反应使溶液呈深棕色。
-
工业上常用亚硝酸钠(NaNO2)作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备NaNO2并探究NO、NO2的某一化学性质(A中加热装置已略去)。

已知:①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+
请回答下列问题:
(1)装置A三颈烧瓶中发生反应的化学方程式为__________________。
(2)用上图中的装置制备NaNO2,其连接顺序为:a→_____________→h(按气流方向,用小写字母表示),此时活塞K1、K2如何操作_______________________。
(3)E装置发生反应的离子方程式是________________________。
(4)通过查阅资料,NO2或NO可能与溶液中Fe2+发生反应。某同学选择上述装置并按A→C→E顺序连接,E中装入FeSO4溶液,进行如下实验探究。

步骤②操作的目的是__________________;步骤③C瓶中发生的化学方程式为________________;
通过实验可以得出:___________(填“NO2、NO中的一种或两种”)和溶液中Fe2+发生反应使溶液呈深棕色。
-
工业上亚硝酸钠可用作媒染剂、缓蚀剂等。实验室以铜、浓硝酸、氢氧化钠为原料制备亚硝酸钠的装置如图所示(部分夹持装置略)。已知:NO和NO2‑均能被酸性KMnO4溶液氧化为NO3-。
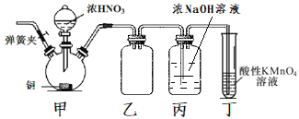
(1)连接装置后首先要进行的操作是___,然后装入药品。
(2)装置甲中反应的离子方程式为___。
(3)装置乙的作用是___。
(4)实验结束后,打开甲装置的弹簧夹,通入N2,其目的是___。
(5)装置丁的作用是___。
(6)为了测定丙中NaNO2的浓度,取丙中溶液20.00mL,用0.1000mol/L的酸性KMnO4溶液进行滴定,消耗KMnO4溶液10.00mL。请回答:
①酸性KMnO4溶液盛放在___滴定管中。
②判断滴定达终点时的依据为___。
③写出上述反应的离子方程式___,计算出NaNO2的浓度为___mol/L。
④配制酸性KMnO4溶液定容时,俯视容量瓶的刻度线,NaNO2的浓度___。(填“偏高”、“偏低”或“无影响”)
-
Fe(NO3)3是一种重要的媒染剂和金属表面处理剂,易溶于水、乙醇,微溶于硝酸,具有较强的氧化性。某学习小组利用如图装置制备Fe(NO3)3并探究其性质。
回答下列问题:
步骤一:制备Fe(NO3)3
a中加入100mL8mol·L-1硝酸,b中加入5.6g铁屑,将硝酸与铁屑混合后水浴加热。

(1)仪器b的名称是___。
(2)反应过程中观察到b中铁屑溶解,溶液变黄色,液面上方有红棕色气体产生,仪器b中反应的离子方程式是___。
(3)c中所盛试剂是___,倒扣漏斗的作用是___。
(4)若要从反应后的溶液中得到Fe(NO3)3晶体,应采取的操作是:将溶液蒸发浓缩、冷却结晶、过滤、用____洗涤、干燥。
步骤二:探究Fe(NO3)3的性质
i.测得0.1mol·L-1Fe(NO3)3溶液的pH约等于1.6。
ii.将5mL0.1mol·L-1Fe(NO3)3溶液倒入有银镜的试管中,约1min后银镜完全溶解。
(5)使银镜溶解的原因可能有两个:a.NO3−(H+)使银镜溶解;b.__使银镜溶解。为证明b成立,设计如下方案:取少量银镜溶解后的溶液于另一支试管中,___。
-
亚硝酸钠广泛用于印染漂白、食品等行业,常作媒染剂、漂白剂、食品添加剂等。某兴趣小组用下列装證制备NaNO2。
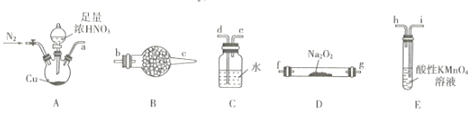
已知:①2NO+Na2O2=2NaNO2; ②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。
请回答下列问题:
(1)利用上图中的装置制备NaNO2,其连接顺序为a→__________ ( 按气流方向,用小写字母表示)。
(2)实验开始时,先通一段时间N2的目的是__________。
(3)装置B中盛放试剂的名称为____,装置C的作用是_______。
(4)装置E中发生反应的离子方程式为_____________。
(5)为测定亚硝酸钠的含量,称取3.000g样品溶于水配成500mL.溶液,量取25.00mL溶液于锥形瓶中,硫酸酸化后加入过量KI,发生反应:2NO2-+2I-+4H+=2NO↑+I2+2H2O(杂质不参与反应)。然后用0.1000mol/LNa2S2O3标准溶液滴定至终点(发生反应:I2+2S2O32-=S4O62-+2I-),消耗20.00mL。
①该实验可选用的指示剂为_____,达到滴定终点时的现象是__________。
②所得样品中亚硝酸钠的质量分数为____________。
③下列操作会导致测定结果偏高的是_______(填代号)。
a.滴定过程中向锥形瓶中加少量水
b.消定前滴定管尖嘴部分有气泡,滴定后气泡消失
c.读数时,滴定前仰视,滴定后府视
d.滴定时,标准被滴到锥形瓶外
-
亚硝酸钠广泛用于媒染剂、漂白剂等。某兴趣小组用下列装置制取较纯净的NaNO2。
甲 乙
乙 丙
丙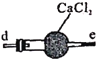 丁
丁
反应原理为:2NO+Na2O2=2NaNO2。已知:NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。下列分析错误的是
A.甲中滴入稀硝酸前需通人N2
B.仪器的连接顺序为a-f-g-d-e-b
C.丙中CaCl2用于干燥NO
D.乙中吸收尾气时发生的离子反应为3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O
-
过硫酸钠 常用作漂白剂、氧化剂等。某研究小组利用如图装置制备
常用作漂白剂、氧化剂等。某研究小组利用如图装置制备 并探究其性质
并探究其性质 加热及夹持仪器略去
加热及夹持仪器略去 。
。
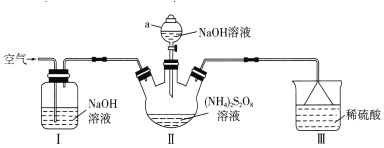
已知:





⑴仪器a的名称是______。装置Ⅰ中NaOH溶液的作用是______。
⑵装置Ⅱ发生反应的同时,需要持续通入空气的目的是______。
⑶装置Ⅲ的作用是______。
⑷ 溶液与铜反应只生成两种盐,且反应先慢后快。
溶液与铜反应只生成两种盐,且反应先慢后快。
①该反应的化学方程式为______。
②某同学推测反应先慢后快的原因可能是生成的 对反应起催化作用。设计实验方案验证该推测是否正确______。(供选试剂:Cu、
对反应起催化作用。设计实验方案验证该推测是否正确______。(供选试剂:Cu、 溶液、
溶液、 溶液、
溶液、 溶液、蒸馏水)
溶液、蒸馏水)
⑸测定产品纯度:称取 样品,用蒸馏水溶解,加入过量KI,充分反应后,再滴加几滴指示剂,用
样品,用蒸馏水溶解,加入过量KI,充分反应后,再滴加几滴指示剂,用 标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为
标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为 。(已知:
。(已知: )
)
①选用的指示剂是______;达到滴定终点的现象是______。
②样品的纯度为______%。
-
氰化钠是一种剧毒物质,工业上常用硫代硫酸钠溶液处理废水中的氰化钠。硫代硫酸钠的工业制备原理为:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2 。某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并检测氰化钠废水处理排放情况。
I.实验室通过如图所示装置制备Na2S2O3
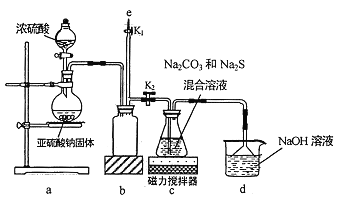
(1)实验中要控制SO2生成速率,可采取的措施有_____________(写出一条)。
(2)b装置的作用是_____________ 。
(3)反应开始后,c 中先有淡黄色浑浊产生,后又变为澄清,此浑浊物为__________(填化学式)。
(4)实验结束后,在e处最好连接盛__________(填“NaOH 溶液”、“水”、“CCl4”中的一种) 的注射器,接下来的操作为______________,最后拆除装置。
II.氰化钠废水处理
(5)已知: a.废水中氰化钠的最高排放标准为0.50mg/L;
b.Ag++2CN-==[Ag(CN)2]-,Ag++I-=AgI↓,AgI 呈黄色,且CN-优先与Ag+反应。
实验如下: 取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
①滴定时1.00×10-4mol/L的标准AgNO3溶液应用________(填仪器名称) 盛装; 滴定终点时的现象是______________。
②处理后的废水是否达到排放标准_______(填“是”或“否”)。
-
氰化钠是一种剧毒物质,工业上常用硫代硫酸钠溶液处理废水中的氰化钠。硫代硫酸钠的工业制备原理为:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2 。某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并检测氰化钠废水处理排放情况。
I.实验室通过如图所示装置制备Na2S2O3
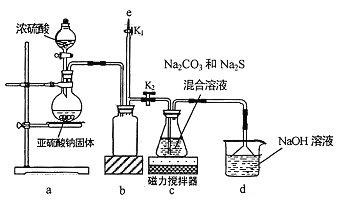
(1)实验中要控制SO2生成速率,可采取的措施有_____________(写出一条)。
(2)b装置的作用是_____________ 。
(3)反应开始后,c 中先有淡黄色浑浊产生,后又变为澄清,此浑浊物为__________(填化学式)。
(4)实验结束后,在e处最好连接盛__________(填“NaOH 溶液”、“水”、“CCl4”中的一种) 的注射器,接下来的操作为______________,最后拆除装置。
II.氰化钠废水处理
(5)已知: a.废水中氰化钠的最高排放标准为0.50mg/L;
b.Ag++2CN-==[Ag(CN)2]-,Ag++I-=AgI↓,AgI 呈黄色,且CN-优先与Ag+反应。
实验如下: 取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
①滴定时1.00×10-4mol/L的标准AgNO3溶液应用________(填仪器名称) 盛装; 滴定终点时的现象是______________。
②处理后的废水是否达到排放标准_______(填“是”或“否”)。
-
过硫酸钠(Na2S2O8)常用作漂白剂、氧化剂等。某研究小组利用下图装置制备Na2S2O8并探究其性质(加热及夹持仪器略去)。
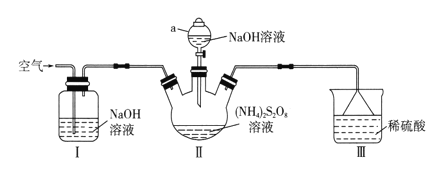
已知:①(NH4)2S2O8+2NaOH Na2S2O8+2NH3+2H2O
Na2S2O8+2NH3+2H2O
②2NH3+3Na2S2O8+6NaOH 6Na2SO4+N2+6H2O
6Na2SO4+N2+6H2O
(1)仪器a的名称是________________。装置I中NaOH溶液的作用是___________。
(2)装置II发生反应的同时,需要持续通入空气的目的是_______________________。
(3)装置III的作用是__________________________。
(4)Na2S2O8溶液与铜反应只生成两种盐,且反应先慢后快。
①该反应的化学方程式为___________________________。
②某同学推测反应先慢后快的原因可能是生成的Cu2+对反应起催化作用。设计实验方案验证该推测是否正确___________。(供选试剂:Cu、Na2S2O8溶液、CuSO4溶液、Cu(NO3)2溶液、蒸馏水)
(5)测定产品纯度:称取0.2500g样品,用蒸馏水溶解,加入过量KI,充分反应后,再滴加几滴指示剂,用0.1000mol/LNa2S2O8标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为19.50mL。(已知:I2+2S2O32-=S4O62-+2I-)
①选用的指示剂是____________;达到滴定终点的现象是______________________。
②样品的纯度为___________%。
作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备
并探究NO、
的某一化学性质
中加热装置已略去
。请回答下列问题:

,其连接顺序为:
___
____
___
___
___
___
按气流方向,用小写字母表示
,此时活塞
、
如何操作____________。
装置发生反应的离子方程式是________________。
或NO可能与溶液中
发生反应。某同学选择上述装置并按
顺序连接,E中装入
溶液,进行如下实验探究。
填“
、NO中的一种或两种”
和溶液中
发生反应使溶液呈深棕色。





 乙
乙 丙
丙 丁
丁



